Resultats de la cerca
Es mostren 8 resultats
licor
Farmàcia
Química
Dissolució en una proporció determinada de substàncies medicinals o de reactius químics en un solvent, generalment aquós.
Sovint reben diversos noms, com licor de Fehling , de Schweitzer , etc En farmàcia són coneguts el licor amoniacal anisat amoníac, alcohol i essència d’anís, el de Hoffmann èter i alcohol, el de Fowler arsenat potàssic i aigua i el de Van Swieten clorur mercúric, alcohol i aigua
mètode de Kjeldahl
Química
Mètode emprat per a la determinació del nitrogen amoniacal.
Es fonamenta en la transformació de la substància nitrogenada en sulfat amònic, per digestió amb àcid sulfúric en presència de sulfat de coure com a catalitzador Hom destilla finalment el líquid per a recollir l’amoníac sobre una solució valorada d’un àcid inorgànic
amoníac

Propietats físiques de l’amoníac
©
Química
Gas incolor, més lleuger que l’aire, compost de nitrogen i hidrogen.
L’amoníac té una olor pungent característica i irrita els ulls i les vies respiratòries El llindar de percepció se situa a 0,04 g/m 3 53 ppm i la màxima concentració tolerable és de 0,3%o en volum a 4-5%₀ esdevé mortal En la natura, l’amoníac es forma en la descomposició de la matèria orgànica nitrogenada i hom el troba, en petita quantitat, a l’atmosfera i en moltes aigües naturals La solució aquosa d’amoníac era ja coneguda dels alquimistes al segle XV Priestley l’aïllà a l’estat gasós el 1774 i Berthollet establí la seva composició el 1785 La molècula d’amoníac és piramidal, amb el …
trimetilamina
Química
Amina alifàtica gasosa, d’olor amoniacal característica, altament inflamable, miscible amb aigua i amb els solvents orgànics, que bull a 2,9°C.
Hom l’obté per reacció del metanol amb amoníac a alta temperatura i en presència de catalitzadors metàllics Presenta caràcter bàsic pK b = 4,26, i és emprada en síntesi orgànica, especialment en la preparació de sals d’amoni, en la manufactura de desinfectants, com a agent de flotació i atraient d’insectes
aldehid
Química
Nom genèric de les substàncies orgàniques caracteritzades per la presència del grup funcional
(carbonil unit a un hidrogen).
Segons les regles de nomenclatura de la IUPAC, els aldehids alifàtics RCHO es designen afegint al nom de l’hidrocarbur RCH₃ el sufix -al , tot preservant la n etimològica p ex metà →metà- n -al, i els aldehids amb el grup funcional directament fixat a un sistema cíclic, afegint el sufix -carbaldehid al nom d’aquest Exemples 2-metilbutanal CH₃CH₂CHCH₃CHO ciclopentacarbaldehid Això no obstant, si la molècula conté un altre grup prioritari en nomenclatura, els aldehids es designen amb el prefix formil - Exemple àcid p -formilfenilacètic Quan l’àcid RCOOH porta un nom trivial, l’aldehid RCHO pot…
al·lilamina
Química
Líquid miscible amb aigua i amb els solvents orgànics, de forta olor amoniacal, esternutatori i lacrimogen, que bull a 55-58°C i és utilitzat com a intermediari en la indústria farmacèutica.
cobalt
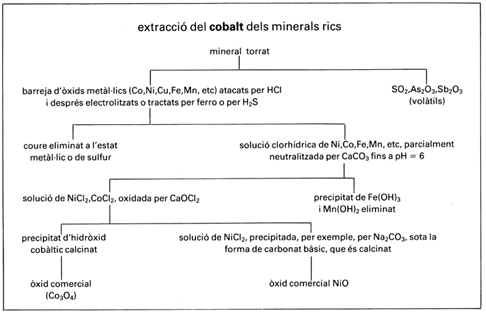
Extracció del cobalt de minerals rics
Química
Tecnologia
Element de transició del bloc d, situat entre els elements del bloc s i els del bloc p de la taula periòdica; el nom li ve de l’alemany kobold, que significa ‘fetiller’.
Té un sol isòtop natural el núclid 59, i 10 núclids artificials 54, 55, 56, 57, 58 i 58 m, 60 i 60 m, 61 i 62 Metall blanc, dúctil i malleable, descobert per Georg Brandt el 1735 Graus d’oxidació del coballt el +3, el +2, que és l’únic estable per a les sals simples en solució, el +1, que ha estat assenyalat per Manchot el 1926, i el +4, que es dóna segurament en l’òxid CoO 2 i en alguns complexos N’hi ha dues varietats allotròpiques la varietat α, que cristallitza en el sistema hexagonal compacte c/a = 1,6, estable a les temperatures ordinàries i que es transforma lentament per sobre de 450…
reactiu de Tollen
Química
Solució aquosa amoniacal de nitrat d’argent (AgNO3), emprada per a la identifació d’aldehids, basada en la capacitat reductora d’aquests composts sobre l’ió argent (I), el qual fet es posa de manifest per l’aparició d’un precipitat negre constituït pel metall en el seu estat lliure: .
Si la reacció és duta a terme en un tub d’assaig la superfície del qual sigui ben neta, hom pot aconseguir que el metall es dipositi en forma de partícules molt fines sobre la superfície del vidre, la qual cosa origina el que hom coneix com a mirall d’argent