Resultats de la cerca
Es mostren 7 resultats
antracè
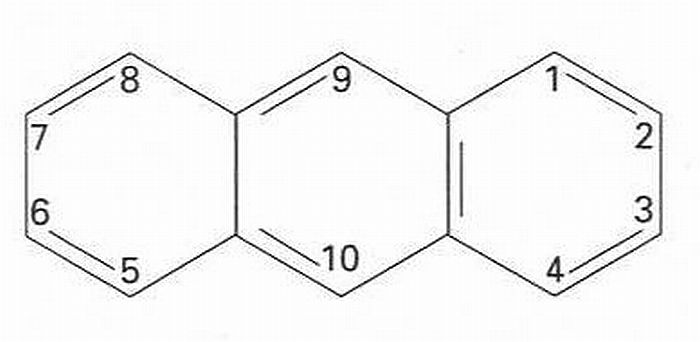
Antracè
©
Química
Hidrocarbur aromàtic tricíclic, que es fon a 218°C i bull a 342°C, insoluble en aigua, soluble en els solvents orgànics, la molècula dels quals forma tres anells benzènics coplanars.
És obtingut en la destillació del quitrà d’hulla i hom l’extreu a partir de la fracció anomenada oli d’antracè Quan és pur presenta una fluorescència blava característica És oxidat fàcilment a antraquinona i serveix com a primera matèria en la fabricació d’alitzarina i de molts altres colorants
reacció de Haber-Weiss
Química
Reacció consistent en el següent cicle de dues reaccions: H2O2 + OH· → H2O + O2- + H+ i H2O2 + O2- → O2 + OH- + OH·.
La segona reacció ha aconseguit notorietat com a possible font de radicals hidroxil Tanmateix, té un constant de reacció negligible Es creu que complexos de l’ió ferro III poden catalitzar aquesta reacció de la següent manera primer, el FeIII es reduït per l’anió superòxid, i després, el FeII és oxidat pel peròxid d’hidrogen reacció de Fenton
bari
Química
Metall alcalinoterri pertanyent al grup II A de la taula periòdica, de color blanc argentí quan és pur, mitjanament dur i mal·leable, molt electropositiu, que actua amb valència 2.
El bari és una mescla natural d’isòtops de masses atòmiques 130, 132, 134, 135, 136, 137, 138, en la qual el 138 Ba es troba en un 71,66% Forma el 0,04% de la crosta terrestre i ocupa el divuitè lloc en ordre d’abundància hom el troba sobretot en forma de sulfat baritina i de carbonat witherita El 1774, Karl Wilhelm Scheele diferencià la barita de la calç , i el 1790, Crawford diferencià, alhora, l' estronciana monòxid d’estronci de la barita La gran afinitat que té el bari per l’hidrogen, els halògens, l’oxigen, el nitrogen i el sofre, per a formar hidrurs, halurs, òxids, nitrurs i…
monòxid de nitrogen
Química
Gas incolor, d’un punt d’ebullició de -151,8°C i un punt de fusió de -163°C, poc soluble en aigua.
En contacte amb l’aire és oxidat ràpidament a NO 2 , de color bru Reacciona amb clor i brom i dona halurs de nitrosil, NOX És preparat en el laboratori per reacció del coure amb àcid nítric diluït, i en la indústria per oxidació catalítica de l’amoníac com a pas intermedi en la fabricació de l’àcid nítric, i també segons l’equació A la dècada del 1980 s’iniciaren una sèrie d’experiments que revelaren que el monòxid de nitrogen, un gas que havia estat considerat només com un contaminant atmosfèric, era generat pel metabolisme cellular i tenia una àmplia gamma de funcions…
catàlisi
Química
Procés de canvi de velocitat de les reaccions químiques per l’acció d’una substància que es manté químicament inalterada ( catalitzador
).
El terme catàlisi ‘descompondre químicament’ fou introduït per Berzelius el 1835, però la idea és molt antiga Un procés de catàlisi pot canviar la velocitat d’una reacció o provocar reaccions que no s’iniciarien, però no pot modificar el rendiment de la reacció és a dir, pel procés de catàlisi és alterada la velocitat amb què una reacció tendeix cap a l’equilibri químic normal, però no és afectat el valor de la constant d’equilibri Si el catalitzador actua augmentant la velocitat de reacció, hom parla de catàlisi positiva i, si actua disminuint-la, hom en diu catàlisi negativa Quan la…
bismut
Química
Element metàl·lic pertanyent al grup 5B de la taula periòdica, de color blanc brillant (quan és pur) tirant a rosat, de molt poca conductivitat tèrmica (la més baixa de tots els metalls, llevat del mercuri).
Propietats i utilització del bismut És el metall més diamagnètic, el que presenta un major efecte de Hall, el de coeficient de dilatació tèrmica més negatiu i el que presenta més augment de volum en solidificar-se Fins a la segona meitat del segle XV era confós amb l’estany, i no fou aïllat fins el 1737 per Hillot, bé que Johann Heinrich Pott 1692-1777 i Torbern Olof Bergman 1735- 84 en són considerats els descobridors científics El bismut natural és constituït exclusivament pel núclid 208, però hom ha aconseguit de preparar-ne molts d’altres núclids radioactius Constitueix el 3x10 -6% de l’…
oxicloració
Química
Variant de la cloració per substitució en la qual el subproducte de la reacció, clorur d’hidrogen, és oxidat catalíticament a clor mitjançant oxigen, d’on resulta un aprofitament total de l’agent clorant.
El procés té una gran importància econòmica augmenta notablement la rendibilitat de les cloracions per substitució i és aplicat en un gran nombre de processos industrials