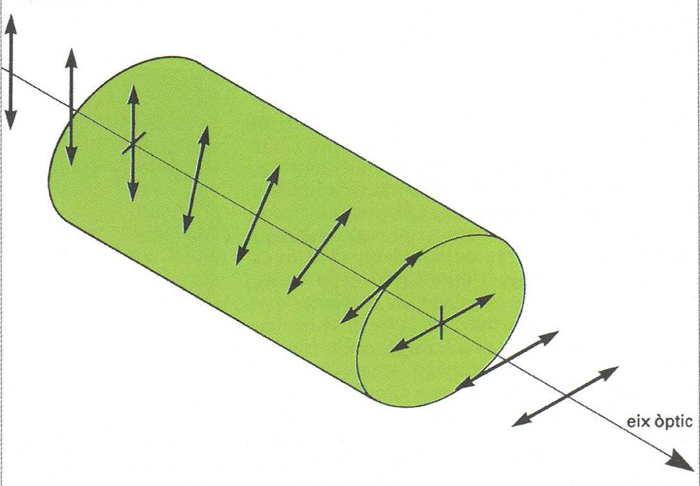
L’angle de rotació depèn de la temperatura, de la llargada d’ona de la llum, del gruix travessat i de la natura de la substància activa. El fenomen de l’activitat òptica fou descobert per Francesc Aragó, el 1811, estudiant el cristall de quars. Ben aviat es posà de manifest que l’activitat òptica podia ésser de dues menes. Concretament, per als sòlids pot ésser deguda a una dissimetria del reticle cristal·lí (aquest és, precisament, el cas del quars), és a dir, pot ésser només una propietat del cristall, que desapareix per fusió o dissolució. Biot descobrí, no obstant això, el 1815, que existeixen substàncies en les quals l’activitat òptica persisteix sigui quin sigui l’estat físic. Posteriorment Faraday descobrí, el 1845, que totes les substàncies conegudes, en qualsevol estat físic, manifesten activitat òptica (en un grau variable segons la substància) quan estan sota la influència d’un camp magnètic (efecte Faraday). Prescindint, però, d’aquest fenomen, en el qual s’imposa una dissimetria des de l’exterior, Pasteur reprengué l’estudi de l’activitat òptica descoberta per Biot i en deduí (1860) que, per les substàncies que la manifesten, la causa no podia ésser altra que una dissimetria de la pròpia molècula. L’experiència demostrà que les substàncies que presenten activitat òptica molecular (és a dir, activitat que no depèn ni de l’estructura cristal·lina ni d’un camp magnètic exterior) existeixen en dues formes, de propietats físiques exactament idèntiques a tots els altres punts de vista, però que difereixen pel signe de llur activitat òptica (sentit de la rotació del pla de vibració de la llum).
Hom diu que aquestes substàncies presenten el fenomen de la isomeria òptica. L’estudi de l’activitat òptica, en posar de manifest aquesta isomeria i tot el que sobre l’estructura molecular pot deduir-se’n, ha estat una eina poderosa que ha contribuït eficaçment a l’avançament de la química. L’activitat òptica molecular és mesurada, a l’estat líquid o en solució, amb els aparells anomenats polarímetres. Per als líquids purs (a una temperatura t i per a una certa longitud d’ona de la llum, λ) és anomenada rotació òptica específica o poder rotatori específic [α] t λ; el quocient: [α] t λ =α/ lo on α és l’angle de rotació (en graus sexagesimals i fraccions decimals de grau), l la llargada de líquid (en dm) que han travessat els raigs lluminosos i o la densitat del líquid. Hom usa la notació [α] t D per a indicar que λ és la longitud d’ona de la línia D del sodi. Si es tracta d’una solució de concentració c en una substància activa (expressada en g per ml de solució), el poder rotatori específic és: [α] t λ = α/ lc. El poder rotatori específic d’una solució és, en primera aproximació i en termes generals, independent de la concentració (llei de Biot), si bé depèn del solvent. [α] t λ es considera positiu quan el pla de polarització de la llum gira en el mateix sentit que les busques d’un rellotge, negatiu en el cas contrari. Segons que tinguin poder rotatori positiu o negatiu, les substàncies són anomenades dextrogires, o levogires. El producte de [α] t λ pel pes molecular M de la substància activa s’anomena rotació òptica molecular o poder rotatori molecular [M] t λ = [α] t λ M. Per a evitar operar amb xifres massa grosses, alguns autors prefereixen definir [M] t λ per la fórmula [M] t λ = [α] t λ M /100. L’existència de l’activitat òptica pot ésser explicada qualitativament de manera satisfactòria partint de la hipòtesi de la dissimetria molecular proposada per Pasteur. Una teoria quantitativa que permeti de calcular a priori el poder rotatori molecular de qualsevol substància d’estructura coneguda, presenta, però, moltes dificultats i, malgrat alguns avenços en aquest sentit, el problema es troba encara molt lluny d’ésser resolt.