Què és la química industrial
Adobs per a les plantes, cola, targetes de plàstic, vernís, detergent, medecines, dissolvents... A primer cop d’ull pot semblar que es tracta d’alguns productes per a la llar que es poden trobar en la llista de la compra. A més, aquests productes, tan diferents els uns dels altres, tenen poc a veure entre ells pel que fa al sistema amb què han estat elaborats. Però observant la llista amb deteniment, podem comprovar que, de fet, tenen en comú un punt important, tots aquests productes són fruit de l’aplicació pràctica dels estudis de la química, en particular de la química industrial. Podríem dir també que el principi fonamental que comparteixen tots aquests productes comercials és la transformació de l’estructura química i física dels compostos inicials en productes que poden ser comercialitzats. Segons aquest principi, la indústria química agrupa activitats industrials de natura ben diferent, tant per la quantitat i el tipus de materials considerats com pel que fa a la manera de produir-los, és a dir, per la maquinària i les tècniques d’elaboració. Així, la indústria química que tracta les primeres matèries, generalment en grans quantitats i en instal·lacions grandioses, s’anomena química primària, mentre que les empreses encarregades de les transformacions dels productes bàsics integren la química secundària.
Substàncies orgàniques i inorgàniques
Convé recordar que la indústria química pot transformar materials orgànics i inorgànics, la distinció dels quals és possible gràcies a la classificació realitzada per la mateixa disciplina. La química orgànica va néixer al segle XVIII, quan el científic Torbern Bergman va establir diferents propietats entre les substàncies segons si pertanyien al món mineral, animal o vegetal. En el món animal i el vegetal s’inclouen les matèries que tenen una estructura molecular formada bàsicament per àtoms de carboni units a una desena d’altres elements, principalment hidrogen, oxigen, nitrogen, sofre i clor, formant una varietat de combinacions molt extensa, que sovint constitueixen fórmules força complexes. En canvi, pel que fa al primer grup, el de les substàncies d’origen mineral, hi pertanyen els compostos amb una fórmula més senzilla, que numèricament són més limitats i es formen a partir de la combinació dels elements de la taula periòdica.
Al començament del segle XX, dos esdeveniments importants van donar un nou impuls a la química industrial. D’una banda, la possibilitat de produir industrialment grans quantitats de substàncies orgàniques, que fins aleshores només es podien extreure de productes naturals; i, de l’altra, la capacitat de sintetitzar substàncies artificials, no presents en la natura. Aquests compostos artificials, per la seva importància i difusió en la vida quotidiana, representen el punt de suport estratègic del mercat de la indústria química en la nostra era; n’hi ha prou amb pensar en els fàrmacs, les fibres sintètiques o els plàstics. Aquestes substàncies han aportat benestar, però alhora han provocat que el sistema industrial del segle XX sigui vulnerable i delicat, ja que depèn considerablement de les primeres matèries, molt especialment del petroli, la font principal dels recursos actuals.
Primeres matèries, productes i residus
La indústria química basa els seus coneixements en l’experiència pràctica i la recerca. A l’inici, en la fase experimental, les instal·lacions es construïen i es milloraven d’acord amb la pràctica adquirida durant les proves. Recentment, s’ha passat a la fase en què els projectes parteixen d’estudis físics i químics teòrics sobre les reaccions. Però abans d’endinsar-nos en la descripció de les bases principals que caracteritzen els processos d’elaboració dels productes químics, convé precisar el significat d’alguns dels termes que apareixen més sovint, com són les primeres matèries, el productes intermediaris, els productes secundaris i els residus.
Les primeres matèries es troben a la natura. Són les substàncies i els compostos que la indústria utilitza com a matèries bàsiques per als seus diversos processos. S’usen en estat pur o bé purificades mitjançant diversos procediments. A partir dels diferents usos, les primeres matèries es poden classificar en matèries d’ús general i matèries d’ús específic. Les que pertanyen al primer grup es consideren fonamentals tant pel fet que s’utilitzen en grans quantitats com perquè s’usen en processos molt diversos, dels quals deriven productes molt variats. Pertanyen a aquest grup, entre d’altres, l’aigua, el sofre, el clorur de sodi, el nitrat de sodi, el fosfat tricàlcic, el carbó, el petroli i el metà. Per la seva banda, les primeres matèries d’ús específic són presents igualment en la natura, però s’empren en la producció en sectors industrials limitats. Pertanyen a aquest grup, entre d’altres, els silicats, les calcàries i les argiles, que formen part de la indústria dels materials de la construcció; els minerals metal·lífers, dels quals s’obtenen els metalls corresponents; les fosforites, que són la base de la indústria del fòsfor; els minerals boratats, necessaris per a la producció dels derivats del bor; els productes amilacis i la cel·lulosa, amb què es produeix l’alcohol; els fruits oliosos, usats en la indústria dels greixos i dels olis; i les remolatxes, d’on s’extreu el sucre. També hem d’incloure en aquesta llista les substàncies que intervenen, encara que sigui en quantitats modestes, en processos de fabricació especials, com és el cas del silici, el cadmi, el platí, l’iridi, el pal·ladi i el seleni.
Els productes intermediaris són les substàncies que s’obtenen durant les diferents fases d’un procés i que són transformades per a l’obtenció del producte final. Poden considerar-se un dels estadis intermedis d’un procés, i encara que poden tenir una gran importància industrial no solen comercialitzar-se directament.
Els productes finals són els últims elements del cicle de producció. Es destinen a la venda i, per tant, tenen un gran interès econòmic. Es presenten de maneres diferents segons a qui vagin destinats. Si el destinatari és el públic en general, els productes es presenten acabats, és a dir, a punt perquè puguin ser adquirits en els llocs de venda corresponents. Com a exemple de productes acabats podem esmentar els medicaments venuts a la farmàcia, els vernissos de les cases de pintures, la benzina de les estacions de servei, els detergents, l’alcohol desnaturalitzat, els esprais o els adobs que es troben en els comerços i els supermercats. En canvi, si el destinatari és una segona indústria, que al seu torn s’encarregarà de la preparació definitiva per a la venda al públic, aleshores són considerats productes semielaborats. Vegem-ne alguns exemples: els metalls en lingots, en barres o en peces que es venen a les indústries metal·lúrgiques, les substàncies termoenduribles en pols per a l’estampació destinades a les indústries de components, els colorants per a les indústries tèxtils, els additius anticorrosius per a les indústries de lubrificants, l’alcohol etílic per a la preparació de begudes alcohòliques i molts d’altres. Les indústries químiques es limiten gairebé sempre a fabricar substàncies pures o semielaborades que altres indústries refinen, transformen, mesclen o, senzillament, preparen per a la distribució comercial.
En els cicles de producció, pot donar-se el cas que les principals reaccions a què se sotmet una substància, o altres reaccions que s’hi produeixin de manera imprevista, generin productes secundaris i subproductes. Aquestes substàncies no es poden considerar residus, ja que posseeixen un cert valor comercial i es poden destinar a altres processos, de manera que la mateixa indústria els recupera o bé els ven a unes altres indústries perquè els aprofitin.
Els residus constitueixen, pel seu pes i volum, una càrrega considerable de materials sobrants de les indústries. Provenen de les diverses etapes de la producció i estan formats pel material de rebuig, les deixalles, les substàncies que ja no són reactives o que no es poden depurar més, en estat sòlid o líquid. En no tenir ja cap utilitat per als processos industrials, els residus s’han de separar, tractar o eliminar d’alguna manera. Els problemes generats pels residus industrials han estat a l’ordre del dia de la crònica periodística d’aquests últims anys, atès que sovint els sistemes de depuració no resulten eficaços o bé no s’apliquen amb les precaucions necessàries, i tot plegat provoca la contaminació ambiental i el malbaratament dels recursos energètics. En aquest sentit, el món de la indústria i els científics compromesos en les solucions dels problemes ambientals fan esforços tant per a aplicar les mesures d’eliminació de residus més adequades com per a convertir els residus, sempre que sigui possible, en “primeres matèries secundàries”, és a dir, en matèries que s’aprofitin equiparablement a les primeres matèries. Malgrat tot, la indústria produeix una gran quantitat de residus no aprofitables, que s’han de tractar i d’emmagatzemar o enterrar en llocs segurs.
Química primària i secundària
La indústria química es pot dividir en dos sectors d’activitat principals: la química primària i la química secundària. Les indústries que pertanyen a la química primària, anomenada també química de base, tracten de manera gairebé exclusiva les primeres matèries naturals en grans quantitats, i sovint fan servir instal·lacions de dimensions considerables. Aquestes indústries transformen les primeres matèries en un nombre limitat de productes bàsics, que són el punt de partida de la preparació i elaboració d’altres productes, els quals són fabricats per unes altres indústries.
El sector de la química secundària comprèn les empreses encarregades de transformar els productes bàsics fabricats per la química primària. Hi ha empreses d’aquest sector, que es defineixen com a empreses de química fina, que al seu torn poden preparar els productes intermediaris per a altres processos. N’hi ha d’altres, en canvi, que es dediquen a la preparació de productes de característiques específiques molt concretes, i per aquest motiu es diu que formen part de la química d’especialitat.
Un aspecte important de divergència entre la química primària i la secundària és el que s’anomena l’economia de gran escala. La química primària, per motius relacionats amb la tecnologia, ha de tractar grans quantitats de materials, en instal·lacions de cicle continu que funcionen a altes pressions i a altes temperatures, amb un consum d’energia i d’aigua considerable. A més, la química primària depèn en gran part del proveïment i dels costos de les primeres matèries. Els marges dels beneficis són ajustats i això implica que les instal·lacions han de rendibilitzar al màxim els diversos processos. És per això que es procura recuperar les matèries secundàries amb el reciclatge dels subproductes, i d’aquesta manera s’estalvia energia. Es crea, així, una xarxa de dependències tecnològiques i de relacions productives en el que s’anomenen “polígons químics”, és a dir, concentracions en una zona determinada d’empreses dedicades a un mateix tipus de producció. Es tracta sovint d’empreses que pertanyen a una mateixa societat o a societats diverses però estretament interrelacionades. En són un exemple les petroquímiques.
En canvi, pel que fa al sector de la química secundària, hi pertanyen fàbriques de dimensions mitjanes o petites, de situació indeterminada, els productes de les quals són molt distints entre ells. És característic d’aquest sector un gran dinamisme i una forta competència. Això explica que les empreses que hi pertanyen renovin constantment els processos tecnològics.
Instal·lacions i procediments
Hem comentat anteriorment que la indústria química es caracteritza per una gran heterogeneïtat de tècniques i de productes. Això comporta, evidentment, una diferenciació clara de les instal·lacions i dels cicles de producció. Sense necessitat d’endinsar-nos-en en una descripció sistemàtica, intentarem posar en relleu alguns elements comuns o molt presents en les diverses tècniques químiques.
L’element central del procés és molt sovint el reactor, a l’interior del qual les primeres matèries se sotmeten a determinades temperatures, pressions i moviments que desencadenen les reaccions de síntesi. El tipus més comú de reactor té l’aspecte d’una cisterna, fabricada amb metall resistent i, en la majoria dels casos, tancada hermèticament. El reactor està proveït de mecanismes i instruments que en regulen el funcionament, com són ara sistemes d’escalfament i de refredament, paletes per a remoure el material, condensadors de vapor, circuits de càrrega i descàrrega, etc.
Però la unitat central també pot estar constituïda per una màquina que transformi i mescli no pas les primeres matèries sinó els productes semielaborats. És el cas de la tina per a tenyir les fibres, l’extrusor a partir del qual s’obté la fina pel·lícula de polietilè o el recipient per a l’adobament de les pells. D’aquests tipus d’aparells s’obtenen els productes desitjats, però barrejats amb una certa quantitat de residus.
Tornem al reactor de síntesi, o sigui, a la gran cisterna. Sigui quina sigui la reacció, és fàcil d’imaginar que del reactor surten els productes acompanyats d’un cert nombre de primeres matèries no transformades i de possibles subproductes. S’imposa, doncs, un procés de purificació de les substàncies útils i de recuperació de les no transformades. Suposem, doncs, que s’ha de separar una fase sòlida d’una de líquida. Per a fer-ho, podem fer servir decantadors, filtres, centrifugadores o cristal·litzadors. En canvi, si el que hem de fer és separar dues fases líquides, aleshores recorrerem a aparells de destil·lació, condensació o rectificació, o bé a reactors d’extracció amb dissolvents.
En un procés de producció, l’element determinant és el rendiment. Per això, és habitual que es regulin les funcions de la instal·lació, des de la temperatura de reacció fins a la durada del procés, per tal d’obtenir-ne el màxim profit. El rendiment d’un procés químic es pot calcular al final de la producció confrontant la quantitat obtinguda de producte acabat amb la quantitat introduïda de matèria bàsica, o bé durant el transcurs de la reacció mesurant-ne la variació amb el temps.
La major part de les reaccions químiques són reaccions d’equilibri. Això vol dir que en una reacció no s’assolirà mai la transformació completa de les substàncies originàries en substàncies de destinació. De fet, significa que s’assolirà el màxim rendiment en una situació d’equilibri. Aquesta idea és vàlida igualment per als processos industrials químics, atès que en els processos de síntesi no s’aconsegueixen gairebé mai conversions totals, sinó com a molt les corresponents a l’equilibri.
De manera anàloga, existeixen uns límits precisos també en les operacions de mera transformació, segons els quals no es poden modificar els productes semielaborats més enllà d’un cert límit. En tots aquests casos, per tal de no malbaratar energia i recursos, es procedeix tant al reciclatge de les substàncies no afectades per la reacció com a la recuperació dels materials que encara són aprofitables, després de la selecció corresponent i d’un eventual nou condicionament.
Un aspecte dels processos de producció propis de la indústria química que hem de considerar amb deteniment és l’alt grau de perillositat que comporten. És ben sabut que es poden produir mescles explosives, reaccions incontrolables, forts augments de calor, descomposicions de compostos inestables tractats sense precaucions o fuites de substàncies altament contaminants. Per aquest motiu, s’han de realitzar tots els controls preventius i les revisions de les instal·lacions necessàries per a evitar tant possibles accidents a l’interior de les unitats de producció com també la contaminació del medi ambient.
Les primeres matèries i la indústria química
La indústria química agrupa un nombre tan variat i nombrós de productes que resulta molt difícil fer-ne una catalogació exhaustiva. Així doncs, ens limitarem a presentar una síntesi dels principals processos de tractament de les primeres matèries i també alguns elements aptes per a il·lustrar la seva complexitat, mentre que tractarem dels productes més variats en els capítols següents.
L’oxigen, l’ozó i l’aigua oxigenada
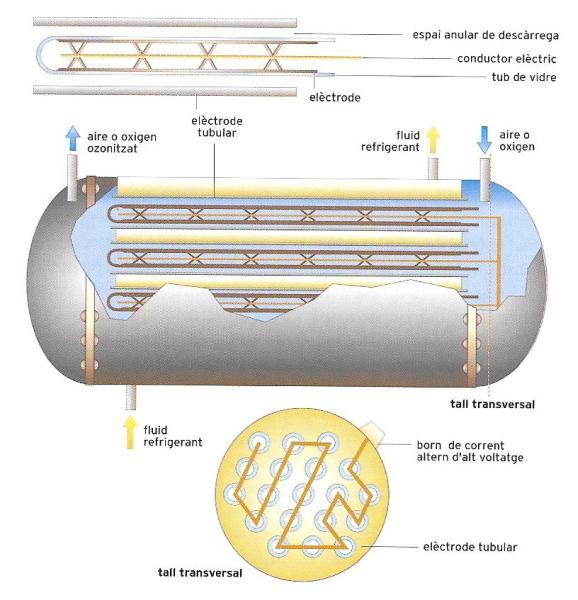
Esquema d’un ozonitzador, emprat per a esterilitzar aigua i aliments o regenerar l’aire. L’oxigen o l’aire hi és sotmés a descàrregues d’alt voltatge. L’aparell ha d’estar refrigerat, perquè la calor descompon l’ozó.
ECSA
Estem acostumats a imaginar-nos les primeres matèries en estat sòlid o líquid, com és el cas per exemple del carbó, el petroli o l’aigua. Però gairebé mai no pensem en els gasos. Prenguem l’exemple de l’oxigen. Tots sabem que l’oxigen és indispensable per a la respiració i, per tant, per a la vida. Però potser no tenim prou present que l’oxigen s’utilitza sovint, com a primera matèria, en la indústria química, la siderúrgia i la producció d’explosius o de propulsors. De fet, l’oxigen representa un dels productes bàsics de la química industrial i, per això, cal produir-ne.
L’oxigen no és un element escàs en la natura, sinó que és present tant en l’aire, acompanyat d’altres gasos, com en l’aigua, íntimament unit amb l’hidrogen. Així doncs, és a partir de l’aigua o de l’aire que podem obtenir l’oxigen.
Partim de l’aire. Es tracta d’una barreja de gasos diversos en què no es poden distingir les molècules d’oxigen de les de nitrogen, el component principal de l’atmosfera, perquè hi són presents en el seu estat gasós habitual. Això no obstant, l’aire està subjecte a les lleis que regeixen els gasos i, per tant, es pot liquar. D’aquesta manera, es podrà efectuar la separació de l’oxigen respecte dels altres components. Per a liquar l’aire, és necessari sotmetre’l a una pressió de 37,2 atmosferes i a una temperatura de –140,7°C. Per tal d’assolir aquestes condicions, es fan servir dos procediments, que reben el nom dels seus descobridors; són el mètode de Linde i el mètode de Claude.
El mètode de Linde, de l’enginyer i inventor alemany Carl Ritter von Linde, funciona amb compressors, refrigeradors, bescanviadors de calor i vàlvules d’expansió, que permeten sotmetre l’aire, purificat de partícules de pols i d’humitat, a cicles de compressió i d’expansió successives. Atès que els gasos, en expandir-se, es refreden, aquest cicle facilita que l’aire es vagi refredant progressivament i passi finalment a l’estat líquid. El segon procediment, conegut com a mètode de Claude, en honor del físic i enginyer francès Georges Claude, crea l’expansió per mitjà de màquines que funcionen amb turbines o amb èmbols, de manera que s’obté un descens de la temperatura amb una pressió menor. Aleshores, l’aire líquid entra en la fase més important, la de la destil·lació fraccionada, en què se separen, com és propi de tota destil·lació de substàncies líquides, els diversos components de l’aire, i entre ells, l’oxigen.
La liqüefacció de l’aire no és l’únic procediment que permet la producció d’oxigen. És possible d’obtenir-ne, i per consegüent també es pot aconseguir hidrogen, per mitjà de la tècnica industrial de l’electròlisi de l’aigua, exactament com es fa en els experiments de laboratori. S’utilitzen cel·les electrolítiques formades per bateries de cel·les disposades en sèrie que contenen càtodes d’acer dolç i ànodes de ferro niquelat. Aquest sistema és aconsellable per a la producció de petites quantitats d’oxigen d’un alt grau de puresa.
Altres productes relacionats amb l’oxigen són l’ozó i l’aigua oxigenada. L’ozó, la molècula del qual està formada per tres àtoms d’oxigen (O3), és a les capes altes de l’atmosfera i acompleix la funció primordial de protegir-nos dels raigs ultraviolats del Sol. En virtut de les seves qualitats de bon oxidant, es fa servir per a depurar l’aigua i per a regenerar l’aire. Com que no es pot extreure de les altes capes de l’atmosfera, és necessari produir-lo industrialment, a partir de l’oxigen que conté l’aire. L’operació s’efectua en uns tubs de vidre especials, refredats amb aigua, en els quals l’aire se sotmet a descàrregues elèctriques d’alta tensió.
L’aigua oxigenada (H2O2), que és emprada entre altres usos per a desinfectar les ferides, s’obté mitjançant l’electròlisi del sulfat d’amoni (NH4)2SO4 amb àcid sulfúric. Aquest procediment és menys perillós que l’electròlisi de l’àcid sulfúric, ja que elimina els inconvenients relacionats amb la generació simultània d’oxigen i hidrogen. Actualment també és obtinguda per la hidrogenació catalítica de la 2-etilantraquinona. L’aigua oxigenada, que és un oxidant poderós, s’utilitza sempre en solució aquosa, a concentracions que varien entre 3 i 90%.
El nitrogen, l’amoníac i l’àcid nítric
El nitrogen constitueix, de molt, el component més important de l’aire atmosfèric, ja que hi és present en un 78%. Els processos de liqüefacció de l’aire i de la successiva destil·lació fraccionada, ja descrits, permeten l’obtenció no solament de l’oxigen sinó també de grans quantitats de nitrogen, que representa un dels puntals de la indústria química, ja que fa possible la síntesi de derivats molt importants, entre els quals ocupa un lloc destacat l’amoníac, encara que també cal esmentar la urea, les sals d’amoni i l’àcid nítric.
Pel que fa a l’amoníac, es tracta d’una substància d’una olor forta i desagradable, prou coneguda, ja que en l’àmbit domèstic se’n sol emprar una solució diluïda per a netejar el terra o les rajoles de València. Però ara no ens entretindrem a descriure’n els usos casolans, ja que l’amoníac, la molècula del qual conté un àtom de nitrogen i tres d’hidrogen (NH3), constitueix, de fet, la base per a la síntesi de nombrosos productes de gran interès industrial, entre els quals destaquen els adobs i els derivats orgànics. L’amoníac s’obté a partir de la reacció de l’hidrogen amb el nitrogen, basada en l’afinitat entre tots dos elements. La reacció requereix un catalitzador i unes condicions determinades de temperatura i pressió.
La urea (CH4N2O) és un altre derivat important del nitrogen. S’empra per a la síntesi dels adobs químics i de resines termoenduribles, anomenades així perquè s’endureixen amb la calor. S’obté a partir de la reacció del diòxid de carboni i l’amoníac a l’interior d’un reactor, en el qual és necessari que s’assoleixi una pressió de vora 200 atmosferes i entre 190-195°C de temperatura, en presència d’un excés d’amoníac equivalent al 100%.
L’amoníac, que és bàsic, i l’àcid clorhídric (HCl), que és un àcid molt fort, es neutralitzen formant la solució de sal d’amoni més comuna: el clorur d’amoni (NH4Cl). L’aigua, en evaporar-se, deixa al fons els cristalls blancs d’aquesta sal. De les reaccions químiques que utilitza la indústria, no n’hi ha gaires que puguin reproduir-se tan fàcilment com aquesta, encara que és ben cert que cal prendre certes precaucions, però no requereix cap maquinària especial i es pot fer fins i tot a casa o al laboratori d’una escola. Les sals d’amoni s’utilitzen en els laboratoris i en la producció d’altres productes químics i fertilitzants. Les més emprades, a més del clorur d’amoni, són el fosfat amònic, el carbonat amònic, el nitrat amònic i el sulfat amònic.
L’àcid nítric (HNO3) és un àcid fort, oxidant, del qual s’obtenen altres substàncies com són ara nitrats de sodi, calci, potassi i amoni, emprats en l’agricultura. Existeixen diversos mètodes per a la síntesi de l’àcid nítric. Actualment predomina el mètode Ostwald, establert pel químic alemany Wilhelm Ostwald, en el qual l’oxidació de l’amoníac es provoca mesclant-lo amb un excés d’aire. L’aire s’insufla en cremadors a través de malles tènues de platí, a una temperatura d’uns 780°C i a pressions de 8 atmosferes. Els vapors d’òxid de nitrogen que es formen es refreden en bescanviadors de calor fins a 20°C i es dissolen en aigua de condensació. Posteriorment, passen a unes torres d’absorció àcida on són rentats amb aigua i oxidats amb aire. Un derivat de l’àcid nítric és el nitrat de plata, una substància usada pels fotògrafs en el revelatge de les pel·lícules fotogràfiques.
El sodi, la sal i el carbonat
Els productes principals de la indústria del sodi són el clorur sòdic, el carbonat de sodi i l’hidròxid de sodi o sosa càustica. El clorur de sodi (NaCl) és una primera matèria que generalment s’extreu de les aigües salades, en concret de les salines, indrets amb aigües molt poc profundes en què la forta evaporació fa augmentar considerablement la concentració del clorur de sodi i de les altres sals presents. Per a separar el clorur de sodi de les altres sals, n’hi ha prou amb controlar la densitat de la solució aquosa a mesura que es va produint la cristal·lització. El clorur de sodi obtingut d’aquesta manera no és encara del tot pur, ja que conté ions de magnesi, potassi, brom, iode i sulfat, que poden ser separats i recuperats successivament per a altres usos. El clorur de sodi no solament s’extreu del mar, sinó que també existeixen mines d’extracció de clorur de sodi mineral, anomenat aleshores sal gemma, com és el cas actual de Cardona (Bages), un cop acabades les explotacions de sals potàssiques. L’àmbit més corrent d’ús del clorur de sodi és l’alimentari (sal de cuina). Del clorur de sodi també s’obtenen altres derivats del sodi.
El carbonat de sodi (Na2CO3) és el producte resultant de la reacció del clorur de sodi en una solució aquosa amb diòxid de carboni. És el “patriarca” d’una vasta família de compostos del sodi, com són el borat, el nitrat i el nitrit, el sulfit, el bisulfit i el silicat. Per a obtenir-lo, es fa servir el procés Solvay —inventat pel químic i industrial belga Ernest Solvay—, que, a més del clorur de sodi, només requereix el diòxid de carboni i l’amoníac; amb tot, cal assenyalar que és un procés complex, l’instrumental i les reaccions químiques del qual necessiten un control rigorós.
La importància de l’hidròxid de sodi està estretament lligada al seu fort caràcter bàsic, que acompleix una funció cabdal en les reaccions químiques tant dels laboratoris com dels processos industrials. S’obté a partir del carbonat de sodi o del clorur sòdic tractats amb mètodes industrials. En el primer cas, s’utilitza el mètode de la caustificació, consistent a fer reaccionar en solució aquosa el carbonat de sodi amb l’hidròxid de calci a uns 100°C. El segon cas, el més freqüent, explota el procés electrolític del clorur de sodi en aigua. Al final de tots dos processos, és necessari concentrar les solucions d’hidròxid de sodi. Això es fa per mitjà d’instruments d’evaporació d’efecte múltiple, és a dir, acumulant el treball de diverses torres d’evaporació disposades en cascada, o bé, al buit, en aparells individuals. La depuració de l’hidròxid de sodi comercial es produeix per dissolució en alcohol etílic, el qual dissol l’hidròxid però no les impureses, que per consegüent poden ser eliminades. Finalment, es procedeix a l’evaporació de l’alcohol.
L’hidròxid de sodi o sosa càustica (NaOH) s’utilitza de vegades a casa, per exemple quan l’aigüera s’embussa, però cal tenir ben present que es tracta d’una substància perillosa i que, per al seu ús, cal extremar les precaucions de manipulació a causa de la seva acció altament càustica.
El clor, el lleixiu i l’àcid clorhídric
De vegades, a casa, per a fer més blancs els teixits, es fan servir productes com el lleixiu, d’una olor irritant i desagradable. Aquesta olor és produïda pel clor que desprèn l’hipoclorit de sodi present en el lleixiu.
Ara bé, el clor no solament serveix per a treure les taques de la roba blanca. A causa del seu fort caràcter oxidant, es tracta d’un dels productes bàsics de la indústria química, del qual s’obtenen derivats de gran importància. Podem recordar, entre els compostos orgànics, els cloroderivats, usats com a anestèsics, antiparasitaris i productes intermediaris per a altres síntesis. I, entre els compostos inorgànics, el clorat de potassi, conegut en el camp de la indústria dels tints, els explosius i els llumins; i el clorat de sodi, emprat com a herbicida. També s’utilitza en gran part com a desinfectant per a les aigües.
El clor no es troba a la natura en estat lliure, sinó majoritàriament en forma de clorurs en l’aigua de mar. S’obté principalment amb mètodes industrials mitjançant l’electròlisi de solucions de clorur sòdic. Després, es refrigera, es deshumidifica, es liqua, s’emmagatzema i es transporta en camions cisterna o en bombones d’acer.
L’àcid clorhídric és un producte industrial molt interessant que és possible d’obtenir mitjançant dos processos. Un primer procés aprofita la reacció directa entre l’àcid sulfúric concentrat i el clorur de sodi, a una temperatura de 150°C. La reacció es produeix en uns forns especials dels quals surt l’àcid clorhídric gasós, amb el sulfat i el bisulfat de sodi com a subproductes. El segon procés és més corrent i dóna un producte més pur. Aprofita l’alt grau d’afinitat entre l’hidrogen i el clor. En cambres de combustió, refrigerades amb aigua, els dos gasos es cremen amb una flama que assoleix temperatures d’uns 2 600°C. Seguidament, el vapor d’àcid clorhídric que s’obté d’aquest procés es refreda, tal com succeeix en el primer tipus de procés, i posteriorment es dissol en aigua, la qual cosa genera quantitats considerables de calor. A casa, és possible que, al costat del lleixiu, hi hagi altres productes domèstics, com ara una ampolla de salfumant. Cal anar molt en compte amb aquest producte, perquè aquesta denominació comercial designa, de fet, l’àcid clorhídric que en solució aquosa es ven a les adrogueries i als supermercats.
El sofre, la pirita i l’àcid sulfúric
Associat al diable, en les seves aparicions sinistres i fantàstiques, sembla que el sofre no gaudeix de gaire bona fama. Però és sens dubte una reputació injusta, tot i que s’ha de reconèixer que la pudor de les emanacions de gasos sulfurosos en terrenys volcànics (solfatares) és poc reconfortant. Tanmateix, és d’aquests jaciments, petits i sovint a la superfície del terreny, que s’extreu el sofre natural, format per oxidació del sulfur d’hidrogen. En altres casos, es troba en jaciments extensos i profunds, en mines de sofre. En tot cas, el sofre és una primera matèria molt important. Per a extreure’l de la ganga, és a dir, del conjunt dels minerals presents en el jaciment, és necessari produir una fusió a 350°C en forns especials, i seguidament refinar-lo per mitjà de processos de destil·lació.
El producte principal d’aquesta indústria és el diòxid de sofre (SO2), que es pot obtenir en quantitats rellevants a partir no solament del sofre sinó també de la pirita i d’altres sulfurs minerals. Ara veurem de quina manera.
La paraula pirita deriva del grec pyrites, que significa ‘de natura de foc’. El foc sembla, doncs, l’acompanyant inseparable del sofre o de les menes que el contenen. La pirita n’és una de les més importants, ja que conté bàsicament sulfur de ferro. Si se sotmet a una combustió forçada amb aire a uns 600°C, s’obté diòxid de sofre i òxid fèrric. La combustió té lloc en forns de grans dimensions o bé, actualment, en reactors de llit fluïditzat.
Però la pirita no és l’únic mineral en què apareix el sofre, ja que la blenda conté sulfur de zinc; el cinabri, sulfur de mercuri; la galena, sulfur de plom; la calcosina, sulfur de coure; i la calcopirita, sulfur de coure i ferro. De tots aquests sulfurs minerals s’obtenen, procedint de la mateixa manera que en el cas de la pirita, diòxid de sofre i els metalls corresponents. Del diòxid de sofre, per reacció amb els òxids alcalins, s’originen molts derivats, entre els quals cal esmentar el sulfit de sodi i el metabisulfit de potassi, usats en la indústria alimentària i també en fotografia.
Tornem ara a la combustió del sofre, de la pirita i dels altres sulfurs. Ja sabem que d’aquest procés s’obté diòxid de sofre. Tanmateix, si la combustió es produeix amb un excés d’aire considerable, el diòxid de sofre s’oxida i, en presència de catalitzadors, dóna triòxid de sofre com a producte intermediari, que es fa reaccionar amb aigua per a obtenir l’àcid sulfúric: 2SO2 + O2 + 2H2O 2H2SO4.
Hi ha dos sistemes per a obtenir àcid sulfúric. Un d’ells —anomenat mètode de les cambres de plom—, ja en desús, es desenvolupava en un aparell complex en forma de torre, revestida de plom, un metall que no es corroeix amb l’àcid, en la qual entraven en reacció, a una temperatura d’uns 100°C, els components d’una mescla gasosa determinada. En el segon tipus de procés, avui preponderant, anomenat mètode de contacte, l’oxidació s’assoleix amb l’ús de catalitzadors de platí i pentòxid de vanadi a uns 500°C de temperatura.
L’àcid sulfúric, un compost importantíssim com a producte bàsic industrial, és conegut per la seva naturalesa altament àcida i oxidant. Les seves reaccions originen derivats molt útils. Permet obtenir altres àcids en reaccionar amb les seves sals com, per exemple, àcid clorhídric a partir del clorur sòdic. Es fa servir també com a sulfat en preparats fertilitzants i com a agent sulfonant, deshidratant i decapant.
El fòsfor, els llumins i els adobs
Ens podem preguntar com és possible que els llumins normals de cuina s’encenguin fregant-los amb qualsevol superfície o amb la sola de la sabata, a l’estil fatxenda dels “durs” del Far West, mentre que resulta impossible de fer la més petita espurna amb els llumins de seguretat, si no és fregant-los amb la banda fosca de la capseta. Tota la culpa la té el fòsfor. Tot seguit, n’aclarirem l’enigma.
El fòsfor està relacionat químicament amb el clor, l’hidrogen, l’oxigen i el sofre, i es troba en la naturalesa, en forma de fosfat tricàlcic, en els minerals anomenats fosforites. Les fosforites es couen, a 1 300°C, en forns elèctrics que contenen sorra de quars i carbó. D’aquesta manera, el fosfat es redueix a fòsfor fos, que es filtra o es destil·la en un flux de vapor d’aigua i diòxid de carboni. Així és com s’obté el fòsfor groc. Escalfat a 260°C, procediment realitzat al buit per evitar que s’inflami, el fòsfor groc es transforma en fòsfor vermell.
El fòsfor és present en molts productes comercials. Per exemple en la fabricació de llumins es fa servir el fòsfor vermell o trisulfur de fòsfor (P4S3), ja que tots dos compostos, s’inflamen per fregament. El trisulfur és el més conegut dels sulfurs de fòsfor, i s’obté escalfant a 100°C el fòsfor groc o vermell mesclat amb sofre.
Ara, mirem de resoldre l’enigma presentat inicialment. En els llumins comuns, el fòsfor o el trisulfur s’empasten amb clorat i cromat de potassi, sofre, goma, òxids de ferro i zinc, argila i cola. Tota aquesta barreja es posa a l’extrem d’un palet que s’encendrà fins i tot amb el frec de la sola de la sabata. En canvi, en el cas dels llumins de seguretat, el trisulfur de fòsfor només es posa a les bandes de la capseta, mentre que a la punta del llumí s’enganxa la pasta, que s’encendrà únicament si el fregament s’efectua en una de les bandes de la capseta.
Però el fòsfor i els seus compostos no s’empren només en la fabricació de llumins. Un altre derivat important del fòsfor és l’àcid fosfòric (H3PO4), que s’obté de la reacció de la fosforita amb l’àcid sulfúric al 70-75%. D’aquesta reacció, a més de l’àcid fosfòric, s’obtenen, com a subproductes separables per mitjà de la filtració, el sulfat de calci i el fosfat monocàlcic. La mescla d’aquests dos subproductes es comercialitza com a fertilitzant amb el nom de superfosfat. En canvi, a l’àcid fosfòric, se li extreu l’aigua per evaporació i assoleix una concentració màxima del 75%. L’àcid fosfòric pot entrar en reacció amb els hidròxids dels metalls i generar una vasta sèrie de fosfats, com el fosfat dicàlcic, monosòdic, disòdic, monopotàssic, dipotàssic, amònic i diamònic, usats en l’alimentació i com a fertilitzants.
Un dels sectors més importants de la indústria química és el que es dedica a la producció d’adobs sintètics o fertilitzants químics, que han fet la competència als adobs naturals tradicionals i els han substituït en una gran part, si més no als països d’agricultura intensiva. La possibilitat de disposar d’aquestes substàncies en grans quantitats és un dels factors que han permès el fort creixement productiu que caracteritza l’agricultura dels nostres dies.
Els adobs poden ser nitrogenats, fosfatats i potàssics. Aquestes tres categories s’estableixen segons l’element constitutiu bàsic, que és respectivament el nitrogen, el fòsfor i el potassi. Sovint es comercialitzen en forma d’adobs mixtos, és a dir, en una mescla binària, si contenen només dos dels elements esmentats, o ternària, si tots tres hi són presents (vegeu “L’agricultura”).
Entre els derivats del fòsfor hem citat el fosfat d’amoni. Aquesta sal conté en la mateixa molècula tant el fòsfor com el nitrogen. Els adobs d’aquest tipus pertanyen a la categoria dels fertilitzants complexos. També són freqüents els adobs compostos, en els quals apareixen barrejats els derivats respectius del nitrogen, el fòsfor i el potassi. Analitzem ara una mica quins són els compostos que caracteritzen les tres categories de fertilitzants.
El nitrogen pot adoptar diverses formes químiques, com el nitrogen nítric, el nitrogen amoniacal i el nitrogen orgànic (vegeu “El sistema viu”). Sobre la base de la forma química del nitrogen, els adobs nitrogenats es divideixen en tres categories. A la primera categoria pertanyen els nitrats, principalment els de sodi, calci i amoni, que tenen una absorció vegetal ràpida, ja que són solubles i no queden fixats al terreny. D’altra banda, hi ha els fertilitzants que contenen nitrogen amoniacal i que queden fixats per les substàncies col·loïdals del sòl i, per tant, són absorbits lentament pels vegetals. Finalment, pertanyen a la tercera categoria els que contenen nitrogen orgànic i que són assimilats en un temps encara més prolongat.
Pel que fa als adobs fosfatats, els més emprats són els fosfats de calci i els superfosfats. Entre els adobs potàssics, cal esmentar el clorur, el sulfat i el carbonat de potassi.
El carbó, un producte natural
Quanta gent, especialment entre els joves, ha tingut a les mans, encara que només hagi estat una vegada, un tros de carbó? Segurament ben poca. El carbó, com a màxim, evoca imatges cinematogràfiques de minaires suats i de rostres ennegrits, mines llòbregues i maquinistes de locomotores antigues i atrotinades. En definitiva, el carbó sembla que ja no pertanyi al nostre temps. Però no és ben bé així. El carbó encara es fa servir moltíssim avui dia, com ho demostra la producció anual d’uns 3 500 milions de tones d’antracita i hulla, i més de 1 200 milions de tones de lignit. Veurem tot seguit els processos i els usos que tenen el carbó com a protagonista.
Segons el seu origen, hi ha quatre tipus de carbó: la torba, el lignit, l’hulla i l’antracita (vegeu “Les fonts d’energia”). L’hulla i l’antracita, els carbons fòssils pròpiament dits, són els més interessants per a la indústria perquè són els d’origen més antic i, per tant, els més rics en carboni.
La destil·lació del carbó té lloc en uns recipients especials, anomenats retortes, en què el material s’exposa a temperatures en augment i fora del contacte amb l’aire. D’aquesta manera, s’alliberen progressivament tots els components volàtils. El residu es compon essencialment de carboni i rep el nom de carbó de coc. En el decurs de l’operació, es graduen amb molta cura l’augment i la durada de les temperatures. Es parteix de la temperatura ambient i aproximadament en una hora s’assoleixen 300°C. Posteriorment, en l’espai d’unes quatre hores, s’arriba a 500°C i, finalment, en dues hores més, la temperatura augmenta fins a 1 100-1 200°C. Aquesta seqüència permet transformar el carbó en substàncies volàtils (gas) i carbó de coc i estalvia l’obtenció de productes degradats poc aprofitables.
Segons les característiques de la instal·lació dels aparells, es facilita la producció de l’un o de l’altre. En el primer cas, parlem de la fabricació del gas (anomenat gas de l’enllumenat, domèstic o ciutat), en què el coc és un subproducte. En el segon, parlem de la fabricació del coc, usat en la metal·lúrgia, en què el subproducte és el gas, anomenat gas de fàbrica de coc.
Vegem més detingudament per a què serveixen el gas, el coc i els seus subproductes. Fins fa pocs anys, abans de ser substituït gairebé arreu pel metà o gas natural, el gas de l’enllumenat o gas ciutat arribava a les cases, on es feia servir de combustible domèstic a tota la xarxa urbana. El gas obtingut de la fabricació del coc, en canvi, s’utilitza per a escalfar els destil·ladors, per a l’extracció de l’hidrogen i per a la síntesi de l’amoníac.
Els dos tipus de coc, el metal·lúrgic i el subproducte del gas d’enllumenat, s’usen com a combustibles en aplicacions específiques. De la destil·lació del carbó també s’obtenen altres subproductes com, principalment, aigües amoniacals, destinades a la producció de sulfat d’amoni; fertilitzants agrícoles, i el quitrà de carbó fòssil, que per mitjà de la destil·lació fraccionada i d’un tractament químic genera hidrocarburs aromàtics i productes orgànics.
La indústria del gas natural
El metà és un gas conegut per tothom. En moltes ciutats, alimenta les flames dels forns i dels cremadors de les instal·lacions de calefacció domèstica. En la indústria, també es fa servir com a combustible, carburant i primera matèria per a síntesis orgàniques importants.
El metà és el component predominant del gas natural, que es troba comprimit en jaciments subterranis a pressions màximes de 150 atmosferes. Però el gas natural no conté només metà. Segons d’on provingui, s’hi troben en proporcions diverses età, propà, butà, pentà, altres hidrocarburs, sulfur d’hidrogen, gasos nobles, diòxid de carboni i nitrogen. Descomprimit a 30 atmosferes, el gas natural passa a través d’uns rentadors i d’uns rectificadors on se separen els diferents components.
L’interès que suscita el gas natural es deu a la recuperació del metà i dels altres hidrocarburs, emprats com a font d’energia i de primeres matèries. El propà i el butà, per exemple, són molt aptes per a les síntesis químiques bàsiques o, si es comprimeixen, es poden utilitzar com a combustibles o propulsors.
La primera aplicació del gas per a l’enllumenat als Països Catalans va ser realitzada a Barcelona el 29 de juny de 1826 pel químic Josep Roura i Estrada, que en va fer una demostració posteriorment a Madrid, el 1832. El 1843 es va iniciar a Barcelona l’enllumenat dels carrers, un any més tard a València i després a la resta de les ciutats importants de l’estat. Fins fa poc, era el gas ciutat el que arribava a les cases a través de les canonades. A Catalunya, el gas natural va ser introduït a la dècada dels seixanta. Es transportava en vaixells des dels països productors fins al port de Barcelona, des d’on es distribuïa —i encara es distribueix— a través dels gasoductes. Però el 1996 es va enllestir el gasoducte que des d’Algèria empalma amb la xarxa espanyola tot travessant el nord d’Àfrica i l’estret de Gibraltar. L’any 1975, a Tarragona, es va instal·lar la primera refineria de gas de Catalunya, la qual ha desenvolupat un complex petroquímic considerat un dels més importants d’Europa.
El petroli i els seus derivats
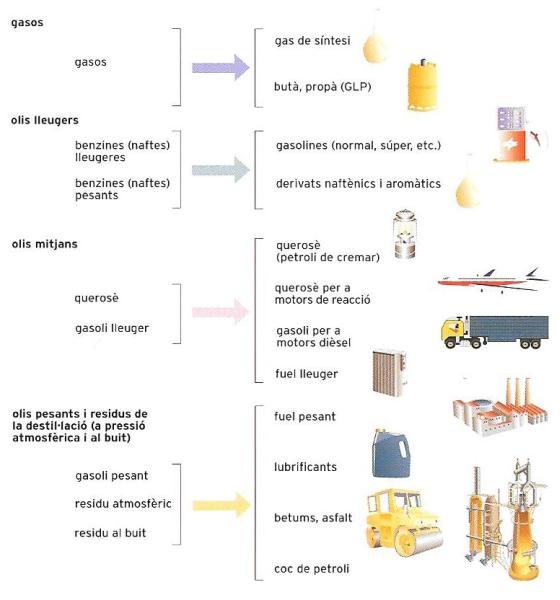
Els principals derivats del petroli són els gasos i els olis lleugers, mitjans i pesants. S’obtenen per destil·lació fraccionada, un procés que permet separar en primer lloc els gasos liqüefactes i la benzina lleugera, i després les benzines pesants, els querosens i el gasoli. Dels residus, tractats en una columna de buit, s’obtenen olis pesants. Després, aquests derivats són transformats en combustibles, lubrificants i asfalts.
ECSA
Benzina i gasoli. N’hi ha prou amb aquestes dues paraules per a posar de manifest la importància determinant que tenen el petroli i els seus derivats en múltiples aspectes de la nostra vida quotidiana. De fet, el petroli és la primera matèria predominant en la indústria química, fins al punt que dóna nom a un dels sectors principals d’aquesta indústria, la petroquímica. A Catalunya, aquest sector industrial s’ha concentrat bàsicament a Tarragona.
El petroli és compost de mescles d’hidrocarburs (vegeu “La gran família del carboni”, i “Les fonts d’energia”). Segons el tipus i la quantitat d’hidrocarburs que hi són presents, es distingeix entre els petrolis de base parafínica, amb més del 65% d’alcans; els petrolis de base naftènica, amb més del 65% de cicloalcans i naftens; els petrolis de base aromàtica, amb més del 15% d’hidrocarburs aromàtics; i els petrolis mixtos.
El petroli, als jaciments de sota terra, no és en estat pur, sinó barrejat amb escòries i petites quantitats d’altres substàncies, com poden ser sals o sulfurs. És per això que, tan bon punt s’ha extret, se sotmet a un tractament consistent a decantar els residus, generalment sorra i fang, i una part de l’aigua. Posteriorment, se n’eliminen les sals, fent ús de solucions àcides o bàsiques, segons el tipus de sal. Aquesta operació s’efectua a una temperatura de 100-150°C i comporta l’evaporació dels gasos no condensables.
En aquest estadi, el petroli cru emprèn el seu viatge cap a les refineries. El transport es fa a través d’oleoductes, o bé per mitjà de vaixells cisterna o grans petroliers. Pel que fa al refinatge, es tracta, primer de tot, d’aïllar les fraccions afins dels hidrocarburs. L’operació més important que es realitza amb aquesta finalitat és la destil·lació fraccionada, que divideix el petroli en hidrocarburs gasosos, fraccions lleugeres i fraccions intermèdies.
Dels hidrocarburs gasosos s’extreu el butà i el propà, que es comercialitzen com a gasos liquats del petroli o GLP. També poden ser transformats per la indústria petroquímica per tal d’extreure’n alquens, útils per a la producció de matèries plàstiques, gomes sintètiques i altres productes orgànics. De les fraccions lleugeres s’obtenen dissolvents com l’hexà i el ciclohexà, llevataques, dissolvents per a vernissos i benzines per a automòbils i aeronaus. De les fraccions intermèdies s’extreu el querosè, usat com a carburant per als motors agrícoles i dels avions i també per a la calefacció domèstica, i el gasoli, que es fa servir de combustible per a la calefacció dels habitatges i com a carburant per als motors dièsel—, ja que té la important propietat d’autoinflamar-se en presència de l’aire quan és comprimit en el cilindre del motor.
La destil·lació finalitza aquí. Però encara es poden obtenir productes importants dels residus, efectuant la destil·lació al buit. D’aquesta manera s’obtenen olis pesants, com els olis minerals lubrificants, els olis per a automòbils i maquinària, les naftes, els olis de vaselina i l’asfalt de petroli.
Els productes derivats de la destil·lació del petroli són molt nombrosos, i si observem els productes i els estris de la vida quotidiana, en trobarem força exemples. Això no obstant, quan es parla de petroli, sempre es fa referència als carburants. I amb raó, atesa la seva importància. Els carburants obtinguts del gas natural i de la fracció lleugera i intermèdia del petroli no són suficients, però, per a cobrir les necessitats del consum. Per aquest motiu se n’incrementa la producció fent servir altres fraccions de la destil·lació, però a condició que es modifiqui l’estructura molecular dels compostos que contenen. Per exemple, amb l’ús de catalitzadors, és possible trencar les molècules dels olis pesants fins a obtenir cadenes moleculars més curtes, és a dir, les fraccions lleugeres, que tenen molta demanda. Aquest procés rep el nom de craqueig catalític. La indústria dels carburants s’ocupa principalment d’aquestes tècniques de modificació de l’estructura molecular, que adopten processos com el craqueig, el reforming, l’alquilació, la polimerització (unió de monòmers en molècules complexes) i la isomerització (reordenació interna dels àtoms d’una molècula).
Aquests processos també formen part de la producció industrial petroquímica, associats a altres mecanismes de reacció que tenen com a funció, entre d’altres, l’obtenció d’hidrocarburs aromàtics a partir de les fraccions que arriben del tractament del petroli. Per corregir-ho s’utilitzen les fraccions d’oli pesant que es reciclen amb el craqueig catalític, o bé les benzines “de cua” del reforming catalític.
Altres productes de la indústria química
Del vidre de les finestres als fulls de diari o dels pneumàtics dels automòbils als detergents, contínuament estem en contacte amb objectes i productes industrials de tota mena. Bona part d’aquests objectes provenen de la indústria química, que els ha fabricat transformant i tractant primeres matèries molt diverses. En aquest capítol, volem oferir una panoràmica general dels tractaments més freqüents i interessants d’aquests productes industrials.
Les resines sintètiques
El terme plàstic es fa servir normalment per a indicar una classe especial de resina sintètica. Es tracta de materials sovint flexibles a temperatura ambient, que s’estoven quan s’escalfen o si són a prop d’una font de calor, mentre que amb el fred s’endureixen, de manera semblant al vidre. Aquests materials es designen amb el nom de resines termoplàstiques. No obstant això, d’altra banda, existeixen resines sintètiques que presenten un comportament oposat, per la qual cosa reben el nom de termoenduribles. Aquestes altres resines es comporten com l’argila, és a dir, són plàstiques i dúctils a una temperatura normal, però en escalfar-se s’endureixen irreversiblement.
La importància de les resines sintètiques en la societat actual és ben coneguda per tothom. Estem envoltats d’objectes i de productes que se’n deriven, com les matèries plàstiques, les fibres, les gomes i els vernissos. Però les resines sintètiques, com ja ho indica el nom, no es troben a la naturalesa. Per a obtenir-les, és necessari partir de molècules individuals que, unides entre elles en grans quantitats, originin grans molècules. Aquestes macromolècules tenen un pes i una llargada que són múltiples de molècules simples idèntiques. Les substàncies que proveeixen les molècules individuals es diuen monòmers; en canvi, les resines obtingudes de la reacció de síntesi i formades per macromolècules són polímers (vegeu “La gran família del carboni”). La primera matèria necessària per a la producció de les resines sintètiques és el petroli, i el 4% del consum actual de petroli es destina a aquest sector. En alguns casos, certes matèries plàstiques es poden obtenir a partir de reaccions químiques en polímers naturals, com per exemple la cel·lulosa.
La indústria actual pot produir moltes classes de resines sintètiques. Només cal pensar en les diferències entre diversos materials plàstics d’ús corrent, per exemple, la bossa de la compra, la galleda de fregar o el quadre de comandaments del cotxe. D’això podem deduir que, per a la producció de les nombroses i diverses resines sintètiques, són necessaris diferents derivats del petroli. Per tant, s’hauran de posar en marxa diverses reaccions de síntesi a fi de produir també diversos tipus de macromolècules.
Les resines es poden obtenir per polimerització i per poliaddició. En les resines per polimerització, que són totes les termoplàstiques, els monòmers originaris no estan saturats, o sigui que presenten enllaços dobles. Sotmesos a reacció, els enllaços dobles s’obren i les molècules individuals s’uneixen entre elles formant llargues cadenes d’hidrocarburs. Diverses espècies de resines s’obtenen per polimerització. Aquest és el cas de les resines poliolefíniques, a les quals pertanyen el polietilè, obtingut de l’etilè mitjançant un procés a altes pressions, a temperatures de 200-300°C i fent servir catalitzadors com l’oxigen i els peròxids, i que s’empra per exemple en la producció de bosses de la compra; el polipropilè, amb què es fan els cubells per a la bugada, i el politetrafluoroetilè o tefló. També s’obtenen per polimerització les resines poliviníliques, entre les quals hi ha el poliestirè (el material d’embalatge més comú), el policlorur de vinil, l’acetat de polivinil i d’altres; les resines poliacríliques, de les quals destaquen els poliacrilats, el polimetacrilat de metil, el poliacrilonitril, que és important per a la producció de fibres tèxtils, i les gomes sintètiques.
En les resines obtingudes per policondensació, que poden ser termoplàstiques o termoenduribles, les macromolècules provenen de la condensació de molècules individuals que tenen dos grups funcionals. El grup funcional d’una molècula es lliga a un grup diferent d’una altra molècula i, a partir d’aquesta reacció, sorgeixen substàncies secundàries, com ara aigua, àcid clorhídric i amoníac, que s’eliminen. Formen part d’aquesta categoria, les resines fenòliques o fenoplasts (la primera resina fenòlica obtinguda, que era també el primer plàstic sintètic, va ser la baquelita, producte de la condensació del fenol amb el formaldehid en presència de catalitzadors), les melamíniques, les poliestèriques saturades i no saturades (entre les quals hi ha la vitroresina, que es reforça amb llana de vidre) i les poliamídiques.
En el cas de les resines obtingudes per poliaddició, les molècules originàries han de tenir dos grups funcionals, exactament com passa amb les resines policondensades; però, per contra, s’uneixen sense eliminar altres molècules. Pertanyen a aquest grup les resines epoxídiques i els poliuretans.
Les matèries plàstiques
La història de les matèries plàstiques és molt recent. El seu inici data del segle XIX, època en què es van realitzar els primers treballs amb el cel·luloide, el producte termoplàstic més antic conegut; posteriorment, a la primera dècada del segle XX, Leo Baekeland aconseguí realitzar la síntesi d’un producte termoendurible (la baquelita), obtingut per la polimerització de fenol i formaldehid. Els anys vint s’establiren les primeres bases científiques per a la comprensió de l’estructura dels polímers, i els anys trenta i quaranta s’eixamplaren els coneixements i es descobriren o es produïren, per primer cop a escala industrial, noves matèries plàstiques, com per exemple el policlorur de vinil, el poliestirè i el polietilè de baixa densitat. Però fou sobretot entre els anys quaranta i setanta que tingué lloc un gran desenvolupament científic en aquest àmbit, amb la descoberta i l’aplicació industrial de nombrosos polímers utilitzables com a matèries plàstiques, per exemple els polièsters i les poliamides, els poliuretans, les resines acríliques i els epòxids, entre d’altres. Actualment, es comercialitzen centenars de matèries plàstiques, derivades de diverses desenes de polímers amb la base convenientment modificada segons l’ús a què es destinin.
La relativa facilitat d’emmotllament de les matèries plàstiques és, sens dubte, un dels aspectes que més han contribuït a la ràpida difusió d’aquests materials. El tractament es pot efectuar de diverses maneres, si bé totes elles tenen en comú l’escalfament del material a una temperatura adequada per a garantir-ne la fluïdesa necessària, el fet de sotmetre el material estovat (disposat en un motlle idoni) a una pressió determinada per a donar-li la forma desitjada, el refredament i l’extracció del motlle. Molt sovint, però, especialment en el cas dels termoenduribles, el producte bàsic requereix ser tractat amb additius abans de l’operació d’emmotllament pròpiament dita.
Un cop afegits els additius, per mitjà d’una senzilla mescla mecànica o en calent, té lloc la transformació de la matèria plàstica en productes semielaborats o en productes manufacturats acabats per mitjà de diverses tècniques, com són ara l’extrusió, l’estampació, el calandratge i el termoemmotllament.
L’extrusió és una tècnica molt emprada en la producció dels termoplàstics, i en alguns casos també dels termoenduribles. Consisteix a fer passar a pressió el material, en estat pastós, a través d’una obertura amb la forma desitjada.
L’estampació pot ser d’injecció o de compressió. L’estampació d’injecció és una de les tècniques més usuals en la transformació tant dels termoplàstics com dels termoenduribles. S’hi fan servir les anomenades premses d’injecció. El material sòlid s’aboca en un cilindre escalfat i, un cop s’ha assolit la fluïdesa necessària, s’injecta per mitjà d’un cargol que fa la funció d’èmbol a la cavitat d’un motlle, on es refreda i se solidifica en la forma desitjada. Finalment, la peça s’extreu del motlle. Tot el cicle, que generalment es produeix de manera automàtica, té una durada que pot variar de pocs segons a alguns minuts, segons el material utilitzat i la forma i les dimensions de la peça. Per la seva banda, l’estampació de compressió es fa servir especialment per als termoenduribles. El material per a l’estampació es col·loca generalment en un semimotlle degudament escalfat i es modela mitjançant l’altre semimotlle, també escalfat. Seguidament, es produeix el refredament i l’obertura del motlle.
El calandratge s’empra per a l’obtenció de diversos tipus de làmines de resines termoplàstiques i consisteix en la compressió del material fluid, que es fa passar per corrons metàl·lics escalfats (generalment quatre, disposats de dos en dos), els quals roden en sentit contrari els uns respecte dels altres. En el termoemmotllament, usat per als termoplàstics, s’escalfa el producte semielaborat en forma de làmina amb raigs infraroigs fins que assoleix un grau d’estovament suficient i, posteriorment, es col·loca en un motlle a pressió al buit.
Les fibres químiques
Avui, els teixits i les fibres que es troben als comerços són en bona part d’origen químic, per bé que les fibres d’origen natural (animal i vegetal) conserven una certa difusió. Les fibres químiques es divideixen en dos grans grups: les d’origen artificial, obtingudes amb el tractament de polímers naturals (principalment cel·lulosa, i també altres substàncies vegetals, proteïnes, etc.), i les d’origen sintètic, produïdes a partir de matèries polimèriques, obtingudes amb les tècniques descrites més amunt (vegeu també “Els vestits”).
Les gomes sintètiques
El cautxú o goma natural, que s’extreu del làtex d’algunes plantes equatorials, i en concret de l’Hevea brasiliensis, va ser durant dècades la primera matèria per excel·lència de la indústria de la goma. En un moment donat, aquesta substància va ser analitzada químicament, es va descobrir que estava constituïda pel polímer de l’isoprè i es van poder produir materials anàlegs per síntesi química. Aquestes resines es designen amb el nom d’elastòmers.
La importància d’un elastòmer es posa de manifest en l’enumeració de les seves propietats mecàniques (resisteix a la tracció i el desgast, i absorbeix els xocs), dinàmiques (s’allarga amb la tracció, es deforma desprenent poca calor i de seguida recupera elàsticament la forma inicial) i químiques (resisteix a l’envelliment, a les reaccions químiques i a la calor, és impermeable a l’aire i als líquids i és insoluble en els dissolvents aquosos i orgànics).
No hi ha dubte que aquestes propietats tenen a veure amb l’estructura química del polímer. De fet, les cadenes d’un polímer d’aquestes característiques han de ser flexibles i estar desarticulades i desordenades, si bé han de ser capaces de disposar-se paral·lelament quan té lloc una tracció.
L’operació que confereix al cautxú més resistència a les forces mecàniques, en manté les propietats inalterables entre 0 i 100°C i en millora la resistència tant als agents atmosfèrics i químics com als lubrificants i als dissolvents, s’anomena vulcanització. El sofre és el principal agent vulcanitzant. Fixant-se als enllaços dobles de l’elastòmer, el sofre forma una mena de pont entre les cadenes, que d’aquesta manera es connecten entre elles. En l’elastòmer, el sofre s’incorpora als accelerants, com ara sulfurs i disulfurs aromàtics, que n’afavoreixen la reacció. També s’hi introdueixen altres additius, per exemple els antioxidants, com els fenols aromàtics, que preserven el cautxú de l’envelliment provocat per l’oxigen, l’ozó, la llum i la calor. S’hi barregen igualment substàncies inertes, com el fum d’estampa (pólvores carbonoses) o la sílice, per tal d’augmentar la resistència al tall o a l’abrasió, o per endurir l’elastòmer o fer-lo més pesat i consistent.
D’altra banda, també s’hi afegeixen substàncies plastificants, com són els olis minerals o els polièsters, perquè sigui més fàcil de tractar. L’addició de colorants, com els òxids de ferro vermells o les sals de cadmi grogues, serveix per a donar a l’elastòmer el color desitjat.
La goma té diferents tractaments. Així, el làtex artificial es barreja amb altres substàncies en mescladors cilíndrics horitzontals o en rotors. Seguidament, la mescla es fa passar entre corrons pesants, anomenats calandres, dels quals surt en forma de làmines. També es pot comprimir en extrusors, uns cilindres amb un forat a la base, per on es fa sortir la mescla en forma de varetes que són enviades al procés d’estampació. Amb l’extrusió també es pot obtenir l’estiratge, és a dir, l’emmotllament directe en objectes amb un patró determinat.
La vulcanització i l’emmotllament de les peces s’efectuen alhora. En un motlle especial s’escampen els antiadhesius i els lubrificants. Tot seguit, per omplir el motlle amb la mescla, s’adopta algun dels múltiples sistemes d’emmotllament, ja sigui a pressió, per transferència, per injecció, per expansió o al buit. Un cop acabada la vulcanització, la peça es desemmotlla i es procedeix als acabats, que consisteixen en rectificacions, tractaments de superfície i diferents controls de qualitat.
Entre les gomes sintètiques més conegudes podem citar el poliisoprè, el polibutadiè i el neoprè, els quals deriven d’hidrocarburs que, com el butadiè, contenen dos enllaços dobles i, per això, s’anomenen diolefines. Altres tipus de gomes sintètiques, no diolefíniques, són el poliisobutilè i el copolímer etilepropilè.
El vidre
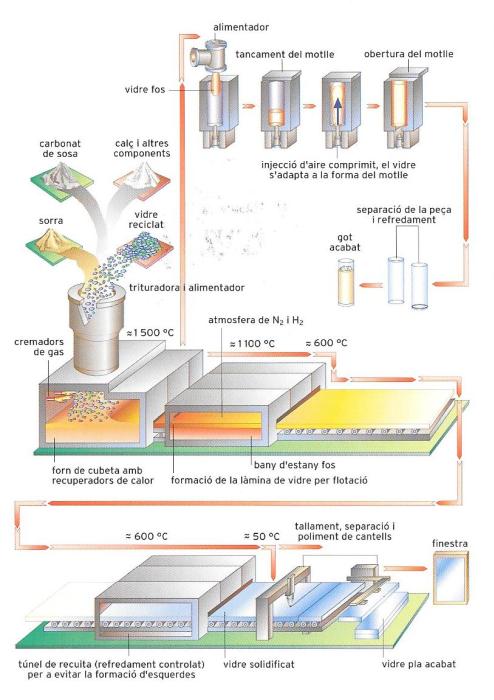
Esquema del procés de fabricació industrial del vidre en un forn continu. Aquest forn és alimentat constantment amb les primeres matèries, inclòs el vidre reciclat. S’obté vidre fos a punt per a ser modelat per emmotllament o estampació, com és el cas de la fabricació d’envasos (vegeu la part superior del dibuix) o per laminatge, com en l’obtenció de vidre pla (part inferior).
ECSA
Si algú ens digués que el vidre és un material líquid, potser no ens el creuríem. Però, en realitat, una afirmació tan paradoxal com aquesta ens permetria recordar que el vidre està emparentat amb les substàncies líquides d’una manera més directa del que ens podríem imaginar. Les molècules de les substàncies sòlides generalment es troben ordenades en una estructura cristal·lina. Les del vidre, en canvi, estan disposades en un reticle desordenat i conserven l’estructura amorfa típica de l’estat líquid. I l’única raó que impedeix que les molècules del vidre llisquin les unes sobre les altres, com s’esdevé en els líquids, és l’elevada viscositat de la massa.
La sílice és la substància que presenta l’estat vítric per excel·lència i, per tant, és la primera matèria més important per a la fabricació del vidre. Però també existeixen altres substàncies que posseeixen aquesta propietat, com per exemple el diòxid de bor, el diòxid de fòsfor, l’òxid d’alumini o l’òxid d’antimoni. Així doncs, el vidre es presenta com una estructura complexa, en què la sílice es combina amb altres additius, com són l’alúmina, els modificadors i les primeres matèries accessòries, en proporcions fixades pels criteris de producció.
La sílice és present en la natura en forma de sorra o de quars. Per a la fabricació dels cristalls, ha d’estar molt purificada i gairebé exempta d’òxid ferrós, que pot arribar al 0,5% en els vidres de les finestres i al 2% en els vidres d’ampolla. L’alúmina ja és present, en quantitats reduïdes, en les sorres silícies. Si no és així, se n’hi afegeix.
Els modificadors són indispensables per a la preparació del vidre. Els òxids de sodi i potassi, afegits en forma de carbonats, constitueixen una categoria especial de modificadors, anomenats fundents, que moderen la temperatura de fusió i faciliten la vitrificació. Els modificadors, en sentit estricte, són molt nombrosos i acompleixen funcions diverses. El diòxid de bor contribueix a augmentar l’índex de refracció i la duresa del vidre, mentre que en disminueix la dilatació. El diòxid de fòsfor permet l’obtenció de vidres òptics especials. L’òxid de calci millora la resistència del vidre a l’agressió de l’aigua i dels agents químics. L’òxid de zinc, usat per a vidres especials, augmenta l’índex de refracció i la resistència química. Per a la fabricació de vidres especials i de cristalls es fa servir l’òxid de plom i de bari, en una quantitat màxima del 70%, amb l’objectiu d’incrementar-ne el pes específic, la transparència i la brillantor.
Les primeres matèries accessòries s’afegeixen en petites proporcions per a corregir o eliminar els defectes, o bé per a caracteritzar el vidre d’alguna manera. Posem l’exemple de l’òxid de ferro (FeO) responsable de la coloració verda del vidre. Podria donar-se el cas que ja estigués present en la sílice i que se’l volgués eliminar. Si apareix en petites quantitats, es pot fer que el ferro es torni innocu afegint-hi diòxid de manganès. D’aquesta manera, es formen òxid de manganès rosa i òxid fèrric groc. Però el groc i el rosa, en ser colors complementaris, es neutralitzen recíprocament, de manera que el vidre es torna incolor. Una altra primera matèria accessòria és el diòxid d’arseni, que garanteix una massa fosa més homogènia i fluida, de manera que les bombolles d’aire s’eliminen més fàcilment. El vidre que s’obté amb aquest procediment pot ser més líquid, transparent i pur, tal com es requereix en la branca de l’òptica.
Tenint en compte tot el que hem dit, resulta evident la possibilitat de produir diversos tipus de vidre. De fet, hem parlat de l’òxid de ferro, responsable del color verd del vidre, o dels vidres especials, resistents als agents químics, com el vidre Jena. I, d’altra banda, tothom coneix els vidres de colors, els opacs o els irrompibles.
Els vidres de colors s’obtenen afegint a la massa fosa òxids de ferro, cobalt, níquel, crom o coure. Pel que fa al color lletós dels vidres opacs, s’obté mitjançant l’addició d’òxid d’estany, fluorur de sodi, fluorur d’alumini i sodi (criolita), i fosfats en forma de cendres d’ossos. Actualment, ocupen un lloc destacat els vidres de seguretat, els quals se sotmeten a un tractament per a millorar-ne la resistència als xocs i per a fer que es trenquin en fragments o en pols en lloc de trossets de vidre estellat. Aquest és el cas del vidre armat, anomenat així perquè, durant el laminatge, s’introdueix en calent una malla metàl·lica entre dues planxes de vidre. En canvi, el vidre irrompible es fabrica en fred, encolant a pressió un full de cel·luloide entre dues planxes de vidre.
Acabarem aquest breu catàleg dels diversos tipus de vidre parlant de la llana de vidre, que s’obté sotmetent els fils de vidre provinents de l’estiratge a uns potents raigs de vapor a alta pressió, o bé a un estirament violent amb l’ajuda d’uns discos metàl·lics que giren a gran velocitat. Així s’aconsegueix una massa suau i lleugera semblant a la llana, que es pot filar i teixir i que s’usa per a reforçar les matèries plàstiques o per a teixits incombustibles, com a filtre o com a material útil per a l’aïllament acústic i tèrmic.
El tractament del vidre
El tractament del vidre es realitza en diverses fases i comporta la utilització de diverses tècniques, segons el producte final desitjat. Per a començar, es prepara la mescla. Es barregen les diverses substàncies, dosificades acuradament en funció del tipus de vidre que es vulgui obtenir, i es molen finament en molins especials. Seguidament, la mescla se sotmet a fusió i a cocció en uns forns també especials. Durant la fase de cocció, la massa s’escalfa primer a una temperatura de 1 200-1 400°C, i posteriorment a uns 1 500°C, per tal de completar l’eliminació de les bombolles d’aire i afavorir l’aflorament de les impureses no vitrificables, que són les escòries del vidre.
A continuació, la pasta fosa es deixa refredar parcialment, fins que està a punt per a ser modelada segons diferents tècniques. Un dels procediments més antics, conegut a Síria ja al segle I aC, és la del bufat, que avui dia només es realitza als tallers artesanals. Un cop s’ha obtingut la pasta vítria, que es manté fluida en recipients de terra refractària a uns 1 200°C, s’hi introdueix l’extrem de la canya del bufador (un tub llarg generalment de ferro) i es recull la quantitat de pasta necessària per a l’objecte que es vol modelar. Aquesta quantitat de pasta s’amassa primer sobre una superfície plana per a un modelatge previ, i després es va bufant per la canya i, alternativament, es va rescalfant la pasta per mantenir-la tova. En la fase final, quan s’han aconseguit les formes i les dimensions desitjades, es fan els acabats plàstics, estirant i modelant el vidre amb unes pinces (o amb pintes per fer nervadures) i tallant-lo amb cisalles. L’objecte fabricat es col·loca en un forn de refredament en què recupera la temperatura normal de forma gradual.
A més del bufat, hi ha altres tècniques de modelatge d’ús freqüent com són la colada, que es fa en motlles que reprodueixen la forma dels objectes desitjats; l’estampació, que s’efectua comprimint o bufant la pasta fosa en motlles; el laminatge, que permet l’obtenció de làmines o planxes de vidre i que consisteix a fer passar la pasta entre corrons que giren en sentit contrari, i l’estiratge, procediment pel qual s’expulsa la pasta per unes obertures de determinades dimensions.
El modelatge en calent no constitueix, però, l’última operació. Abans que es refredi el vidre, es procedeix al tremp, un procés que consisteix en un refredament gradual de la pasta i que té lloc en forns alimentats amb calor recuperada. L’objectiu del tremp és evitar que les tensions internes, causades per caigudes brusques de la temperatura, debilitin el material. A partir d’aquí, el vidre ja està a punt per a les operacions d’esmolament, poliment, gravació o decoració.
Productes de ceràmica i materials refractaris
Aquest sector industrial agrupa nombrosos productes obtinguts per mitjà del tractament de l’argila. Pastada amb aigua, en una proporció màxima del 70%, l’argila adquireix un aspecte plàstic i es pot modelar en la forma desitjada. Però, així que s’escalfa a una temperatura elevada, s’endureix per sempre. Aquesta és la seva propietat principal.
L’argila deriva de la descomposició d’unes roques determinades, anomenades feldspats, constituïdes bàsicament de silicats d’alumini i metalls (alcalins o alcalinoterris). Això no obstant, no és possible indicar una composició fixa de l’argila, ja que el fenomen de la descomposició rocosa segueix evolucions variables i les roques no tenen sempre el mateix origen. L’argila és la base de la ceràmica. Per a fabricar peces ceràmiques és necessari, primer de tot, preparar la pasta. L’argila s’ha de pastar amb aigua durant una bona estona i, eventualment, amb altres ingredients que en facilitin l’enduriment, fins que s’obtingui una barreja consistent. Per a obtenir la pasta, cal extreure’n les partícules més grosses i l’aigua sobrant, de manera que es torni densa i compacta. Després es pot comprimir i laminar fent-la passar a través de corrons.
Aleshores comença el modelatge, que pot realitzar-se en un torn, en el cas que es vulguin fabricar objectes artístics, o bé en motlles i en premses, si es tracta de fabricació industrial. D’altra banda, per a l’obtenció de maons, es fan servir màquines amb fileres, en què un cargol helicoïdal expulsa la pasta per forats de dimensions determinades.
Seguidament, es passa a la fase de dessecació, que ha de ser gradual i uniforme i que té lloc en espais tancats especials, adjacents als mateixos forns en què es procedirà a la cocció, de manera que se n’aprofita la calor. La cocció es produeix a temperatures que poden oscil·lar entre 900 i 1 500°C, segons el tipus d’argila i els altres ingredients usats. Normalment, si es vol envernissar l’objecte, és necessària una primera cocció a una temperatura més elevada, amb la qual s’obté el que s’anomena bescuit, i, seguidament, una segona cocció, que té com a objectiu coure el vernís, que s’afegeix a la peça entre la primera i la segona cocció. També pot efectuar-se una tercera cocció per a fixar-ne la decoració. La tècnica d’envernissar consisteix a aplicar sobre el bescuit, per aspersió o amb pinzell, un vernís transparent, d’una composició semblant al vidre. Però també és possible fer servir vernissos opacs o esmalts, que s’aconsegueixen afegint als vernissos transparents diòxid d’estany, criolita o cendres d’ossos. Els materials que componen les peces ceràmiques per a la construcció (teules, maons massissos o foradats, blocs) no es diferencien dels que s’empren en la fabricació de la ceràmica artística o destinada al parament de taula. De tota manera, és cert que les peces de ceràmica es comercialitzen per separat, ja sigui perquè tenen unes aplicacions específiques, o bé perquè es produeixen en fàbriques especialitzades. Per als materials de la construcció, la primera matèria és l’argila comuna, que passa pels mateixos processos que hem descrit, a excepció de l’envernissament. La cocció es fa generalment en un forn especial, anomenat forn de Hoffmann, de funcionament continu, i a una temperatura de 800-900°C.
És sabut que a l’interior dels forns es produeixen grans quantitats de calor i s’hi assoleixen temperatures molt altes. Per tant, és d’una importància cabdal el material amb què es revesteix l’interior dels forns i de les cambres calorífiques. Aquests materials es designen amb el nom de refractaris, i han de posseir unes propietats específiques si es vol evitar que el forn es faci malbé o fins i tot que es fongui. En primer lloc, els materials refractaris han de ser resistents a la calor i a les exigències mecàniques. En segon lloc, han de ser necessàriament poc porosos i han de tenir una escassa dilatació tèrmica, mentre que poden ser bons conductors de calor o no segons l’ús que se’n vulgui fer.
Els refractaris naturals, és a dir, els que s’obtenen a partir de materials presents en la naturalesa, se seleccionen en funció de la composició química. Un grup important de refractaris naturals és el dels refractaris neutres. S’inclouen en aquest grup els refractaris argilosos, aluminosos i de carboni. Els argilosos estan constituïts d’argila cuita segons els procediments habituals i resisteixen, depenent de cada tipus, temperatures compreses entre 1 300°C i 1 600°C. En canvi, en el cas dels refractaris aluminosos, l’argila es cou amb la bauxita i, d’aquesta manera, suporta temperatures que arriben als 1 900°C. Quant als materials refractaris de carboni, es componen de grafits, coc o carbó, i es consideren pràcticament infusibles, per bé que no poden utilitzar-se amb substàncies capaces de reduir-se.
La sorra d’emmotllament és un refractari especial emprat en la indústria metal·lúrgica. Es tracta normalment de mescles de sorra, argiles i altres ingredients segons la peça fabricada, indispensables en la fabricació de peces de metall. La sorra d’emmotllament es comprimeix entorn del model que reprodueix la peça en qüestió. D’aquesta manera s’obtenen els motlles en què es colaran els metalls i els aliatges fosos. Per això, aquests materials refractaris, que són de gran importància, no poden experimentar cap variació i les seves dimensions han de ser constants durant l’escalfament; al mateix temps, han de posseir prou porositat per a deixar filtrar l’aire generat per la colada.
Els materials de construcció
És fascinant veure construir un pont, un dic, una casa o els seus fonaments. Es pot observar com de mica en mica els materials aglomeradors permeten la cohesió sòlida i durable dels diversos elements de la construcció, o fins i tot es fan servir per a fabricar estructures portants. Prenguem, doncs, els materials de construcció per descobrir-ne les propietats i els aspectes principals. Els materials bàsics de la construcció són el guix, la calç i els aglomerants hidràulics.
El guix, utilitzat ja pels egipcis, és l’aglomerant més antic que es coneix. Es troba en la natura en forma de mineral compost de sulfat de calci dihidrat. En coure’s a una temperatura de 170-200°C, en forns rotatius o en marmites, el mineral perd aigua i es transforma en sulfat de calci deshidratat, que és utilitzat, segons el grau de finesa, per diferents professionals, com ara paletes o artistes. I és que el guix té cada cop més aplicacions i és emprat en àmbits més diversos, els quals inclouen des del camp de la construcció i la decoració fins al modelisme o la traumatologia (el “guix” utilitzat per a immobilitzar els membres que han sofert una fractura òssia). Malgrat tot, aquest material també té les seves limitacions. Per exemple, no es pot fer servir per sobre de 120°C perquè pot provocar la deshidratació dels cristalls i la disgregació dels materials. Tampoc no és apte per a la construcció exterior, les clavegueres o les fosses sèptiques, ja que el contacte amb l’aigua, amb vapors amoniacals o també amb el ferro, en provoca la disgregació.
La calç es feia servir usualment com a aglomerant fins a la introducció del ciment. Avui, gairebé no s’utilitza, encara que en ocasions es barreja amb el ciment per donar-li flexibilitat. El procés de preparació de la calç té com a base diversos tipus de pedres calcàries, que es couen a uns 900°C en forns de calç, on el carbonat de calci es transforma en òxid de calci, més conegut amb el nom de calç viva.
La calç viva es descarrega en forma de terrossos i s’introdueix en tines o tambors rotatius, on se sotmet al que s’anomena apagament, és a dir, la barreja amb aigua. S’obté així una massa pastosa de calci, que rep el nom de calç apagada (amarada o morta). L’aigua sobrant es converteix, segons la quantitat que en resta, en lletada de calç o aigua de calç. La calç morta és dessecada fins que se n’obté una pols. El volum de calç morta obtingut a partir d’una determinada quantitat de calç indica la seva qualitat. Així es poden distingir les calçs grasses, que donen més calç morta i s’amaren més, de les calçs magres, que proporcionen menys calç morta i s’amaren menys.
El fenomen de la presa es deu al diòxid de carboni present en l’aire. El diòxid de carboni es desfà en l’aigua de dissolució de la calç morta, que com hem vist es compon d’hidròxid de calci i de diòxid de carboni, es genera calor i es forma carbonat de calci. L’evaporació de l’aigua fa possible que el carbonat de calci se solidifiqui en cristalls compactes i adherents de calcita. Com és lògic, la reacció es produeix mentre hi ha prou aigua per a dissoldre el diòxid de carboni. Quan no és així, el procés s’atura i el morter es torna “mort”.
Pel que fa als aglomerants hidràulics, cal dir que s’anomenen d’aquesta manera perquè es prenen en contacte amb l’aigua. Les classes d’aglomerants hidràulics que més es fan servir són les putzolanes, les calçs hidràuliques i els ciments. Les putzolanes són unes roques silícies poroses, pròpies de Pozzuoli, una ciutat de la Campània italiana. Constituïdes per cendres i pols volcàniques consolidades, estan formades per compostos d’òxids de sílice, alumini, ferro, calci, magnesi, potassi i sodi. Solen utilitzar-se mòltes i barrejades amb calç en la fabricació de ciment hidràulic. Per la seva banda, les calçs hidràuliques s’obtenen per mitjà de la cocció de calcàries argiloses. Amb la cocció, la calcària es transforma en òxid de calci, que es combina amb l’alúmina, la sílice i l’hidròxid fèrric de l’argila i forma un compost dotat de capacitat hidràulica, ja que en contacte amb l’aigua no es comporta com la calç sinó més aviat com el ciment.
Finalment, cal assenyalar el ciment, el material de construcció per excel·lència. El que normalment es coneix com a ciment també rep el nom de pòrtland, a causa de la semblança d’aquest material amb les pedres calcàries dels imponents penya-segats de la península homònima, a la costa sud-est d’Anglaterra. Els components bàsics dels ciments naturals són les calcàries argiloses o margoses, que poden incloure del 22% al 27% d’argila. Els ciments artificials, en canvi, es produeixen a partir de la mescla de calcàries i argila en les dosis desitjades.
La fase de preparació del ciment es pot fer en sec o en condicions d’humitat. En el primer cas, els components es trituren per separat, es mesclen, es dessequen i, al final, es molen finament. En l’altre cas, els components es trituren i es molen amb aigua i s’uneixen finalment en un mesclador. La fase següent és la de la cocció, a 1 450°C, en forns rotatius, de 100 metres de llargada i de 2 a 3 metres de diàmetre, lleugerament inclinats i revestits a l’interior de materials refractaris. La pasta fluida s’introdueix des de dalt, mentre que l’aire s’insufla des de baix, on hi ha el cremador de gas, nafta (mescla d’hidrocarburs) o carbó. Des de l’orifici de l’extrem, es descarrega l’anomenat clinker, en forma de trossos foscos, que s’envien a la mòlta per convertir-los en pols fina, el ciment.
El ciment s’utilitza normalment en mescles per a l’obtenció de morter, formigó o formigó armat, segons les necessitats. En el cas del morter, l’amalgama es fa amb sorra, ciment, calç i aigua. El formigó es prepara barrejant ciment amb sorra, grava i aigua, mentre que el formigó armat consisteix a reforçar el morter o el formigó amb una armadura de ferro a fi de millorar-ne la resistència a la flexió i a la tracció.
Un dels principals punts febles del ciment rau en la formació de calç hidratada durant la presa, la qual cosa fa que el ciment s’erosioni fàcilment per l’efecte de l’aigua de pluja o de solucions aquoses que continguin bicarbonat de calci i diòxid de carboni i que, a resultes d’això, s’hi formin porus. Els sulfats també agredeixen el ciment, ja que creen un sulfoaluminat, anomenat el “bacil del ciment”, que n’augmenta el volum en un 70% i en disgrega la massa.
A més del ciment pòrtland, n’hi ha d’altres amb aplicacions especials. Els dos més freqüents són el ciment de forn alt, que aprofita les escòries siderúrgiques, i el ciment putzolànic, que barreja el clinker amb les putzolanes. Tots dos ciments presenten una major resistència a l’agressió de l’aigua i la salinitat. D’altra banda, cal esmentar els ciments de gran resistència, seleccionats per mitjà de condicionaments i de processos de cocció molt acurats amb l’objectiu de millorar la capacitat de suportar la tracció i la compressió; i els ciments blancs, obtinguts a partir de la mescla de caolins purs i calcàries per a usos ornamentals. També cal fer referència als ciments de ferro, que es preparen amb una proporció d’òxid fèrric més alta, amb vista a afavorir la resistència als agents químics.
La indústria farmacèutica
La indústria farmacèutica és una branca especialitzada del sector químic que s’encarrega de l’estudi, la preparació i la comercialització dels productes medicamentosos. Aquest sector, que sorgeix de la necessitat de proveir els productes que responen a les demandes sanitàries de la població, ha adquirit unes dimensions considerables en el transcurs dels anys, tant pel que fa als equipaments com a les inversions de capital o al volum de negoci. Hi tenen una especial rellevància els sectors encarregats de la recerca i de l’experimentació científica, els quals fan de la farmacologia un camp especialment dinàmic i innovador.
Simplificant al màxim els processos de producció, que són força complexos i variats segons el producte que es vulgui aconseguir, podem indicar dues fases essencials en la producció farmacèutica. La primera és la formació per síntesi dels compostos que constitueixen els principis actius dels fàrmacs. L’equipament industrial de què es disposa per a la realització d’aquestes síntesis (majoritàriament orgàniques) és molt variat, tant pel que fa al tipus d’aparells com a la naturalesa dels materials utilitzats. Pràcticament totes les operacions de la química orgànica es troben reproduïdes en l’àmbit de la producció, des de la mescla amb dissolvents, el rescalfament en l’autoclau i la destil·lació fins a la filtració, la cristal·lització o l’extracció dels dissolvents, entre d’altres.
La segona fase consisteix en el trasllat de les substàncies preparades segons els procediments esmentats al magatzem de primeres matèries i, d’aquí, a les diverses seccions on es realitzen les operacions tècniques farmacèutiques que donen al fàrmac la seva presentació i dosificació establertes per tal que el medicament exerceixi els efectes esperats.
Una indústria que darrerament ha assolit dimensions considerables, clarament diferenciada de la indústria farmacèutica, és la cosmètica, que engloba empreses que elaboren una extensa gamma de productes (des de sabons fins a xampús, dentifricis, productes de maquillatge, cremes hidratants o perfums) utilitzats per a netejar, perfumar, protegir i embellir la pell, els cabells o les dents. Antigament, es preparaven amb ingredients naturals i de manera artesanal, però avui els productes cosmètics es componen de primeres matèries majoritàriament sintètiques, estudiades per una branca especialitzada de la química, la cosmètica.
El tractament del paper
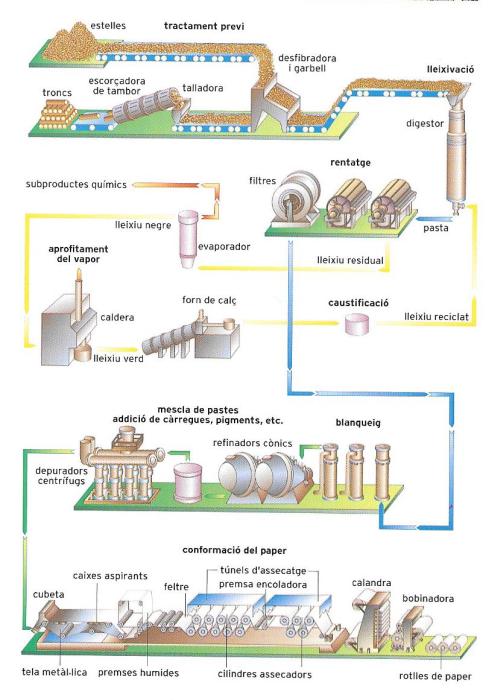
Esquema de la fabricació de paper, que comprèn la preparació de la pasta i la fabricació pròpiament dita. Al final del procés, es pot donar al paper un tractament superficial (estucatge o setinatge).
ECSA
El tractament del paper és una activitat amb una llarga història (vegeu “La transmissió del text”). Els actuals procediments per a la fabricació del paper s’estructuren en dues fases principals; en la primera, es prepara la pasta de cel·lulosa a partir d’una primera matèria fibrosa derivada bàsicament de la fusta, mentre que en la segona fase s’elabora el paper pròpiament dit.
La pasta de cel·lulosa s’obté desfibrant els troncs triturats en aigua bullent (pasta mecànica) i tractant químicament la pasta per mitjà de certs reactius, com ara sulfats o sulfits de sodi, amb la finalitat de separar la lignina i les substàncies acompanyants, que convé eliminar al màxim. La cel·lulosa crua, un cop rentada per tal d’extreure’n els residus lignis, es blanqueja amb reactius oxidants (clor, hipoclorits o peròxid d’hidrogen). Actualment, es tendeix a abandonar l’ús del clor elemental a causa de l’alt grau contaminant dels residus líquids que genera (vegeu “El paper “ecològic””). També hi ha altres tractaments mixtos, però mantenen una quantitat superior de lignina a la pasta. El paper de maceració recuperat dels diaris no venuts, dels residus de la fabricació i de la recollida selectiva, un cop desfet i llevades la tinta i altres impureses, constitueix un material fibrós que es recupera per a la fabricació de nombrosos tipus de paper, anomenat llavors paper reciclat, utilitzat en premsa i en material d’oficina.
La pasta mecànica no necessita cap altre tractament, tret dels ja esmentats, mentre que les pastes químiques i semiquímiques s’han de sotmetre a un tractament mecànic de refinatge. El material es desfà en una gran quantitat d’aigua fins a formar una pasta, que es refina fent-la passar per dues sèries de tallants.
Segons l’ús a què és destinat el paper, la pasta pot contenir altres components, per exemple els anomenats materials de càrrega, com el caolí, el carbonat de calci o d’altres, que fan el full de paper més blanc, més opac i més receptiu a la tinta d’impressió. Les coles són substàncies resinoses que s’afegeixen a la pasta per fer possible la impressió amb tintes aquoses. El paper encolat és especialment apte per a l’escriptura manual o mecànica. A més, la incorporació de colorants permet obtenir totes les tonalitats possibles o corregir el color groguenc de les matèries fibroses.
En finalitzar els tractaments mecànics i químics descrits, s’envia la pasta a una màquina contínua per transformar-la en paper. Primerament, es dilueix la pasta amb molta aigua i s’aboca sobre una taula plana, formada essencialment per una tela de malla ampla i contínua, de fils metàl·lics o sintètics, que avança ràpidament. La major part de l’aigua s’escola a través de la malla, mentre que les fibres i els altres components sòlids de la pasta queden retinguts a la superfície. La tela passa per damunt d’una sèrie de caixes aspiradores, on es fa el buit, que extreuen una quantitat d’aigua superior a la que s’escolaria amb la força de la gravetat. A l’extrem de la taula plana, la tela torna enrere, girant al voltant d’un cilindre aspirador, que també és al buit, que elimina l’aigua restant. En aquest punt, tot i que encara és molt humit, el full ja s’ha format i es pot desenganxar de la tela. Aleshores, s’estén sobre un feltre o un altre teixit molt absorbent i se’l fa passar per uns corrons que el comprimeixen, de manera que el feltre absorbeixi l’aigua que hi restava. Amb tot, el paper encara conté entre el 55% i el 70% d’aigua, que no es pot extreure amb mètodes mecànics. Per tant, s’envia a una assecadora formada per un gran nombre de tambors assecadors, escalfats amb vapor a una temperatura de poc més de 100°C. Tal com surt de l’assecadora, el full és massa rugós i encara no es pot emprar. Normalment, abans d’empaquetar-lo, és allisat a través d’una sèrie de corrons, que el comprimeixen intensament i en fan uniforme la superfície. La majoria dels papers d’impremta estan revestits d’una capa molt fina de vernís, anomenada pàtina, composta de pigments (caolí, carbonat de calci o diòxid de titani) i d’un adhesiu que fa la funció d’aglomerant (midó, caseïna o aglomerants a base de resines sintètiques).
La fabricació del paper és un procés en sèrie dirigit per un complex mecanisme automàtic de regulació i ajust, controlat per sensors de pes, humitat, gruix, color, opacitat i llisor, instal·lats en diferents màquines del procés. Aquests mecanismes estan coordinats i controlats per ordinadors que permeten reduir al mínim la intervenció humana en el funcionament de les màquines.