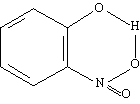
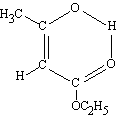
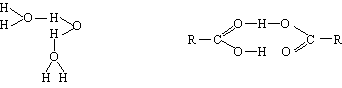Aquest fenomen és el responsable de les propietats físiques anormals que presenten l’aigua, l’amoníac, els alcohols, els fenols, els àcids carboxílics, etc. Hom el troba en dissolucions, en líquids purs i en vapors i es manifesta pels mètodes corrents de determinació de pesos moleculars, puix que les molècules associades es comporten com a unitats de pes molecular múltiple, segons el grau d’associació.