Per hidròlisi, l’aigua reacciona amb els cations per a produir bases febles, i amb els anions per a donar àcids febles. La sal d’un àcid feble i d’una base forta, la d’una base feble i d’un àcid fort i la d’un àcid i una base febles tenen tendència a hidrolitzar-se. El grau d’hidròlisi és la relació entre el nombre de mols hidrolitzats i el nombre total de mols de sal. En el cas de la reacció d’hidròlisi de l’ió acetat, CH 3 COO - + H 2 O ⇌CH e - COOH + OH - , la constant de dissociació és donada per l’equació
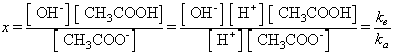
K e essent la constant de dissociació de l’aigua i K a la constant de dissociació de l’àcid acètic. Industrialment tenen importància la hidròlisi de les matèries grasses per a obtenir els àcids grassos i el glicerol, i la hidròlisi de les proteïnes per a obtenir els aminoàcids constitutius. En bioquímica té molta importància la hidròlisi de certs enllaços de composts rics en energia, com l’ATP.