No existeix cap definició absoluta del terme, puix que molts reactius poden comportar-se com a oxidants o reductors, segons el sistema enfront del qual actuen: així, per exemple, el peròxid d’hidrogen, que actua generalment com a oxidant, actua com a reductor enfront del permanganat en medi àcid:
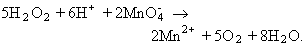
No obstant això, els potencials d’oxidació-reducció
constitueixen una mesura, exacta si hom treballa en condicions de reversibilitat, del poder oxidant de les substàncies. Els composts emprats comunament com a oxidants pertanyen a tipus molt diversos, i entre ells cal esmentar, a més de l’oxigen i l’ozó, el peròxid d’hidrogen i diversos peroxiàcids, les solucions àcides, neutres o bàsiques de permanganat potàssic, triòxid de crom i dicromat potàssic, diversos òxids metàl·lics (tetròxid d’osmi, diòxid de manganès, diòxid de seleni), diversos oxoàcids halogenats i llurs sals (hipoclorit, clorat, àcid periòdic), àcids minerals (àcid sulfúric, àcid nítric) i sals de les valències superiors d’alguns metalls —clorur de ferro (III), nitrat de ceri (IV), tetraacetat de plom—.