Un corol·lari d’aquesta relació és la constància aproximada de l’entropia de vaporització de les substàncies líquides:
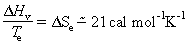
Cal fer esment del fet que els líquids associats presenten desviacions notables (aigua, 26,1; etanol, 26,9), i també els líquids de punt d’ebullició elevat (cadmi, 22,9; argent, 24,6) i els de pes molecular i de punt d’ebullició baixos (nitrogen, 17,2; oxigen, 18,1). L’any 1915 J.H. Hildebrand introduí en aquesta regla una modificació, consistent a mesurar les entropies de vaporització a temperatures tals que les concentracions moleculars del vapor (P/RT) fossin constants, amb la qual cosa s’obtenen resultats molt més concordants.