Les solucions amortidores, dites també solucions tampó, deuen llurs propietats a la presència d’un sistema amortidor constituït, en general, per una mescla d’un àcid feble i una de les seves sals, o d’una base feble i una de les seves sals, o de dues sals estadis successius de la neutralització d’un poliàcid. Escollint convenientment l’àcid (o la base) i les concentracions relatives, és possible d’obtenir solucions amortidores per a qualsevol valor del pH. La magnitud de l’efecte amortidor és molt considerable. L’addició de 10 ml de solució normal d’àcid fort a un litre d’aigua pura fa passar el pH de 7 a 2. La mateixa quantitat d’àcid afegida a un litre de solució decinormal en àcid acètic i en acetat sòdic, fa baixar el pH (a 25°C) només de 4,74 a 4,66. L’acció dels sistemes amortidors s’explica pel fet que les solucions d’àcids i de bases febles són poc ionitzades i, per tant, llur pH depèn molt poc de la concentració. Si a una solució que conté, per exemple, l’àcid feble HA i la seva sal MA, hom afegeix un àcid o una base forta, les reaccions són, respectivament:
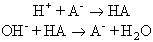
En ambdós casos els ions H⁺ o OH- afegits desapareixen i només varia la concentració de HA. És en virtut d’això que hom diu que les solucions amortidores tenen una reserva alcalina (o una reserva àcida). Quantitativament l’efecte amortidor és deduït de l’equació aproximada d’Henderson-Hasselbach: pH = pKA + log CS/CA, que mostra que en una solució de l’àcid feble A i de la seva sal S, les variacions del pH resten limitades a les variacions del logaritme del quocient de les concentracions. La capacitat amortidora de la solució és màxima quan aquest quocient és igual a 1 i és proporcional a la concentració total. Els líquids biològics són tots solucions amortidores. A la sang, el principal sistema amortidor és el sistema àcid carbónic-bicarbonats. A més dels sistemes amortidors de pH hi ha també sistemes amortidors d’òxidoreducció, que tendeixen a estabilitzar el potencial d’òxidoreducció de les solucions.