Què és el SARS-CoV-2?
El SARS-CoV-2 és el virus responsable de la covid-19 (acrònim de l’anglès coronavirus disease 2019, per l’any en què es va iniciar la pandèmia). Pertany a la família dels coronavirus, que s’anomenen d’aquesta manera per l’aspecte que tenen les glicoproteïnes que cobreixen la seva superfície, que tenen forma de corona solar. Són causa de diverses malalties, que acostumen a afectar, entre altres òrgans i sistemes del cos, l’aparell respiratori. S’han identificat set coronavirus capaços d’infectar els humans (anomenats genèricament HCoVs): HCoV-OC43, HCoV-HKU1, HCoV-229E i HCoV-NL63, que són causa d’un percentatge significatiu de refredats comuns, i el SARS-CoV, el SARS-CoV-2 i el MERS-CoV, que s’associen a epidèmies amb una afectació respiratòria d’intensitat variable. El SARS-CoV, o simplement SARS, per exemple, va provocar un brot epidèmic l’any 2002, i el MERS ho va fer el 2012, cap dels quals, però, va esdevenir una pandèmia global.
Els coronavirus es caracteritzen per tenir el material genètic format per un RNA de cadena senzilla positiva (ssRNA+, de l’anglès single stranded RNA +). Això significa que el seu material genètic és format per una sola cadena d’àcid ribonucleic la qual pot ser llegida i traduïda directament pels ribosomes de les cèl·lules que infecta, per produir totes les proteïnes necessàries per a la seva replicació. En el cas concret del SARS-CoV-2, el seu material genètic és format per uns 33.500 nucleòtids (33.5 kilobases o 33.5 kb), la qual cosa fa que sigui el virus d’RNA més gran identificat fins l’actualitat. Aproximadament dues terceres parts del seu material genètic, els anomenats fragments ORF1a i ORF1b, codifica per a 16 proteïnes no estructurals (anomenades nsp1 a nsp16), la majoria de les quals són necessàries per al procés de replicació del genoma víric. L’altra tercera part codifica les proteïnes estructurals E (de l’embolcall), M (de la membrana), N (de la nucleocàpsida on s’uneix el genoma víric) i S (de les espícules), a banda d’algunes altres proteïnes accessòries implicades en la capacitat d’evasió del virus als sistemes de resposta immunitària innata (Figura 1).
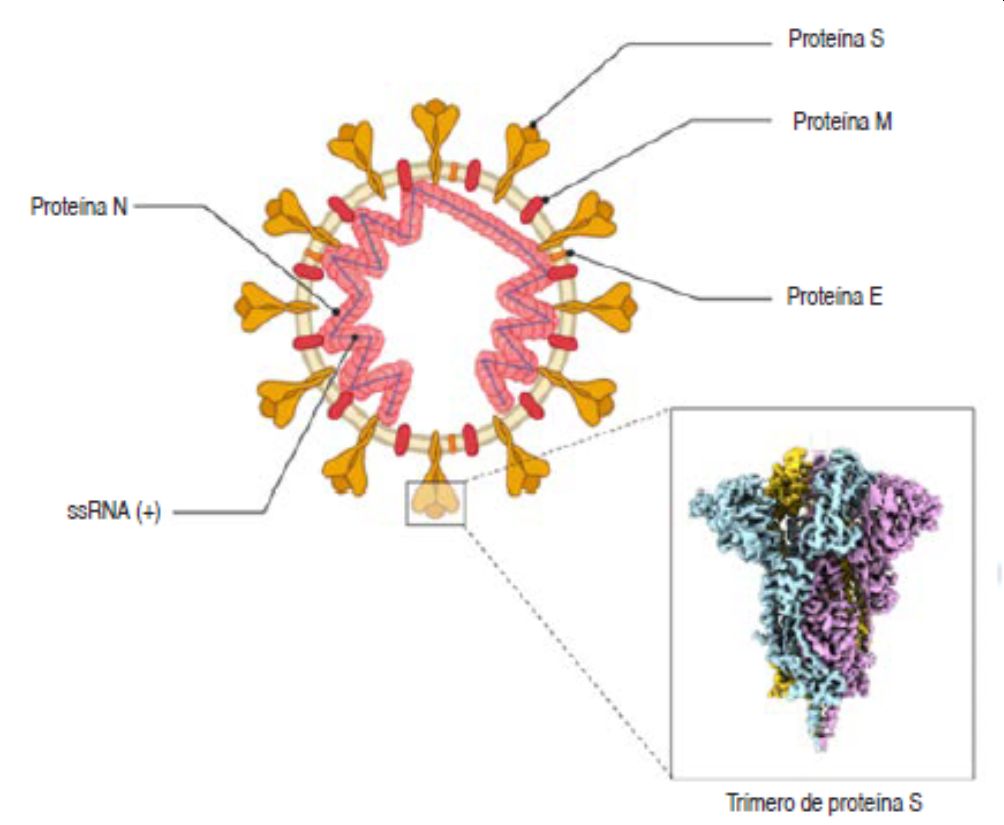
Estructura molecular del SARS-CoV-2
© Fernández-Camargo DA , Morales-Buenrostro LE. (2020). "Biología del SARS-CoV-2". Rev Mex Traspl 9 S2): s139-s148. doi: 10.35366/94503
Com es produeix la infecció del SARS-CoV-2?
Durant la infecció, el SARS-CoV-2 entra als pneumòcits de tipus II i en altres cèl·lules de l’aparell respiratori i d’altres òrgans del cos mitjançant la unió de la proteïna S a un receptor cel·lular específic, anomenat ECA2. Els pneumòcits de tipus II formen part dels alvèols pulmonars, on es produeix la incorporació de l’oxigen atmosfèric, i la seva funció és secretar una substància anomenada surfactant pulmonar que afavoreix aquest procés d’intercanvi de gasos. Per això un dels símptomes de la covid-19 és la pneumònia. Pel que fa al receptor ECA2, o enzim convertidor d’angiotensina, participa en la regulació de la pressió arterial i produeix pèptids antiinflamatoris, la qual cosa explica la inflamació pulmonar típica en un percentatge significatiu de persones afectades per la covid-19.
Una de les vies més habituals d’infecció del SARS-CoV-2 és a través de les foses nasals. La proteïna S també permet que el SARS-CoV-2 infecti cèl·lules de l’epiteli olfactiu de la cavitat nasal i s’hi repliqui, i des d’elles es pot propagar a la resta de les vies respiratòries fins als pulmons. Aquesta infecció de l’epiteli nasal explica la pèrdua d’olfacte que experimenten algunes persones amb covid-19. A més, el receptor ACE2 també es troba en altres diversos teixits, inclòs el sistema cardiovascular, el tracte gastrointestinal i el sistema nerviós central, la qual cosa justifica les afectacions gastrointestinals, circulatòries i neurològiques que s’han descrit en alguns malalts amb símptomes greus. En aquest sentit, es creu que determinats macròfags situats a la melsa i als ganglis limfàtics (els anomenats CD169+) poden servir com a portadors virals que poden mantenir la càrrega viral en les persones infectades i facilitar la disseminació d’aquest virus en altres teixits. Els macròfags són cèl·lules del sistema immunitari i la seva funció normal és detectar, fagocitar i destruir bacteris i cèl·lules infectades per virus.
Una vegada dins el citoplasma de la cèl·lula hoste, el genoma viral és reconegut pels ribosomes, que són les estructures cel·lulars encarregades de desxifrar i traduir el missatge del material genètic per fabricar les proteïnes corresponents. Llavors s’inicia la traducció del gen de la replicasa del SARS-CoV-2, a partir del quals es fabriquen les 16 proteïnes no estructurals (nsp1 a nsp16) que conformen el complex proteic implicat en la replicació de l’RNA víric. La replicació del material genètic del virus es produeix en petites vesícules que es formen a partir del reticle endoplasmàtic rugós de la cèl·lula hoste, un orgànul cel·lular la funció normal del qual és la síntesi i el transport de proteïnes i la glicosilació de les glicoproteïnes (Figura 2).
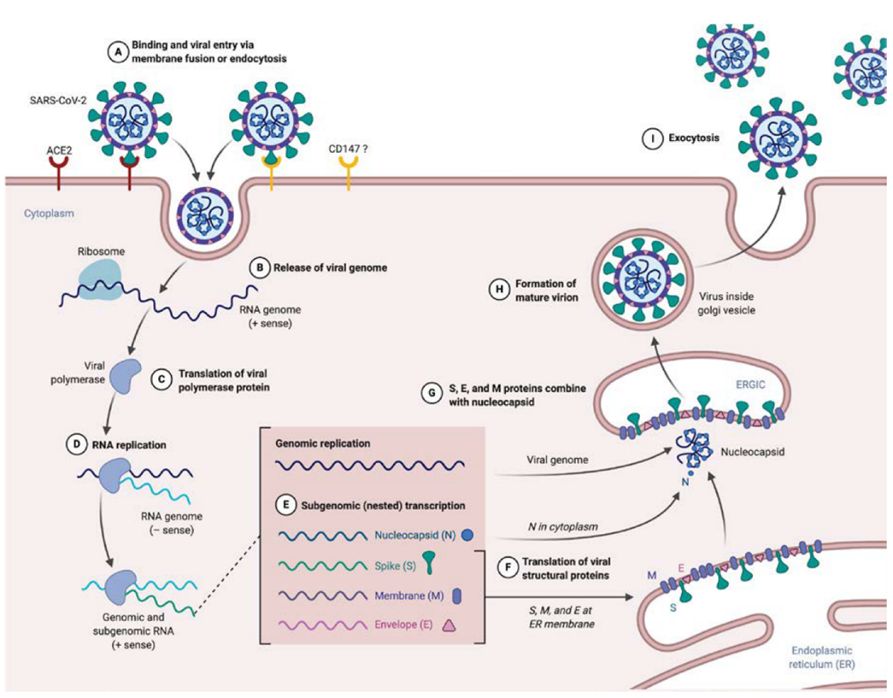
Cicle infectiu del SARS-CoV-2
© www.mdpi.com/1422-0067/21/16/5932
Dins d’aquestes vesícules, l’RNA víric es transcriu a una còpia d’RNA de cadena negativa, que és complementària a la positiva, i llavors aquesta còpia complementària de cadena negativa és utilitzada de motlle per fer els nous genomes virals d’RNA de cadena positiva. En aquest procés intervé també una exonucleasa (ExoN), un enzim fabricat a partir de la informació genètica del mateix virus la funció del qual és mantenir la fidelitat del procés de transcripció del genoma i, per tant, evitar l’acumulació de mutacions. Dit d’una altra manera, malgrat que es vagin produint soques noves de SARS-CoV-2 per mutació, aquest sistema fa que el potencial per mutar que té aquest virus sigui molt inferior al d’altres virus. Simultàniament també es fabriquen les proteïnes E, M i S, que s’associen al reticle endoplasmàtic, i la proteïna N, que s’uneix als RNA virals a mesura que es van produint. Finalment aquestes vesícules migren cap a la membrana plasmàtica de la cèl·lula hoste on son alliberades a l’exterior, la qual cosa els permet tornar a iniciar el cicle infectiu amb altres cèl·lules.
Com respon el cos a la infecció?
Després de l’entrada del virus a les cèl·lules hoste, el sistema immunitari innat comença a reconèixer l’RNA viral i s’inicia una resposta immunitària immediata i inespecífica. Les cèl·lules encarregades són, principalment, les cèl·lules dendrítiques del sistema immunitari, la funció de les quals és fagocitar els elements estranys i presentar-los a la seva superfície perquè siguin reconeguts per altres cèl·lules del sistema immunitari. Això desencadena cascades de senyalització que porten a la producció d’interferons, que, al seu torn, inicien la síntesi de proteïnes antivirals. I també s’activa l’anomenat factor de transcripció NFκB, que indueix la producció de citocines proinflamatòries. Aquestes citocines, juntament amb altres mediadors d’inflamació alliberats com a conseqüència dels danys cel·lulars derivats de la infecció, recluten altres cèl·lules del sistema immunitari, com macròfags i neutròfils. Tanmateix, quan l’activació d’aquest sistema de defensa innat és excessiu, s’afavoreixen processos de vasodilatació, de fugida vascular i de producció d’edema alveolar que en conjunt causen hipòxia, un altre dels efectes greus de la simptomatologia de la covid-19.
Paral·lelament, s’inicia una resposta immunitària específica o adquirida, en la qual determinats tipus de limfòcits T inicien la producció d’anticossos neutralitzants. Aquests anticossos reconeixen específicament zones concretes de les proteïnes de la coberta vírica, la qual cosa té un paper molt important en el control de la infecció i en la prevenció de reinfeccions futures. També redueixen la infectivitat dels virus, atès que eviten o dificulten que s’uneixin als receptors cel·lulars, i estimulen la lisi de les cèl·lules infectades a través de l’anomenat sistema del complement del sistema immunitari per evitar que serveixin de vehicle de propagació del virus. Finalment, un cop superada la infecció es produeixen cèl·lules de memòria, la funció de les quals és permetre una resposta molt ràpida i específica davant una nova infecció, per evitar que es produeixi o per reduir-ne la gravetat. Precisament, una de les funcions de les vacunes és activar la resposta immunitària específica per generar cèl·lules de memòria que evitin possibles infeccions o que en redueixin significativament la gravetat, atès que la resposta immunitària és molt més ràpida i específica.
En aquest sentit, una de les possibles conseqüències que poden tenir les soques o variants noves de SARS-CoV-2 que es van formant espontàniament per mutació és que s’hagin alterat algunes d’aquestes proteïnes de superfície. Això els permetria escapar amb més facilitat de l’acció de la resposta immunitària adquirida, tant si s’ha generat després d’una infecció com per vacunació. Fins a finals del 2021 s’havien identificat cinc variants potencialment infectives de SARS-CoV-2, anomenades alfa, beta, gamma, delta i òmicron, i n’hi ha dues més que estan sent monitoritzades per veure quin abast poden arribar a tenir, anomenades lambda i mi.