Resultats de la cerca
Es mostren 13 resultats
cianamida
Química
Cristalls obtinguts industrialment per carbonatació de la cianamida de calci
.
S'obté segons les equacions Té caràcter d’àcid dèbil dipròtic, i són importants, comercialment, les seves sals de sodi i de calci Aquesta darrera és anomenada, sovint, simplement cianamida
àcid pivàlic
Química
Sòlid incolor que es fon a 35°C i bull a 164-168°C.
És poc soluble en aigua i soluble en alcohol i èter Hom l’obté per tractament amb hipoclorit sòdic de la pinacolona Presenta una acidesa molt dèbil És emprat com a intermediari en síntesi orgànica
àcid tel·lúric
Química
Oxoàcid del tel·luri que, en estat sòlid, presenta l’estructura octaèdrica de Te(OH)6.
És un sòlid cristallí, soluble en aigua calenta i en els àlcalis, que es fon a 136°C Hom el pot preparar per oxidació del telluri o del diòxid TeO 2 amb peròxid d’hidrogen En dissolució, es comporta com un àcid dibàsic molt dèbil pK 1 =7 i presenta caràcter oxidant
ricinina
Química
Alcaloide de dèbil toxicitat i gust amarg present a les llavors del ricí.
És un sòlid cristallí incolor, soluble en l’aigua i el cloroform calents, que es fon a 202°C
acridina
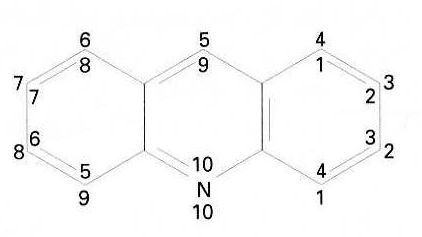
Acridina
©
Química
Compost heterocíclic.
Dóna en els dissolvents orgànics solucions de fluorescència blava És una base dèbil i forma sals cristallines, grogues, amb els àcids minerals És extret de la fracció antracènica del quitrà d’hulla i pot ésser preparat per síntesi Té escasses aplicacions, ja que els seus derivats importants són preparats a partir d’altres primeres matèries El seu punt de fusió és de 111℃ i el d’ebullició de 346℃
mètode de Fischer
Química
Procediment químic d’anàlisi de traces d’aigua.
Aquest mètode es basa en el fet que l’anhídrid sulfurós no redueix el iode amb una solució de metanol i piridina, segons una reacció estequiomètrica, si no és en presència d’aigua La reacció de base és 2H 2 O + SO 2 + I 2 → SO 4 H 2 + 2IH o més exactament segons la reacció final següent La piridina base orgànica dèbil és indispensable per a neutralitzar les quantitats d’àcid en excés, puix que la primera reacció és reversible quan la quantitat d’àcid passa del 0,05% D’aquí ve la possibilitat de calcular la quantitat d’aigua d’una mescla per la mesura de la quantitat de iode…
calor de reacció
Química
Energia tèrmica alliberada o absorbida en qualsevol procés químic.
Quan aquest és dut a terme a pressió constant, l’esmentada energia coincideix amb la que en termodinàmica rep el nom d' entalpia , i quan ho és a volum constant, amb l’anomenada energia interna Segons la natura del procés, la calor de reacció té expressions pròpies Així, la calor de formació d’un compost és l’increment d’entalpia que tindrà lloc quan un mol d’aquest és format teòricament a partir dels seus elements considerats en l’estat tipus, a una pressió i una temperatura determinades la calor de combustió , quan és cremat completament un mol, a una temperatura determinada i a la pressió…
àcid sulfhídric
Química
Denominació de les solucions aquoses del sulfur d’hidrogen (H2S), tòxiques i de dèbil acidesa (pK1=7; pK2=15).
Té aplicació com a agent precipitant de cations d’abast molt general
acidimetria
Química
Part de la volumetria
que comprèn els mètodes d’anàlisi de substàncies de caràcter bàsic per valoració amb una solució d’un àcid de concentració coneguda.
Els mètodes de l’acidimetria són fonamentats en reaccions de neutralització , quan és una base lliure la que hom valora amb la solució àcida, o de desplaçament , quan la substància valorada és una sal d’un àcid molt dèbil i l’agent valorant un àcid fort Hom calcula la quantitat de substància bàsica problema a partir del volum d’agent valorant àcid necessari perquè la reacció arribi a ésser completa, moment que la solució assoleix un valor específic del pH Hom posa de manifest aquest moment mitjançant l’ús d’alguns dels indicadors de neutralització , substàncies orgàniques àcides…
anilina
Química
Fenilamina C 6
H 5
NH 2
Amina primària, la més simple de les aromàtiques.
Líquid oliós, incolor, d’olor característica, que s’embruneix a l’aire i a la llum Se solidifica a -6,2°C i bull a 184,4°C És una base dèbil pk B = 9,30 i és poc soluble en aigua però miscible amb la major part de solvents orgànics Fou obtinguda per primera vegada per Unverdorben 1826 per destillació destructiva de l’indi Fristzche la preparà el 1841 tractant l’indi amb hidròxid potàssic i li donà el nom d’anilina del portuguès anil És present en petita quantitat al quitrà d’hulla i és obtingut en grans tonatges per síntesi El procediment actualment més important és la reducció…