Resultats de la cerca
Es mostren 6 resultats
aristoloquina
Química
Alcaloide tòxic que hom extreu d’algunes aristolòquies, de cristalls de color marró, brillants, que es descomponen a l’entorn de 281°-286°C, solubles en alcohol, cloroform, èter i àlcalis.
Causa aturades cardíaques i respiratòries, i té ús medicinal
salbutamol
Farmàcia
Química
Substància cristal·lina que es fon a 157-158°C.
És un estimulant adrenèrgic dels receptors β 2 ubicats en l’arbre bronquial És administrat sobretot per via inhalatòria perquè el seu efecte directe permet l’administració d’una dosi baixa Hom l’empra com a broncodilatador en el tractament de malalties respiratòries obstructives reversibles
adamsita
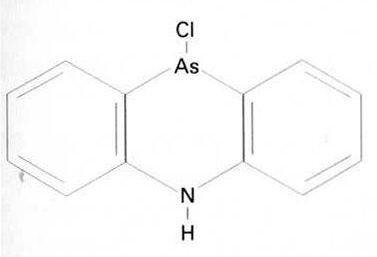
Adamsita
©
Química
Agent agressiu químic.
És un sòlid de color groc canari, molt venenós, irritant de la pell i de les vies respiratòries, insoluble en aigua obtingut escalfant difenilamina amb triclorur d’arsènic Les forces de policia l’utilitzen en forma de fum i sovint barrejat amb gasos lacrimògens per a dispersar manifestacions Provoca secreció nasal, tos i esternuts, dolors, mareigs i vòmits, depressió i feblesa Els seus efectes persisteixen un cert temps, però normalment no tenen conseqüències posteriors El punt de fusió és a 195ºC, i el d’ebullició a 410ºC
càmfora
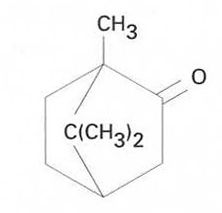
Càmfora
©
Farmàcia
Química
Cetona terpènica existent en les seves dues formes òpticament actives i com a racèmic.
És obtinguda per destillació amb arrossegament de vapor de la fusta del camforer hom assoleix, així, la forma dextrogira Té el punt de fusió a 179,75ºC i el d’ebullició a 204ºC Les zones productores de càmfora més importants són el Japó, Taiwan i algunes comarques de la Xina central La forma sintètica racèmica és obtinguda a partir del pinè Els seus cristalls fan una olor penetrant característica És soluble en els dissolvents orgànics i en els àcids minerals És emprada com a plastificant de la cellulosa hom n'usa els èters i èsters en la fabricació de plàstics, sobretot celluloide, laques i…
monòxid de nitrogen
Química
Gas incolor, d’un punt d’ebullició de -151,8°C i un punt de fusió de -163°C, poc soluble en aigua.
En contacte amb l’aire és oxidat ràpidament a NO 2 , de color bru Reacciona amb clor i brom i dona halurs de nitrosil, NOX És preparat en el laboratori per reacció del coure amb àcid nítric diluït, i en la indústria per oxidació catalítica de l’amoníac com a pas intermedi en la fabricació de l’àcid nítric, i també segons l’equació A la dècada del 1980 s’iniciaren una sèrie d’experiments que revelaren que el monòxid de nitrogen, un gas que havia estat considerat només com un contaminant atmosfèric, era generat pel metabolisme cellular i tenia una àmplia gamma de funcions biològiques com a…
amoníac

Propietats físiques de l’amoníac
©
Química
Gas incolor, més lleuger que l’aire, compost de nitrogen i hidrogen.
L’amoníac té una olor pungent característica i irrita els ulls i les vies respiratòries El llindar de percepció se situa a 0,04 g/m 3 53 ppm i la màxima concentració tolerable és de 0,3%o en volum a 4-5%₀ esdevé mortal En la natura, l’amoníac es forma en la descomposició de la matèria orgànica nitrogenada i hom el troba, en petita quantitat, a l’atmosfera i en moltes aigües naturals La solució aquosa d’amoníac era ja coneguda dels alquimistes al segle XV Priestley l’aïllà a l’estat gasós el 1774 i Berthollet establí la seva composició el 1785 La molècula…