Resultats de la cerca
Es mostren 23 resultats
detector d’ionització gasosa
Física
Detector de radiació constituït per un recinte ple de gas la ionització del qual s’utilitza per a produir el senyal de detecció.
gasós | gasosa
enriquiment
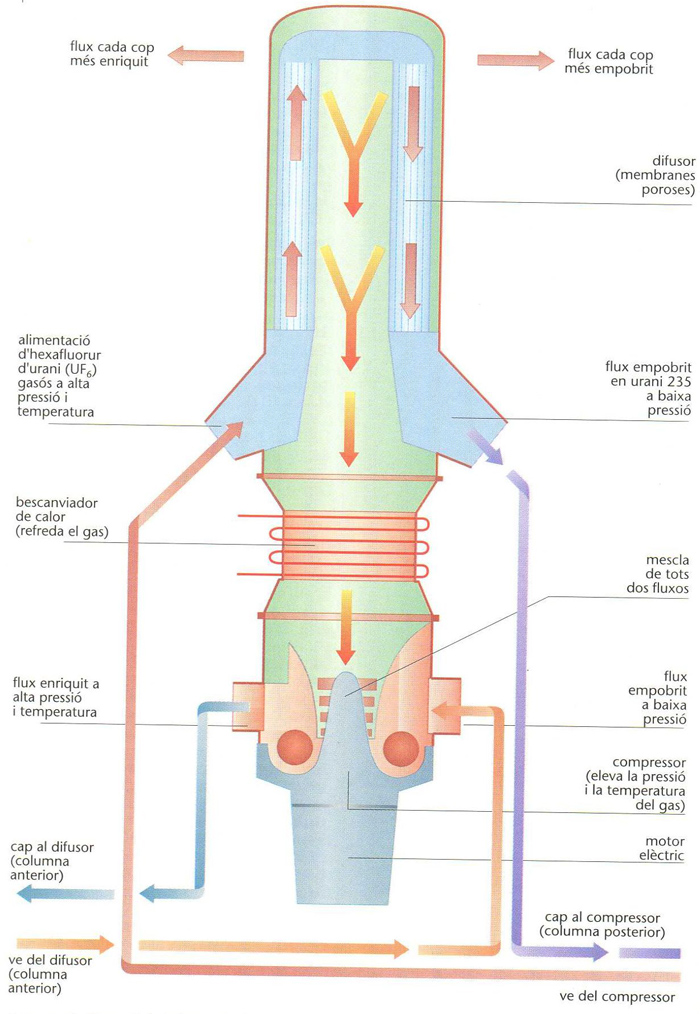
Columna de difusió gasosa per a l' enriquiment de l’urani: les molècules de gas amb l’isòtop 235, més lleugeres, travessen més ràpidament el disufsor; repetint moltes vegades l’operació, es forma un flux cada vegada més ric en urani 235
© Fototeca.cat
Física
Química
Procés per mitjà del qual hom incrementa la proporció amb què es presenta un component d’una mescla, en detriment dels altres.
L' enriquiment de l’urani té per objecte augmentar la proporció d’urani-325 el material fissible que hi ha en una mostra d’urani natural, en què es barreja aquest isòtop amb el d’urani-328 Els prosessos d’enriquiment, siguin per difusió gasosa o per centrifugació , aconsegueixen que la proporció de l’U-235 passi del 0,72% a prop del 3%
vapor
Física
Dit de la fase gasosa d’una substància que és a una temperatura inferior a la temperatura crítica.
Bé que correntment hom anomena vapor el gas que és pròxim a la condensació o el que correspon a la fase gasosa d’una substància que, en les condicions habituals de pressió i de temperatura, és també en estat sòlid o líquid, com és ara l’aigua, des del punt de vista d’estat d’agregació vapor i gas són una mateixa cosa
llei de Boyle-Mariotte
Física
Cas particular de l’equació d’estat d’un gas perfecte.
Estableix que, a temperatura constant, el volum ocupat per una massa gasosa és inversament proporcional a la pressió a la qual és sotmès el gas Analíticament, s’expressa pV = constant, on p representa la pressió total, i V el volum de la massa gasosa
estat d’agregació
Física
Estat d’un sistema material segons el grau de cohesió de les molècules que el formen.
Segons l’estat d’agregació, un sistema material es pot presentar en tres fases fonamentals, sòlida, líquida i gasosa , i hom anomena canvi d’estat o canvi de fase el pas d’un d’ells a un altre qualsevol
funció de Gibbs
Física
Funció termodinàmica G definida per l’equació G = U-TS+pV = H-TS (U essent-hi l’energia interna, T la temperatura absoluta, S l’entropia, p la pressió, V el volum i H l’entalpia).
Anomenada també entalpia lliure , és una funció d’estat del sistema considerat Una propietat important és que, per a un sistema en equilibri, la funció de Gibbs específica té el mateix valor per a les fases líquida i gasosa Una conseqüència d’aquesta propietat és la regla de les fases o de Gibbs fase
tensió de vapor d’aigua
Meteorologia
Física
Pressió parcial que exerceix el vapor d’aigua contingut en l’atmosfera.
El seu valor pot augmentar fins a un límit tensió màxima o saturant a partir del qual el vapor d’aigua es condensa fins que el volum de la porció que resta en forma gasosa no excedeix del que és compatible amb la tensió saturant La tensió màxima del vapor d’aigua depèn de la temperatura
cremador
Física
Aparell emprat per a barrejar un combustible amb aire o oxigen per tal d’ésser cremat.
Els més simples regulen el fluix del combustible que es crema en contacte amb l’aire ambient Atès que la combustió només té lloc en fase gasosa, els cremadors de combustibles líquids o sòlids carbó polvoritzat han d’assegurar la polvorització del combustible i barrejar-lo uniformement amb l’aire necessari per a la combustió Certs combustibles, com el petroli i el fueloil pesant, han d’ésser escalfats abans de la polvorització
gas
Física
Estat de la matèria en què les molècules que el componen resten poc lligades entre elles per les forces de cohesió.
No presenta ni una forma ni un volum definits, sinó que sempre omple totalment i uniformement el recipient que el conté És costum de dir que una substància és gas quan es presenta en forma gasosa a la temperatura ambient La densitat dels gasos sempre és més petita que la de la mateixa substància a l’estat sòlid o líquid, car, en el gas, les molècules resten molt més separades La calor específica d’un gas depèn de les condicions en què té lloc la variació de la seva temperatura a pressió constant o a volum constant La calor específica a pressió constant…