Resultats de la cerca
Es mostren 7 resultats
configuració electrònica
Física
Distribució dels electrons d’un àtom o molècula en els diversos orbitals d’aquests.
Per a deduir les configuracions electròniques dels àtoms, hom es basa en el fet que un àtom multielectrònic pot collocar els seus electrons en un conjunt d’orbitals formalment anàleg al de l’àtom d’hidrogen, bo i seguint l’ordre de menor a major energia dels orbitals i tenint en compte el principi d’exclusió L’ordre en què es van emplenant d’electrons els orbitals d’un àtom neutre és 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 6d, ~ 5f orbital atòmic La configuració electrònica d’un àtom és simbolitzada per mitjà de la notació dels orbitals amb un índex volat…
model atòmic de Schrödinger
Física
Química
Model derivat de l’aplicació de l’equació de Schrödinger (Hψ = Eψ) per a l’estudi de l’estructura atòmica.
Per a un sistema determinat, les diferents funcions pròpies ψ, solucions de l’equació, són conegudes com a orbitals orbital , i són caracteritzades per uns valors propis que corresponen a l’energia dels esmentats orbitals El mòdul al quadrat de la funció ψ té el significat de la probabilitat de localització de l’electró que descriu l’esmentada funció en una regió determinada de l’espai, i la seva representació gràfica constitueix la imatge visual dels orbitals, habitualment emprada pels químics El coneixement exacte del hamiltonià H pot ésser únicament…
John Clarke Slater
Física
Físic nord-americà.
Ha investigat la teoria quàntica en àtoms, molècules i cristalls, els orbitals atòmics, les bandes d’energia en els cristalls, etc Ha publicat nombroses obres, sobretot de teoria atòmica
Kenichi Fukui
Física
Química
Químic-físic japonès.
Professor a la Universitat de Kyoto, compartí el premi Nobel de química del 1981 amb R Hoffmann , pels seus treballs d’aplicació de la mecànica quàntica a l’estudi dels orbitals fronterers en relació amb la reactivitat de les molècules
factor giromagnètic
Física
Quocient entre el moment magnètic i el moment angular d’un cos elèctricament carregat: g=μ/L.
En mecànica clàssica, g = q / 2m, essent m la massa del cos en qüestió i q la seva càrrega elèctrica En mecànica quàntica l’expressió continua essent vàlida per als moments magnètics associats als moments angulars orbitals, però no pas per als moments magnètics associats al spin, que depenen del tipus de partícula
àtom
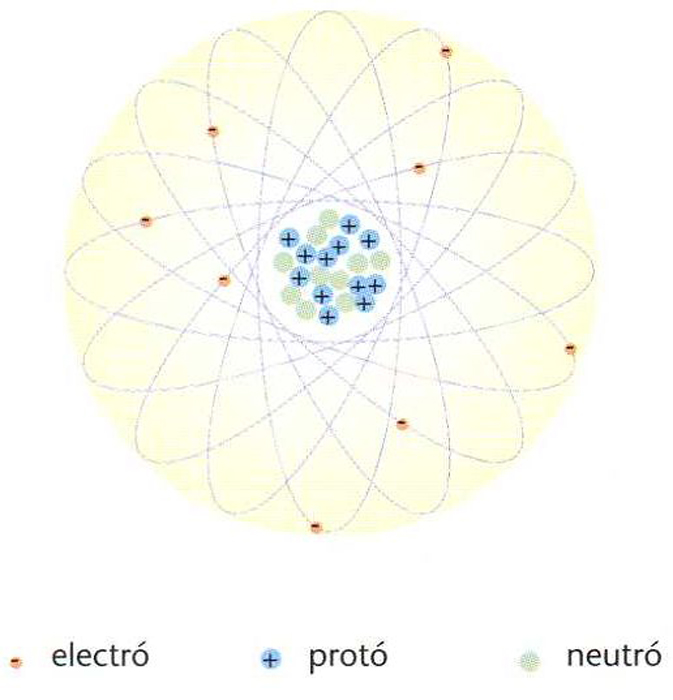
Model d’àtom de Bohr-Rutherford
© Fototeca.cat
Física
Sistema format per un determinat nombre de partícules elementals (essencialment protons, neutrons i electrons) que, essent elèctricament neutre, posseeix intrínsecament les característiques d’un element químic i n’és la quantitat més petita que pot intervenir en una combinació química.
Bàsicament un àtom consta de dues parts D’una banda el nucli , format per protons i neutrons, que conté gairebé tota la massa de l’àtom ~99,9% però que només n’ocupa una part infíma ~10 - 5 vegades les seves dimensions Els electrons, d’altra banda, envolten el nucli formant capes a diferents nivells i, a conseqüència de llur càrrega elèctrica negativa, neutralitzen la càrrega positiva del nucli Les masses dels àtoms van dels 10 - 2 7 kg als 10 - 2 5 kg, i llurs dimensions dels 10 - 1 0 m als 10 - 9 m Els àtoms d’un mateix element tenen el mateix nombre de protons i electrons nombre atòmic, Z…
regla de Hund
Física
Regla segons la qual tots els orbitals d’un mateix nivell energètic han d’ésser ocupats per un electró abans que un d’ells pugui ésser ocupat per un doblet electrònic.