Resultats de la cerca
Es mostren 5 resultats
ebullioscòpia
Física
Química
Mètode per a determinar el pes molecular d’un compost químic en dissolució a partir de l’observació experimental del punt d’ebullició d’aquesta.
L’expressió que dóna el pes molecular del solut és M s = 1 000 a s K e | a d Δ T e , a s essent la quantitat de solut en dissolució donada en grams, a d la quantitat de dissolvent, també en grams, K e la constant molal del punt d’ebullició del dissolvent, i Δ T e , l’increment de temperatura del punt d’ebullició de la dissolució respecte al del dissolvent pur
osmosi
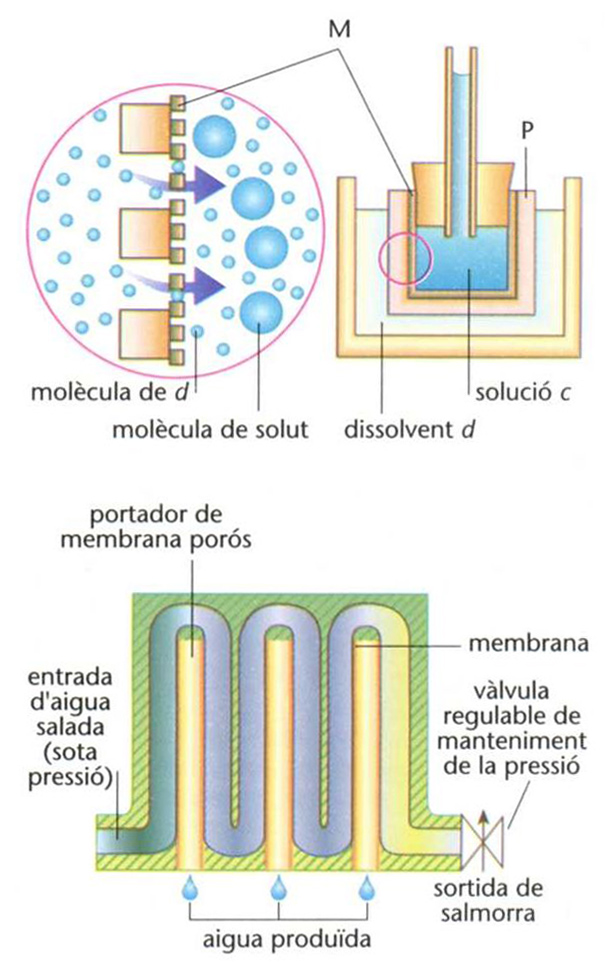
Omosi adalt, les molècules de d són les úniques que travessen la mambrana M (P suport porós); abaix, principi de funcionament d’una instalació d’osmosi inversa per a dessalar aigua de mar
© Fototeca.cat
Física
Química
En un sistema format per dues dissolucions de concentracions diferents, però amb el mateix dissolvent, separades per una membrana dita semipermeable,
tendència a passar dissolvent de la dissolució menys concentrada a la que ho és més.
Una membrana semipermeable, d’origen natural o artificial, és la que deixa passar uns tipus de molècules les del dissolvent i uns altres no les del solut
coeficient osmòtic
Física
Química
Coeficient introduït per Bjerrum, que inclou tots els factors que expressen la desviació del comportament d’una solució respecte del comportament ideal.
D’aquesta forma, per un component i d’una barreja, el potencial químic s’expressa per μ i =μ o i + g i RT ln x i on g i és el coeficient osmòtic i x i és la fracció molar del solut en la dissolució
llei de Beer
Física
Llei que permet de calcular la disminució de la intensitat d’un raig de llum, o d’una radiació electromagnètica semblant, després d’haver travessat una solució.
La quantitat de llum absorbida I és donada per l’expressió essent la intensitat del raig de llum incident, b el coeficient d’absorció per unitat de concentració de solut, que depèn de la longitud d’ona de llum emprada, c la concentració de la solució, i x el gruix travessat per la radiació L' absorbància de les substàncies que satisfan la llei de Beer és proporcional a la concentració
Peter Joseph Wilhelm Debye

Peter Joseph Wilhelm Debye
© Fototeca.cat
Física
Físic i químic alemany d’origen neerlandès.
Es doctorà a la Universitat de Munic 1910 i ocupà la càtedra de física a les universitats de Zuric, Utrecht, Göttingen i Leipzig El 1940 s’exilià als EUA, on fou nomenat professor de la Cornell University, Ithaca Nova York Estudià la teoria de les dissolucions de sals, els moments dipolars i l’estructura molecular Estengué la idea de la ionització de les sals en dissolució d’Arrhenius a l’estat sòlid cristallí, investigà el cas de les solucions concentrades i determinà de forma quantitativa el nivell d’associació existent entre les molècules de solut i les de dissolvent Els seus…