Resultats de la cerca
Es mostren 441 resultats
duresa de l’aigua
Química
Qualitat de l’aigua dura deguda al contingut d’ions de metalls pesants, principalment d’ions calci i magnesi.
La duresa temporal o carbònica , deguda al contingut de bicarbonats, pot ésser eliminada per ebullició, mentre que la duresa permanent , produïda per sulfats, clorurs i silicats, sobretot, no pot ésser eliminada d’aquesta manera La duresa total és la suma de la duresa temporal i de la duresa permanent La unitat de mesura de la duresa és el grau hidrotimètric el grau francès equival a 10 mg CaCO 3 /l, i el grau alemany, a 10 mg CaCO/l
Niels Bjerrum
Química
Químic danès, deixeble de Julius Thomsen i de Walter Nernst, professor del col·legi de veterinària i agricultura de Copenhaguen.
Feu importants aportacions en el camp de la química física i de l’electroquímica, amb estudis sobre la teoria àcid-base, la mesura de la concentració d’ions hidrogen i els electròlits amfòters Aplicà la teoria quàntica a l’estudi de les calors específiques dels gasos
permeasa
Bioquímica
Sistema transportador específic a través de membranes biològiques de natura totalment o parcialment proteica.
En un sol bacteri hi ha molts milers d’aquests sistemes La membrana interna dels mitocondris en té algunes que permeten de passar diversos metabòlits a través de la membrana així, n'hi ha per a l’ADP, ATP, fosfats, sucres, ions, hidroxils, àcids del cicle de Krebs, etc
anisotropia

Anisotropia
© NASA/Goddard Space Flight Center
Mineralogia i petrografia
Fenomen que presenten certes substàncies, una de les propietats físiques de les quals, almenys, varia segons la direcció.
Presenten anisotropia aquelles substàncies en els cristalls de les quals les molècules o ions no són disposats idènticament en totes les direccions Hom constata diferències sensibles quant a propagació de la llum índex de refracció, resistència a la tracció, dilatació lineal, piezoelectricitat, etc S'oposa a la isotropia
aluminó
Química
Aurintricarboxilat d’amoni.
Sòlid vitri de color groc terrós soluble en aigua Forma laques vermelles amb els ions Al 3 + , Fe 3 + , Be 2 + i altres menys corrents És emprat en la recerca qualitativa i en la determinació quantitativa colorimètrica de l’alumini, i també en l’anàlisi del Sc i de l’In
benitoïta
Mineralogia i petrografia
Silicat de titani i bari, BaTi(SiO3)3, del grup dels sorosilicats.
Els tetràedres formen anells triples, entre cada tres dels quals s’intercalen, alternativament, ions de Ba i de Ti Cristallitza en el sistema hexagonal, i forma cristalls de fractura concoidal d’un color blau clar, molt pleocroics Té duresa de 6-6,5 i pes específic de 3,65 És emprada en joieria
sensibilitat
Química
Quantitat mínima de substància que dóna resultat positiu en una reacció d’identificació.
En aquest sentit, la sensibilitat pot ésser expressada tant en termes de concentració com en termes de quantitat En l’actualitat, i gràcies al desenvolupament d’una gran varietat de reactius orgànics i organometàllics, hom disposa de reaccions d’extrema sensibilitat per a una gran majoria d’ions inorgànics, així com de grups funcionals orgànics
zirconat
Química
Denominació genèrica, no recomanada per la IUPAC, de diversos òxids dobles.
De fórmules generals M I 2 ZrO 3 , M 2 I I ZrO 4 i M 2 I Zr 2 O 5 , que hom obté per reaccions, a temperatures elevades, d’òxids, hidròxids o nitrats de zirconi i els corresponents compostos d’un altre metall, en els quals no existeixen ions de zirconat discrets
benzidina
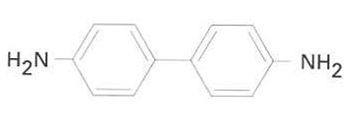
Benzidina
©
Química
Compost bàsic, que es presenta en forma de pólvores blanques o lleugerament vermelloses.
És obtinguda a partir de l’hidrazobenzè en presència d’àcids minerals mitjançant la transposició benzidínica Fon a 115-120ºC És emprada com a producte intermediari en la fabricació de colorants azoics, i en la caracterització i en la determinació d’ions inorgànics, sulfats i volframats Tòxica, produeix dermatitis i tumors a la bufeta
Paginació
- Primera pàgina
- Pàgina anterior
- …
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- …
- Pàgina següent
- Última pàgina