Resultats de la cerca
Es mostren 24 resultats
debye
Física
Unitat CGS-electroestàtica per a mesurar el moment dipolar elèctric, equivalent a 10-18 unitats electroestàtiques o 3,33×10-24 C.m.
apantallament de Debye
Física
Debilitació de l’atracció entre ions d’una dissolució causada per la formació, al voltant de cada ió, d’una atmosfera o pantalla d’ions de signe contrari (teoria de Debye-Hückel).
Peter Joseph Wilhelm Debye

Peter Joseph Wilhelm Debye
© Fototeca.cat
Física
Físic i químic alemany d’origen neerlandès.
Es doctorà a la Universitat de Munic 1910 i ocupà la càtedra de física a les universitats de Zuric, Utrecht, Göttingen i Leipzig El 1940 s’exilià als EUA, on fou nomenat professor de la Cornell University, Ithaca Nova York Estudià la teoria de les dissolucions de sals, els moments dipolars i l’estructura molecular Estengué la idea de la ionització de les sals en dissolució d’Arrhenius a l’estat sòlid cristallí, investigà el cas de les solucions concentrades i determinà de forma quantitativa el nivell d’associació existent entre les molècules de solut i les de dissolvent Els seus…
teoria de Debye-Hückel
Química
Teoria que explica les propietats de les solucions aquoses d’electròlits forts tot admetent que són completament dissociats en ions i que les desviacions observades respecte al comportament previst per l’equació d'Arrhenius provenen de llurs interaccions electroestàtiques.
La teoria suposa cada ió envoltat d’una “atmosfera” iònica de signe contrari apantallament de Debye i obté, per al coeficient d’activitat mitjà de l’electròlit, una fórmula simple, funció de la força iònica I , que per a solucions molt diluïdes se simplifica encara en una expressió independent de tot paràmetre La fórmula més simple coeficient d'activitat dóna valors en bon acord amb els experimentals només per a I < 0,003 la més complicada, que conté un paràmetre no calculable a priori , és vàlida fins a I ≈0,1 Més enllà, l’acord desapareix a causa de les aproximacions…
apantallament
Física
Efecte de pantalla pel qual un medi o un conjunt de partícules debiliten una determinada interacció; per exemple, hom diu que els electrons interiors d’un àtom apantallen l’atracció del nucli atòmic sobre els electrons perifèrics, ja que la debiliten.
L’apantallament té gran importància en la física de l’estat sòlid teoria BCS i en les dissolucions d’electròlits apantallament de Debye
Paul Scherrer
Física
Físic suís.
Ha fet recerques sobre els raigs X, física nuclear, teoria quàntica, estructura cristallina, magnetisme, etc L’any 1916 desenvolupà, amb Debye, un procediment d’aplicació dels raigs X a la indústria, per a l’anàlisi de substàncies en pols
efecte Compton
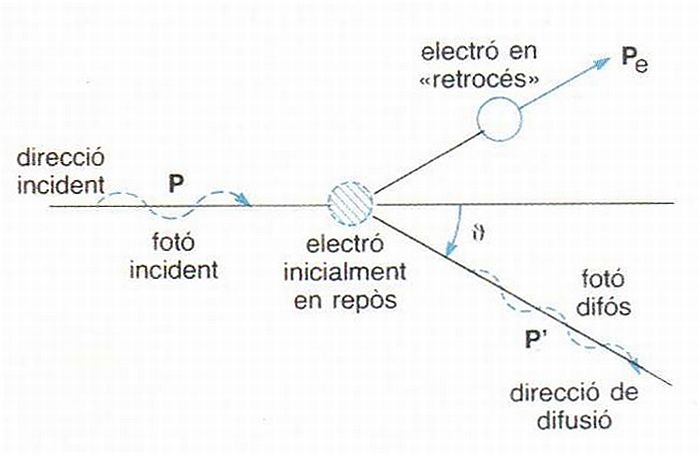
Efecte Compton
Física
Augment de la longitud d’ona de la radiació electromagnètica (en les bandes dels raigs X i raigs γ) difosa pels electrons menys lligats dels àtoms.
Fou observat per primera vegada per AH Compton i, simultàniament i independentment, per PJW Debye, el 1923 El fenomen s’esdevé en incidir un feix de radiació de freqüència ν sobre una làmina material hom observa que la radiació difosa té una freqüència menor, ν'
Lars Onsager
Física
Físic i químic noruec, naturalitzat nord-americà.
De molt jove es dedicà a l’estudi de la termodinàmica dels processos irreversibles Catedràtic a la universitat nord-americana de Yale des del 1945, aprofundí i millorà les teories de Debye i Lorentz sobre els electròlits i els dielèctrics Hom li deu la formulació del quart principi de la termodinàmica El 1968 li fou atorgat el premi Nobel de química
Émile-Eugène Darmois
Física
Físic francès.
Professor de física a la Universitat de Rennes i a la Sorbona Fonamentant els seus treballs en la teoria de Debye i Hückel sobre els electròlits, aconseguí d’explicar la variació de la viscositat de les solucions electrolítiques en funció de llur concentració També investigà la polarització rotatòria i la teoria general de les forces electromotrius El 1951 fou elegit membre de l’Académie des Sciences
producte de solubilitat
Química
Constant pròpia dels electròlits poc solubles, relativa a la dissociació de la molècula:
que és definida per l’expressió
, on a
representa les activitats de l’anió i del catió i v
el nombre d’anions i cations que es formen per cada molècula de solut.
El producte de solubilitat és constant a una temperatura determinada i la seva expressió pot ésser deduïda de la teoria de Debye-Hückel, tot i que ja fou introduïda, de manera aproximada, per W Nernst l’any 1889 A la pràctica, i suposat el cas de substàncies poc solubles dissoltes en aigua pura, hom pot substituir en la seva expressió les activitats per concentracions Atès que el producte de solubilitat regeix un equilibri que s’estableix en solució saturada, hom pot deduir del seu valor conseqüències de gran aplicació pràctica respecte a processos de dissolució i precipitació