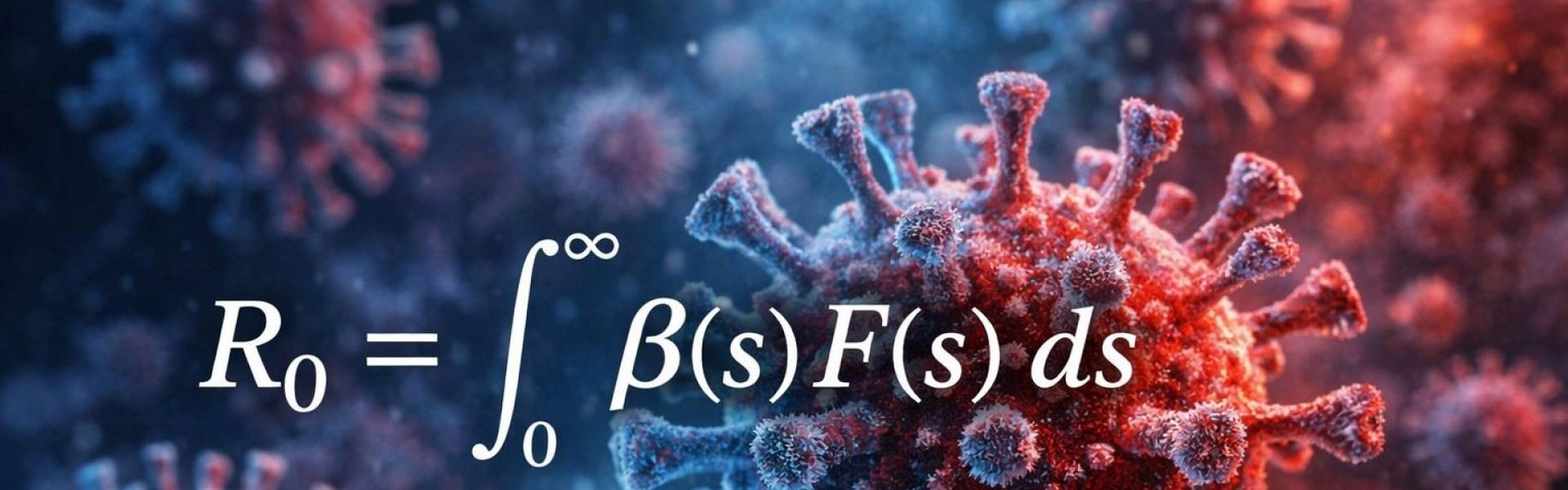
Per què s’acaba una epidèmia?
-
- Home
-
- 1 of 1
Aquesta pregunta, que avui té una resposta ben coneguda, no la tenia a principis del segle XX. De fet, per poder respondre-la abans calia saber quins són els agents causants de les malalties infeccioses i com es transmeten. Pensem que, fins a mitjan segle XIX, es creia que les malalties infeccioses eren causades per miasmes, que era com s’anomenaven els vapors o efluvis pudents que s’originaven a partir de matèria orgànica en descomposició, aigües estancades o sòls insalubres. L’origen del nom “malària”, de l’italià mal aria (mal aire), és un reflex d’aquesta creença.
Els treballs realitzats durant la segona meitat del segle XIX per investigadors com Louis Pasteur i Robert Koch, entre d’altres, van demostrar que malalties com la pesta del pollastre, el còlera o la tuberculosi eren causades per microbis. Curiosament, a més, en casos com la febre puerperal o el còlera, es va saber abans com es transmetia la infecció que no pas l’agent infecciós que la causava.

Figura 1: Imatge creada amb IA - Font: Elaboració pròpia.
Les epidèmies recurrents de xarampió
Un cop la teoria miasmàtica de les epidèmies va ser substituïda per la teoria microbiana, calia entendre la dinàmica de les epidèmies per poder-les controlar i, si fore possible, erradicar. A principis del segle XX, un dels reptes que hi havia era explicar el caràcter recurrent de malalties com el xarampió o la verola.
El metge anglès W.H. Hamer, en la tercera d’una sèrie de tres conferències fetes el 1906 al Royal College of Physicians de Londres, plantejà la tesi que el curs d’una epidèmia depenia de la taxa de contactes entre els individus susceptibles a la infecció i els individus infectats. D’aquesta manera, quan el nombre d’individus susceptibles baixava, també baixava el nombre de nous casos que es produïen, el que es coneix com a incidència. Així, després d’analitzar l’evolució en el temps dels nous casos (corba epidèmica) durant un brot de xarampió a Londres, Hamer diu (pàg. 54): “La corba del xarampió que acabem de definir mostra clarament que una epidèmia pot arribar al seu final, malgrat l’existència d’un gran nombre de persones susceptibles en la població, únicament sobre la base d’una ‘teoria mecànica de nombres i densitat’, i que la hipòtesi de pèrdua de virulència o poder infecciós per part de l’organisme (patogen) és totalment innecessària”.
Aquesta idea va derivar en el que més endavant va anomenar-se principi d’acció de masses, la teoria “mecànica” a la qual feia al·lusió Hamer. Segons aquest principi, la taxa d’aparició de nous casos (o taxa d’incidència) és proporcional al producte de nombre d’individus susceptibles pel nombre d’individus infectats.
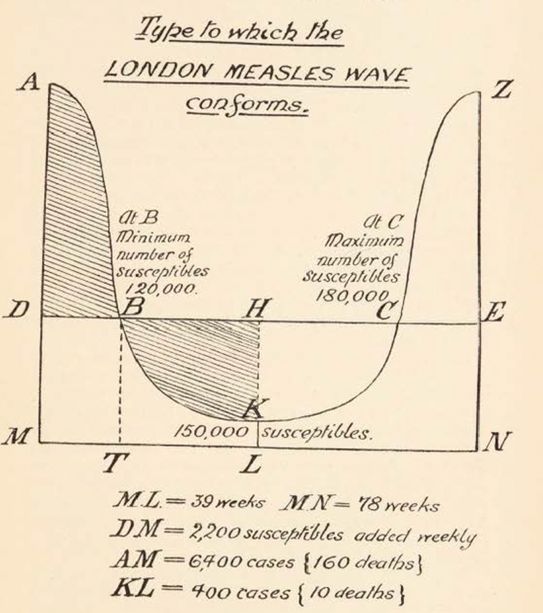
Figura 2. Corba epidèmica del xarampió - Font: Imatge treta de Hamer (1906); el llibre gaudeix de llicència CC Public Domain Mark
El mateix any de les conferències de Hamer, el 1906, el metge escocès John Brownlee presentava a la Royal Society of Edimburg un article on, després d’analitzar diverses corbes epidèmiques, defensava l’explicació contrària a la donada per Hamer per a l’acabament d’una epidèmia. Brownlee, com d’altres, defensava que la disminució del nombre de casos durant una epidèmia era causada per una pèrdua progressiva de la capacitat infecciosa del patogen quan aquest es transmet d’individu a individu. Així, les persones infectades serien cada cop menys contagioses, fins a arribar un moment en què l’epidèmia s’extingiria. De fet, aquest autor descartava la possibilitat que la capacitat infecciosa es mantingués constant (com suposava Hamer) perquè, segons ell, si cada infectat infectés sempre el mateix nombre de susceptibles, llavors acabarien no havent-hi susceptibles a qui infectar i la corba epidèmica tindria un final sobtat que no s’observava en les dades reals.
Enmig d’aquesta controvèrsia, el 1911 Ronald Ross publica l’article “Some quantitative studies in epidemiology” convidat per l’editor de la revista Nature, en què planteja un model dinàmic per a l’evolució del nombre de persones i mosquits infectats pel paràsit de la malària. Ross era un ferm defensor de la idea que, per entendre la dinàmica de les epidèmies, calia fer “una anàlisi acuradament raonada de les relacions entre la magnitud de la malaltia i els diversos factors que la influeixen”, és a dir, defensava la “quantificació” de l’epidemiologia, la qual cosa no era l’opinió majoritària en aquell moment. L’article és, de fet, un resum dels estudis quantitatius que apareixien en la segona edició del seu llibre Prevention of malària, i constitueix un exemple excel·lent de modelització.
El primer model per a la malària
La malària era una malaltia que plantejava un desafiament científic per la seva complexitat, i que tenia interès militar perquè afectava molts soldats de l’imperi Britànic en moltes zones on era present. Tot i que el 1880 el metge militar francès Alphonse Laveran va descobrir que la malària era causada per un paràsit (Plasmodium) —fet que li va valdre el premi Nobel de medicina el 1907—, no va ser fins el 1897 que no es va saber com es transmetia el paràsit.
El primer que va descobrir que el paràsit de la malària es transmet per la picada d’un mosquit va ser un altre metge militar, el britànic Ronald Ross, que ho demostrà en ocells (malària aviar). Poc després, el 1898, l’italià Giovanni Battista Grassi ho va demostrar en humans establint que eren les femelles del mosquit Anopheles les que transmetien el paràsit. Tanmateix, a diferència de Ross que el 1902 va rebre el premi Nobel de medicina pel seu descobriment, Grassi no el va rebre mai (malgrat haver-ne estat nominat en 21 ocasions!).
El model de Ross del 1911 era un sistema de dues equacions diferencials on s’assumia el principi d’acció de masses que Hamer havia intuït estudiant l’evolució del xarampió però, ara, entre els mosquits infectats i els humans susceptibles per un costat, i entre els humans infectats i els mosquits susceptibles per l’altre: mosquits i humans s’infecten mútuament i mantenen viva la presència de la malària.
Paga la pena presentar les equacions del model de Ross per veure com se’n deriva un resultat que va canviar la lluita contra la malària. Les equacions descriuen la variació en el temps del nombre de persones infectades i del nombre de mosquits infectats:
on
x és el nombre de persones infectades en una població de N individus;
y és el nombre de mosquits infectats d’una població total de n mosquits;
b és el nombre de picades d’un mosquit per unitat de temps (suposem que cada picada es fa a una persona diferent);
p és la probabilitat de transmissió en una picada de la malària d’humà a mosquit;
p’ és la probabilitat de transmissió de mosquit a humà;
r és la taxa a la qual els humans es recuperen de la malària i m la mortalitat dels mosquits.
El terme és, doncs, el nombre de picades per mosquit infectat i per unitat de temps que transmeten la malària a individus susceptibles (n’hi ha
), és a dir, el nombre de noves infeccions per mosquit infectat i per unitat de temps. Anàlogament, el terme
és el nombre de mosquits susceptibles (n’hi ha
) que contrauen la infecció en picar persones infectades.
Com que la malària és endèmica en molts llocs, Ross va considerar que el cas més interessant era aquell en què les poblacions d’humans i mosquits infectats assoleixen un valor constant x* i y*, respectivament, allò que avui en diem un equilibri endèmic. Per trobar-lo, només cal fer que les variacions temporals de x i y siguin igual zero i resoldre el sistema que en resulta. D’aquesta manera, trobem que l'equilibri endèmic predit pel model és:
Aquestes expressions mostren, com calia esperar, que el nombre de persones infectades x* creix amb la població total de mosquits n, i que, quan aquesta és molt elevada, gairebé tothom acaba infectat ( quan
).
Des del punt de vista de la lluita contra la malària, però, el resultat més important és que l’equilibri endèmic desapareix () quan n és igual al valor crític donat per
Aquest valor de n defineix el llindar crític de la població de mosquits per sota del qual la malària quedaria eliminada. En altres paraules, Ross va identificar els factors principals en la transmissió de la malària i va demostrar un fet que la majoria dels professionals que treballaven en salut pública no acceptava: reduir suficientment la població de mosquits permetia eliminar el caràcter endèmic de la malària en una regió. No calia, doncs, eliminar tota la població de mosquits per erradicar la malària. Pensem que, a principis del segle XX, l’opinió general era que lluitar contra els mosquits no era una estratègia encertada perquè era impossible eliminar-los completament d’una regió i, per tant, no servia per controlar la malària en els llocs on era endèmica.
Així, doncs, aquest resultat —que el mateix Ross va batejar com el “teorema del mosquit”—, el prestigi del mateix Ross i la seva empenta van contribuir a canviar la manera amb què es combatia la malària. De fet, anys abans de la publicació d’aquest article, Ross ja havia participat en campanyes de sanejament per reduir la població de mosquits a Ismaïlia (1903), la ciutat que va ser la base per a la construcció del canal de Suez i on va aconseguir controlar la malària que portava anys castigant la seva població (el 1904 no se’n va informar de cap cas). També va participar en una campanya a Freetown (1899-1901), la capital de Sierra Leone tot i que, en aquest cas, sense gaire èxit per la manca de continuïtat en l’aplicació de les seves mesures antimosquit. Les seves mesures també van ser adoptades amb èxit en altres zones com l’Havana (1901), durant l’ocupació militar de l’illa de Cuba pels Estat Units, o Panamà, durant la construcció del seu canal.
Per la seva banda, Grassi va proposar lluitar contra la malària amb mesures de prevenció per reduir les picades de mosquit. Davant la incredulitat dels seus compatriotes, l’estiu de 1900 Grassi va realitzar amb èxit un experiment amb voluntaris a Capaccio (Campània), la regió d’Itàlia més afectada per la malària, per demostrar l’eficàcia de mesures tan senzilles com instal·lar mosquiteres en finestres i portes. Al final de l’estiu d’aquell any, els casos de malària en les cases protegides van ser anecdòtics mentre que, a les cases que no ho estaven, la gran majoria dels voluntaris van contraure la malària. En el seu cas, les mesures no anaven dirigides a minvar la població de mosquits, sinó la transmissió de la malaltia. En termes del model de Ross, les mesures de Grassi fan disminuir la taxa de picades b i, per tant, augmenten el valor de .
Aquest model, completat posteriorment per George MacDonald durant la dècada dels 50, ha estat la base per a l’estudi de la propagació de les anomenades malalties vectorials, en què les infeccions són transmeses per vectors com ara mosquits, mosques, paparres o altres insectes. Aquesta aportació, per si mateixa, ja hauria fet que Ross fos mereixedor d’entrar per la porta gran a la història de l’epidemiologia. Pensem que més del 17% de les malalties infeccioses al món són transmeses per vectors.
Quan comença un epidèmia?
Saber per què s’acaba una epidèmia quan la infecció es transmet de manera directa entre individus no ho va dir Ross, malgrat haver publicat diversos articles que pretenien fonamentar una teoria general de les epidèmies i que ell anomenà “theory of happenings”.
De fet, per trobar una resposta abans cal saber respondre la pregunta “quan comença una epidèmia?” i això és el que van fer els escocesos William O. Kermack, químic, i Anderson G. McKendrick, metge, en un article que tots dos van publicar el 1927, titulat “A contribution to the mathematical theory of epidemics” i considerat per molts com l’article fundacional de l’epidemiologia matemàtica moderna.
McKendrick va coincidir amb Ross el 1901 en una de les campanyes contra la malària que aquest últim va dirigir a Sierra Leone, quan tots dos treballaven al Servei Mèdic de l’Índia de l’exèrcit britànic. Arran d’aquesta trobada, Ross va animar McKendrick, que acabava d’entrar al Servei Mèdic, a aprendre matemàtiques per poder-les aplicar a problemes mèdics. McKendrick va seguir el seu consell i, el 1926, va publicar l’article “Applications of mathematics to Medical problems” on ja introduïa algunes idees que després van desenvolupar-se a l’article del 1927. Una d’aquestes idees era dividir els membres d’una població en tres categories segons el seu estat: susceptibles a la malaltia (S), infectats (I) i recuperats (i immunes a noves infeccions) (R). Una idea senzilla però clau per a l’anàlisi del model i absent en els models de Ross.
La resposta que donen Kermack i McKendrick queda molt ben resumida a la introducció mateixa del seu article del 1927. Manllevant les paraules dels autors, podem dir que, si totes les persones són igual de susceptibles a contraure la malaltia i la infecció confereix immunitat completa i permanent, aleshores existeix una densitat poblacional crítica o llindar de població que dependrà de la taxa d’infecció i de la taxa de recuperació dels infectats. Si la població susceptible és inferior a aquest valor llindar, la introducció d’una o més persones infectades no originarà cap epidèmia. En canvi, si la població inicial és superior a la densitat crítica, aquesta introducció d’infectats farà que el seu nombre augmenti. Al mateix temps, la població susceptible anirà disminuint i, quan arribi a la densitat crítica, l’epidèmia començarà a minvar i, finalment, s’extingirà. El model considerat en aquest treball, conegut com a model SIR per les inicials dels estats dels individus, era determinista i suposava una població tancada, és a dir, sense naixements ni morts. En aquestes condicions, doncs, l’epidèmia s’extingeix perquè el nombre de susceptibles acaba sent massa baix per mantenir viva la cadena de contagis en la població.
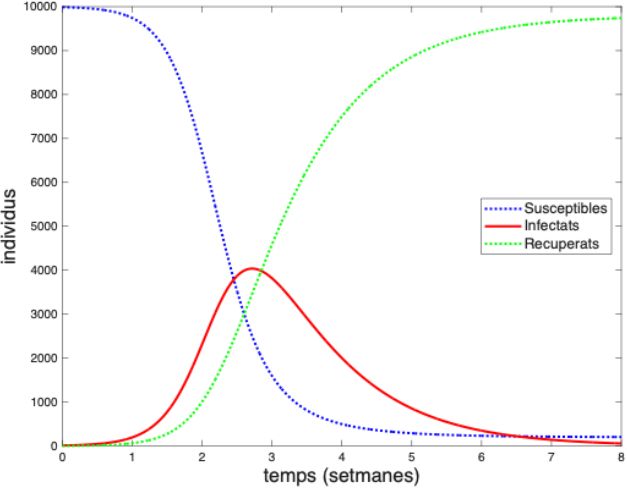
Figura 3. Exemple d’evolució del nombre d’infectats obtingut a partir del model SIR - Font: elaboració pròpia
Arribar a veure que calia una població mínima perquè es produeixi l’esclat d’una epidèmia quan hi ha transmissió directa va ser un procés més llarg que en el cas de la malària, tot i la complexitat de la transmissió d’aquesta última. Els 21 anys que van passar des de la conferència de Hamer de 1906 fins a la publicació de l’article de 1927 de Kermack i McKendrick no van servir per tancar el debat. De fet, en la introducció de l’article, els autors comenten que “dues de les raons que sovint s’addueixen per explicar la finalització d’una epidèmia són (1) que tots els individus susceptibles han estat eliminats, i (2) que, durant el curs de l’epidèmia, la virulència de l’organisme causant hagi anat disminuint gradualment”. En ciència, canviar de paradigma no és mai una cosa que es faci d’un dia per l’altre!
El nombre bàsic de reproducció R0
Kermack i McKendrick escriuen l’equació per a la població llindar N0 com , essent A la suma (de fet, la integral) de les infectivitats esperades d’un individu durant el temps que pot transmetre la malaltia (període infecciós). L’expressió de A depèn de la taxa de transmissió de la infecció i de la taxa de recuperació i, en el cas general ja suposat en l’article del 1927, ambdues taxes depenen del temps que es porta infectat.
Si reescrivim aquesta equació com , llavors N0 es pot interpretar com la mida que ha de tenir una població inicialment susceptible per garantir que una persona infectada produeixi (en mitjana) una sola infecció durant tot el seu període infecciós quan la resta de persones en són susceptibles. Per tant, en una població de mida N > N0, cada infectat acabarà produint més d’un infectat (AN > 1), és a dir, el seu nombre total començarà a créixer. Aquest nombre d’infeccions produïdes per un infectat a l’inici d’un brot epidèmic és el que avui anomenem “nombre bàsic de reproducció” (i representem per R0) i constitueix un concepte clau en l’epidemiologia actual.
Sorprenentment, però, no va ser fins al 1952 quan George MacDonald, estudiant les solucions d’equilibri d’un model de la malària i adaptant les idees de Ross, introdueix el nombre bàsic de reproducció en epidemiologia (abans ja s’utilitzava en demografia un concepte equivalent introduït per Alfred Lotka el 1925). Van passar, doncs, més de 40 anys des del treball de Ross fins a la definició de R0 de MacDonald, i passaran més de 20 anys des del treball de MacDonald fins que, el 1975, Klaus Dietz no el redescobreixi i el defineixi en els termes que ho acabem de fer. Finalment, els treballs de Robert May i Roy Anderson dels anys 80 donen l’empenta definitiva a l’ús de R0 en l’estudi d’epidèmies. Va haver de passar tot aquest temps, malgrat que la condició AN >1 per al creixement inicial d’una epidèmia apareixia literalment a l’article de Kermack & McKendrick de 1927!
L’ús de R0 té l’avantatge que, per a models prou senzills, té una fórmula explícita. A més, pot calcular-se quan, a més de tenir diferents categories d’individus, es considerin variables com l’edat dels individus, el temps que porten infectats, el seu nombre de contactes o la seva mobilitat geogràfica. De fet, una part dels treballs actuals en epidemiologia se centren a calcular R0 per a models que incorporen ingredients més realistes de la transmissió de les infeccions, especialment des de l’aparició de la COVID-19.
Des d’un punt de vista conceptual, la novetat de treballar amb R0 rau en el fet de considerar la dinàmica de les epidèmies en termes de generacions d’infectats. No es posa el focus en l’aparició diària de nous casos (taxa instantània), sinó en la producció per càpita de nous casos al llarg d’un període infecciós (generació): “quants infectats ha produït un infectat mentre ha estat infecciós?”. Si no ens centrem en l’inici del brot epidèmic, llavors parlem del nombre de reproducció efectiu Rt a l’instant t del curs d’una epidèmia. En aquest cas, però, el càlcul de Rt no és directe perquè una part significativa (però desconeguda) de la població ja ha contret la infecció i, per tant, no tots els contactes dels individus infectats es produeixen amb individus susceptibles de contraure la infecció, com se suposa en la definició de R0.
De manera molt gràfica, el matemàtic i epidemiòleg anglès Adam Kucharski explica els factors que intervenen en el nombre de reproducció efectiu amb la següent fórmula (dots vol dir ‘punts’ en anglès):
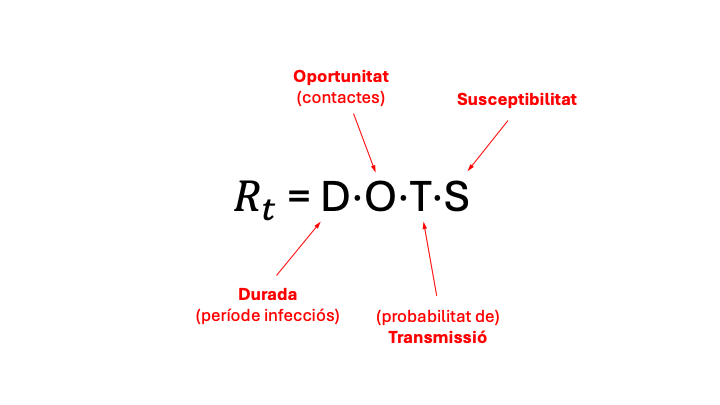
Figura 4. Fórmula del nombre de reproducció efectiu - Imatge adaptada de la que apareix a https://www.youtube.com/watch?v=tdDs13-paDA
Així, per a qualsevol malaltia infecciosa, podem disminuir el valor de Rt escurçant la durada del període infecciós (tractament), disminuint les oportunitats de contagi amb la reducció del nombre de contactes (quarantena, allunyament social, mosquiteres en malalties com la malària), dificultant la transmissió amb mesures profilàctiques (higiene, mascaretes en infeccions respiratòries, preservatius en malalties de transmissió sexual), o disminuint la susceptibilitat de la població amb campanyes de vacunació.
Extincions estocàstiques
Però aquest no és el final de la història. Certament, si s’aconsegueix reduir el valor de Rt per sota d’1 en una o més d’aquestes mesures, l’epidèmia desapareixerà. Ara bé, si Rt >1, encara hi ha una probabilitat no menyspreable que la malaltia s’extingeixi quan el nombre d’infectats sigui molt baix. Aquesta situació es presenta amb l’aparició dels primers casos durant un brot epidèmic i, també, un cop s’ha deixat enrere el pic de la corba epidèmica i la prevalença de la malaltia és molt baixa (Figura 3). És llavors quan, per atzar, les persones infectades poden no transmetre la infecció, bé perquè es recuperen molt ràpid, bé perquè els contactes que han tingut no han estat efectius. Així, doncs, l’epidèmia s’acaba extingint, malgrat tenir capacitat de propagar-se, perquè les poques ocasions que ha tingut per fer-ho no han estat reeixides. És el que es coneix com a extinció estocàstica.
Un dels primers a adonar-se d’aquest fet va ser l’estadístic anglès Maurice S. Bartlett. En la dècada dels anys 50, es va interessar pels models estocàstics d’epidèmies i, com Hamer en el seu moment, pels brots recurrents de xarampió. En l’article “Measles periodicity and community size”, publicat el 1957, Bartlett constata que les extincions (períodes de tres o més setmanes sense notificacions de nous casos) després d’un pic epidèmic eren freqüents en ciutats petites d’Anglaterra i Gal·les, mentre que, en ciutats grans com Manchester o Birmingham, el xarampió mai no desapareixia del tot (entre 1925 i 1950 hi va haver 13 epidèmies de xarampió a Manchester). Arran d’aquestes observacions, Bartlett introdueix el concepte de mida comunitària crítica definint-la com la mida d’una comunitat per a la qual hi ha una probabilitat del 50% que una epidèmia desaparegui després d’assolir el seu pic.
En el cas del xarampió, la mida comunitària crítica estimada és 250.000-400.000 individus. Com que el xarampió confereix immunitat permanent i és molt contagiós (les estimacions del seu R0 van entre 12 i 18), després d’una epidèmia bona part de la població acaba patint la infecció i cal, doncs, una font prou important de nous susceptibles (naixements) per mantenir l’aparició periòdica de brots epidèmics. En poblacions més petites, les extincions estocàstiques són més freqüents i els brots epidèmics, més esporàdics, s’originen a partir de l’arribada de casos provinents d’altres comunitats (casos importats).
Així, doncs, tant des d’una perspectiva determinista com estocàstica, el final d’una epidèmia ve marcat per la falta de transmissions infeccioses. Ara bé, per arribar-hi, no cal que desapareguin tots els individus susceptibles d'una població (o que s’eliminin tots els mosquits d'una regió); n’hi ha prou que el seu nombre sigui prou baix perquè les recuperacions superin els contagis. L'objectiu de les campanyes de vacunació és precisament assolir aquesta situació, que correspon a l'anomenada immunitat de grup.
Referències
- N. Bacaër: A short history of mathematical population dynamics. Springer-Verlag, Londres, 2011.
- M. S. Bartlett: “Measles periodicity and community size”. Journal of the Royal Statistical Society 120 (1957), 48-70.
- W. H. Hamer: The Milroy lectures on epidemic diseases in England: the evidence of variability and of persistency of type. Recull de les tres conferències impartides el 1906 al Royal College of Physicians de Londres. Disponible a: https://wellcomecollection.org/works/cvjetwe5.
- J.A.J. Heesterbeek: “A brief history of R0 and a recipe for its calculation”. Acta Biotheoretica 50 (2002), 189-204.
- M. J. Keeling i B. T. Grenfell: “Disease extinction and community size: Modeling the persistence of measles”. Science 275 (1997), 65-67.
- W. O. Kermack i A. G. McKendrick: “A contribution to the mathematical theory of epidemics”. Proceedings of the Royal Society of Medicine 115A (1927), 700-721.
- A. Kucharshi: The rules of contagion: Why things spread and why they stop. Profile Books, Londres, 2021.
- R. Ross: “Some quantitative studies in epidemiology”. Nature 87 (1911), 466-467.
- D. Quammen: Spillover: Animal infections and the next human pandèmic. Vintage Books, Londres, 2012.
- The Nobel Prize. https://www.nobelprize.org/nomination/archive/show_people.php?id=3615.
NOTA: Foto de capçalera © Joan Saldaña