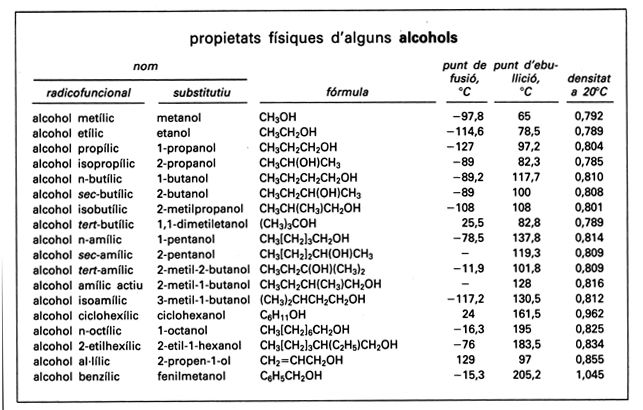
Els alcohols, ROH (que han pres llur nom del més antigament conegut de tots ells, l’alcohol ordinari o etanol), poden considerar-se derivats de l’aigua HOH per substitució d’un hidrogen per un grup alquil R. Segons que el carboni unit a l’hidroxil sigui primari, secundari o terciari, els alcohols són anomenats també primaris, secundaris o terciaris. Si la molècula conté dos, tres o més grups funcionals alcohol, els alcohols s’anomenen, respectivament, diols (o glicols), triols i, en general, poliols.
Segons les regles de la IUPAC, els alcohols es designen afegint al nom de l’hidrocarbur el sufix -ol, tot preservant la n etimològica (ex: metà, metà- n -ol), i indicant la posició de l’hidroxil amb un nombre en prefix. (ex: 2-butanol CH 3 CH 2 CH(OH)CH 3). Això no obstant, si la molècula conté un altre grup, prioritari en nomenclatura, els alcohols es designen amb el prefix hidroxi -. Ex: 4-hidroxipentanal CH 3 CH(OH)CH 2 CH 2 CHO. Els alcohols poden, encara, designar-se, sigui fent seguir el mot alcohol de l’adjectiu corresponent al grup R (ex: alcohol al.lílic CH 2 = CHCH 2 OH), o bé considerant-los com a derivats de substitució del metanol (que abans s’anomenava, en aquest cas, carbinol). Així, l’1,1-dimetiletanol (CH3)3 COH, és anomenat trimetilmetanol (abans, trimetilcarbinol).
Les propietats físiques dels alcohols depenen del grup R. Quan R és petit, són líquids miscibles amb l’aigua o molt solubles, d’olor característica i de sabor ardent i fortament associats (per formació d’enllaços hidrogen), cosa que fa que llurs punts d’ebullició siguin molt més elevats que no els dels tiols corresponents. La solubilitat en aigua disminueix ràpidament quan el pes molecular augmenta. Quan existeixen diversos isòmers de posició, el punt d’ebullició acostuma a ésser tant més baix (i el punt de fusió tant més alt) com més gran és la substitució al veïnatge del grup OH.
Els alcohols no absorbeixen en l’ultraviolat pròxim i el visible, però donen absorcions característiques en l’infraroig. La principal té lloc (en absència d’enllaços hidrogen) a la regió 3.650-3.590 cm-1. Quan hi ha tals enllaços, la banda es desplaça cap a les baixes freqüències. Químicament, els alcohols són substàncies reactives, de caràcter dèbilment amfòter. Per acció de la temperatura, i més fàcilment en presència de catalitzadors, perden aigua i donen olefines. La facilitat de deshidratació creix en passar dels alcohols primaris als terciaris.
L’hidrogen del grup OH té propietats àcides i dona amb certs metalls sals anomenades alcoholats; amb els organomagnèsics aquesta acidesa provoca la formació d’hidrocarburs. Amb els halurs d’hidrogen els alcohols donen derivats halogenats, i amb els àcids carboxílics o llurs clorurs formen èsters. La velocitat i el límit d’esterificació disminueixen en passar dels alcohols primaris als terciaris. Per oxidació o per deshidrogenació catalítica els alcohols primaris donen aldehids, i els secundaris, cetones. Els alcohols terciaris resisteixen certs oxidants, i quan s’oxiden ho fan amb ruptura de la molècula. Com a derivats característics, ben cristal·litzats i de fàcil identificació, els alcohols donen p-nitrobenzoats, 3,5-dinitrobenzoats i feniluretans.
Els alcohols són obtinguts al laboratori per reaccions molt diverses, segons la primera matèria accessible. En alguns casos poden ésser preparats per hidròlisi (d’èsters, d’halurs o sulfats d’alquil, etc.). Més correntment són obtinguts per reducció de compostos carbonílics (aldehids, cetones, àcids carboxílics, anhídrids, èsters o clorurs d’àcid). Aquesta reducció pot ésser feta bé catalíticament, amb hidrogen i níquel o platí (o cromit de coure, quan hom redueix èsters o necessita selectivitat:
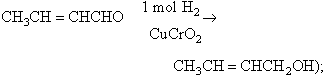
amb hidrurs metàl·lics (hidrur d’alumini i de liti —l’únic reactiu capaç de reduir àcids:
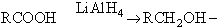
o borohidrur de sodi, que permet d’efectuar reduccions molt selectives:
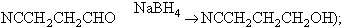
amb alcoholats (reducció de Meerwein-Ponndorf-Verley; amb metalls alcalins i alcohol (reducció de Bouveault i Blanc), etc. A partir d’aldehids poden també obtenir-se alcohols per dismutació (per reacció de Cannizzaro o, a través d’un èster, per reacció de Tiščenko). També hi ha un altre mètode de preparació molt general (que pot donar alcohols primaris, secundaris i terciaris), que és la reacció dels organomagnèsics (o organolítics) amb els aldehids i cetones (i també amb èsters, anhídrids o clorurs d’àcid):
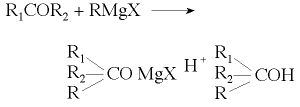
Altres mètodes d’aplicació més restringida són, per exemple, la reacció d’amines primàries amb àcid nitrós, o la reacció d’alquens amb diborà seguida d’oxidació (que permet d’efectuar una hidratació que no segueix la regla de Markovnikov), o, en fi, els procediments molt variats que condueixen a alcohols polifuncionals. Alguns dels mètodes esmentats són utilitzats també industrialment (especialment la reducció catalítica, per exemple, per a obtenir ciclohexanol, i la hidròlisi de clorurs d’alquil, per exemple, per a obtenir alcohols amílics). Això no obstant, la indústria utilitza, a més, procediments específics, tals com la hidratació d’alquens (amb àcid sulfúric en fase líquida o catalíticament en fase vapor), l’oxidació directa d’hidrocarburs saturats (que condueixen a mescles complexes), la síntesi de Fischer-Tropsch i el procediment oxo. Per hidratació d’alquens són obtinguts l’etanol, el 2-propanol, el 2-butanol i l’1,1-dimetiletanol. La reacció obeeix la regla de Markovnikov i, per tant, exceptuant en el cas de l’etilè, no permet d’obtenir alcohols primaris:
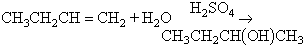
Per oxidació directa s’obté sobretot metanol. La síntesi de Fischer-Tropsch dona sobretot alcohols normals, i el procediment oxo, alcohols en C 4 i superiors. Altres procediments industrials importants són la síntesi del metanol a partir de CO i H2; la síntesi de l’1-butanol, del 2-etil-1-hexanol i del metilisobutilmetanol per condensació aldòlida, i la síntesi d’alcohols primaris de cadena lineal a partir de trialquilaluminis. En fi, els procediments fermentatius continuen essent una font important d’etanol i d’1-butanol. Els alcohols no són gaire abundants a la natura a l’estat lliure i s’hi troben sobretot en forma d’èsters. Això no obstant, l’etanol i alguns dels seus homòlegs superiors es formen en la fermentació dels sucres i nombrosos olis essencials i resines contenen alcohols diversos. Deixant de banda els poliols, els àcids alcohols i els aminoalcohols, els alcohols bioquímicament importants són l’axeroftol o vitamina A, els alcohols grassos i, sobretot, els esterols.
Els alcohols essent molt nombrosos, llurs aplicacions són forçosament molt diverses. Molts d’ells són utilitzats com a dissolvents o troben aplicació directa en nombroses indústries, per exemple, perfumeria, cosmètica, pintures, adhesius, indústria farmacèutica, etc. Llur principal ús és, tanmateix, la síntesi, especialment d’èsters, per a obtenir dissolvents, plastificants, detergents, medicaments, etc.