Pertany al grup IIIB de la taula periòdica i és un dels metalls de la sèrie dels lantànids. Ocorre a la natura, conjuntament amb els altres lantànids, en la monazita, constituint-ne un 3% en pes. La seva separació és efectuada per tècniques de bescanvi iònic i extracció amb dissolvents. El samari natural té un pes atòmic de 150,35 i és una mescla de 7 núclids, tres dels quals (147Sm, 148Sm i 149Sm) són radioactius, amb vides mitjanes molt llargues. Són també coneguts nou radioisòtops artificials de l’element. El metall pot ésser obtingut per reducció de l’òxid Sm2O3 amb bari. Té un llustre argentí i és dur i fràgil i relativament estable en l’aire a temperatura ambient. Pot existir en dues formes al·lotròpiques: α, estable per sota de 917°C, i amb una densitat de 7,52 g/cm3, i β, estable a temperatures superiors i amb densitat de 7,40 g/cm3. Es fon a 1.077°C i bull a 1.791°C. S’encén en l’aire per damunt de 150°C formant l’òxid Sm2O3 i reacciona amb l’aigua alliberant-ne hidrogen 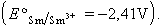
Forma dues sèries de composts, principalment iònics, en els quals actua amb les valències 2 i 3, la darrera de les quals és la més estable. L’ió Sm+3 té un radi de 0,964 A i presenta configuració [Xe] 4f5 i coloració groga. L’ió Sm2+ és fortament reductor 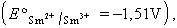 té un radi d’1,11 Å i presenta configuració [Xe] 4f6 i coloració vermella. El samari troba aplicació, en forma elemental, en la preparació d’arcs de carboni per a il·luminació, en el dopatge del fluorur càlcic per a làsers i màsers i en la preparació d’aliatges. En forma combinada, principalment com l’òxid Sm2O3, és emprat en la preparació de vidre òptic com a absorbent de l’infraroig, com a absorbent de neutrons en reactors nuclears i com a catalitzador de deshidratació i deshidrogenació.
té un radi d’1,11 Å i presenta configuració [Xe] 4f6 i coloració vermella. El samari troba aplicació, en forma elemental, en la preparació d’arcs de carboni per a il·luminació, en el dopatge del fluorur càlcic per a làsers i màsers i en la preparació d’aliatges. En forma combinada, principalment com l’òxid Sm2O3, és emprat en la preparació de vidre òptic com a absorbent de l’infraroig, com a absorbent de neutrons en reactors nuclears i com a catalitzador de deshidratació i deshidrogenació.
Propietats físiques del samari
| nombre atòmic | 62 |
| pes atòmic | 150,4 |
| estructura electrònica | [Xe] 4f6 5d0 6s2 |
| estats d’oxidació | +2, +3 |
| densitat | 7,54 g/ml |
| punt de fusió | 1 072ºC |
| punt d’ebullició | 1 778ºC |
| radi iònic (Sm+3) | 0.964 Å |
| potencial d’ionització, en eV | I: 5,63 Å |
| II: 11,07 | |
| consuctivitat tèrmica (a 25ºC) | 0’133 W/cm∙k |
| resistivitat elèctrica (a 20ºC) | 88 μΩ |