Resultats de la cerca
Es mostren 24 resultats
N
Química
Símbol que, en el nom de certs compostos, serveix per a indicar que un substituent d’una molècula (anomenat immediatament després del símbol) resta unit a un àtom de nitrogen d’aquesta, com per exemple en el cas de la N, N-dimetil formamida.
Hom acostuma a posar aquest símbol en cursiva
substància pura
Química
Cadascuna de les classes de matèria homogènia, de composició química definida, per contraposició a mescla
.
Les substàncies pures no poden ésser resoltes en d’altres de més simples per mètodes físics Hom acostuma a classificar les substàncies pures en simples element i compostes compost
elèctrode d’hidrogen
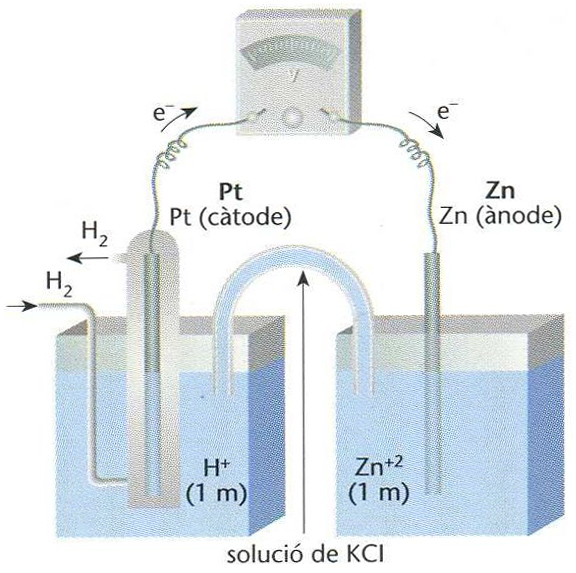
Elèctrode d’hidrogen que actua com a càtode en una cel·lula electroquímica
© Fototeca.cat
Química
Elèctrode de platí entorn del qual bombolleja hidrogen.
Hom acostuma a prendre com a potencial zero el d’un elèctrode d’hidrogen, a la pressió atmosfèrica, en una solució d’ions hidrogen d’activitat unitat És emprat com a elèctrode de referència
anhídrid
Química
Òxid que forma un oxoàcid en combinar-se amb l’aigua.
La denominació d’anhídrid no és admesa en les normes de nomenclatura inorgànica de la IUPAC S'acostumà d’utilitzar-la per a designar especialment òxids de no-metalls, i solament en casos rars òxids metàllics
èter de petroli
Química
Mescla d’hidrocarburs saturats de 5 a 7 àtoms de carboni, procedents de les fraccions volàtils de la destil·lació del petroli.
Hom acostuma a indicar-hi l’interval del punt d’ebullició de la mescla en qüestió per exemple, èter de petroli 40-60°C La fracció d’èters de petroli d’alt punt d’ebullició 90-120°C és anomenada ligroïna Tots aquests èters de petroli són molt emprats com a dissolvents apolars Malgat el nom, no tenen la funció èter
potencial d’elèctrode
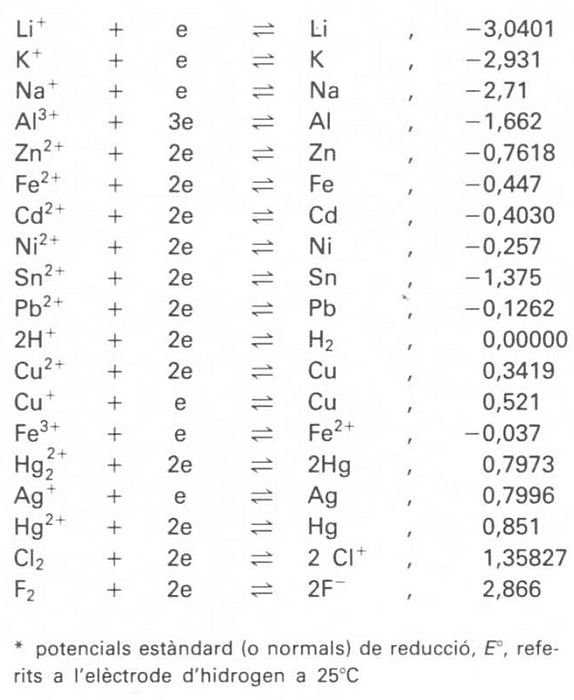
Potencial d’elèctrode
©
Química
Estat d’equilibri elèctric d’una substància (element químic o compost) que és submergida en una dissolució que la conté en forma iònica.
Formalment, és expressat per la equació o llei de Nernst El potencial d’elèctrode d’una substància no pot ésser mesurat d’una manera absoluta, sinó formant una pila amb una altra que és presa com a referència de potencial zero Hom acostuma a prendre com a referència l' elèctrode d'hidrogen o l' elèctrode de calomelans
degradació
Química
Descomposició que ocorre en etapes amb productes intermediaris ben definits.
Sovint, però, hom acostuma a definir específicament la degradació com una reacció de disminució del nombre d’àtoms de carboni d’un compost orgànic, normalment alifàtic, com és ara la reacció de Hofmann o la de Curtius generalment es produeix per oxidació de l’àtom de carboni terminal, segons l’equació R-CH 2 -CH 3 →R-CH 2 -COOH →R-CH 3 +CO 2
reactiu
Química
En una reacció química, qualsevol de les substàncies que hi participen estequiomètricament per originar uns productes.
Però en un sentit més restringit i per contraposició a substrat, hom acostuma a denominar reactiu l’agent que provoca un determinat canvi sobre la substància que hom desitja transformar En aquest darrer sentit, un mateix reactiu pot actuar de manera semblant enfront d’una gran varietat de substrats que pertanyen a la mateixa categoria química Així, per exemple, el diazometà CH 2 N 2 és un reactiu metilant d’àcids, fenols, alcohols i enols
terpè
Química
Denominació genèrica dels hidrocarburs de fórmula general (C5H8)n, que ocorren en la majoria d’olis essencials i d’oleoresines i que poden ésser considerats com a oligòmers o polímers de l’isoprè.
Poden ésser de cadena oberta o cíclics i, en aquest darrer cas, poden cobrir una gran varietat d’estructures Hom acostuma a classificar-los en hemiterpens C 5 H 8 , monoterpens C 1 0H 1 6, sesquiterpens C 1 5H 2 4, diterpens C 2 0H 3 2, triterpens C 3 0H 4 8, tetraterpens C 4 0H 6 4 i politerpens C 5 H 8 n , en els quals el valor de n és gran
concentració
Química
Quantitat d’una substància en una unitat de mescla, solució o mineral que la conté.
Correntment hom acostuma a expressar la concentració d’una manera general i, en el cas d’una solució, relacionant el solut en pes o en volum i cent parts en pes o en volum de la solució tant per cent en pes o en volum, relacionant el nombre de mols o el d’equivalents de solut i un litre de la solució molaritat i normalitat, respectivament, relacionant el nombre de mols de solut i un quilogram del solvent molalitat o bé relacionant el nombre de mols d’un component de la solució i el nombre total de mols dels components fracció molar