Resultats de la cerca
Es mostren 18 resultats
molar
Química
Dit d’aquella dissolució la concentració de la qual és expressada en termes de molaritat.
fracció molar
Química
Fracció de mols d’un determinat component d’una mescla o dissolució sòlida, líquida o gasosa que és continguda en 1 mol de la mescla o dissolució.
potencial químic
Química
Per a cada constituent d’una mescla, derivada del potencial termodinàmic respecte al nombre de partícules del constituent considerat.
També és anomenat energia lliure molar parcial
coeficient osmòtic
Física
Química
Coeficient introduït per Bjerrum, que inclou tots els factors que expressen la desviació del comportament d’una solució respecte del comportament ideal.
D’aquesta forma, per un component i d’una barreja, el potencial químic s’expressa per μ i =μ o i + g i RT ln x i on g i és el coeficient osmòtic i x i és la fracció molar del solut en la dissolució
llei de Raoult
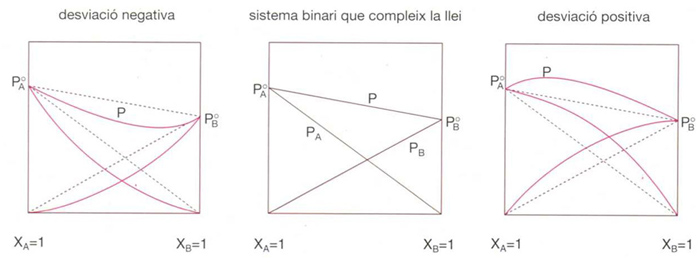
Llei de Raoult
Química
Relació descoberta per F. M. Raoult l’any 1887 en estudiar la pressió de vapor de solucions salines.
Estableix que el descens relatiu de la pressió de vapor d’un líquid pur i en dissoldre-hi una substància no volàtil s , és proporcional a la fracció molar d’aquesta p i o - p i /p i o = x s = 1- x i La llei de Raoult pot ésser també aplicada a mescles líquides binàries i d’ordre superior amb la següent formulació la pressió de vapor parcial del component i p i és igual a la pressió de vapor del líquid i p i o pur a la mateixa temperatura multiplicada per la seva fracció molar en la mescla p i = p i o x i Molt poques solucions compleixen la llei de Raoult en…
equació del virial
Química
La més general de les equacions d’estat per a gasos.
Introduïda per HKOnnes l’any 1901, consisteix en el desenvolupament de l’anomenat factor de compressibilitat pv / R θ en sèrie de potències de 1/ v v volum molar essent R la constant de gasos, θ la temperatura del gas ideal del sistema a la temperatura del qual el gas exerceix la pressió p i B , C unes funcions de la temperatura conegudes com a segon, tercer, etc, coeficients del virial
paracor
Química
Constant pròpia dels líquids, introduïda per S.Sugden el 1924.
És definida per la relació p = Mγ1/4ρ-ρ0- , on M és el pes molecular del líquid en particular, γ és la tensió superficial i ρ i ρ0 són les densitats del líquid i del seu vapor a una temperatura determinada Per a líquids no associats, es manté constant dins un marge ample de temperatures i dóna una mesura del seu volum molar És una propietat additiva i ha estat emprada històricament en l’estudi de l’estructura molecular dels composts
concentració
Química
Quantitat d’una substància en una unitat de mescla, solució o mineral que la conté.
Correntment hom acostuma a expressar la concentració d’una manera general i, en el cas d’una solució, relacionant el solut en pes o en volum i cent parts en pes o en volum de la solució tant per cent en pes o en volum, relacionant el nombre de mols o el d’equivalents de solut i un litre de la solució molaritat i normalitat, respectivament, relacionant el nombre de mols de solut i un quilogram del solvent molalitat o bé relacionant el nombre de mols d’un component de la solució i el nombre total de mols dels components fracció molar
fugacitat
Física
Química
Funció termodinàmica que substitueix la pressió parcial en les equacions que tracten de descriure el comportament dels gasos reals.
Si G 1 i G 2 són les energies lliures normals d’un gas a dues pressions p 1 i p 2 , les fugacitats f 1 i f 2 del gas a aquestes pressions són definides de forma que es compleixi l’equació G 2 — G 1 = nRT ln f 2 / f 1 Comparant aquesta equació amb l’equació dels gasos ideals G 2 — G 1 = nRT ln p 2 / p 1 , hom veu que, per al comportament ideal, la fugacitat és proporcional a la pressió contràriament, per al comportament no ideal la fugacitat no coincideix amb la pressió corresponent La fugacitat pot ésser determinada per l’equació RT ln f/p = v — RT /p dp , on v = V/ n és el volum …
coeficient d’activitat
Química
Quantitat γ per la qual cal multiplicar les pressions gasoses o les concentracions per a obtenir les activitats.
Amb les convencions usuals respecte als estats de referència, γ = a/P en el cas dels gasos i γ = a/c en el cas de les solucions Segons que la concentració sigui expressada en fracció molar, molalitat o molaritat, el valor numèric de γ varia L’interès dels coeficients d’activitat resideix en el fet que varien molt més lentament que les activitats i es presten millor, per tant, a les interpolacions i extrapolacions En el cas dels electròlits forts, com que és impossible calcular les activitats individuals dels ions, hom introdueix un coeficient d’activitat mitjà γ ± , deduïble de…