Resultats de la cerca
Es mostren 164 resultats
pressió parcial
Química
En una mescla de fluids, pressió que exerceix cadascun dels components.
En una mescla de gasos perfectes, cada component exerceix la pressió que li correspondria si ocupés ell sol el volum que el conté
pressió osmòtica
Física
Química
Diferència de pressions que hi ha entre un costat i l’altre d’una membrana semipermeable (osmosi) que separa dues dissolucions de concentracions diferents quan el sistema és en equilibri.
L’expressió formal de la pressió osmòtica és l’anomenada fórmula de Van't Hoff
petroli

Esquema d’un jaciment típic de petroli i del procediment d’extracció per aire a pressió
© Fototeca.cat
Química
Oli mineral constituït per hidrocarburs de composició diversa i en proporcions molt variables segons el jaciment d’origen.
Hom els classifica en petrolis de base parafínica, naftènica, aromàtica o mixta, segons els tipus d’hidrocarburs que hi predominen Així, els petrolis americans són freqüentment de base parafínica els de Bakú, de base naftènica els de Borneo, de base aromàtica, etc Hi ha diverses teories que intenten explicar l’origen del petroli la més comunament acceptada és la d’Engler-Hofer, la qual suposa que una gran quantitat de matèria orgànica algues, diatomees, plàncton, etc s’acumulà en el fons d’algunes mars, on, en absència d’oxigen, es formà una massa albuminoidea que, primerament per acció…
fugacitat
Física
Química
Funció termodinàmica que substitueix la pressió parcial en les equacions que tracten de descriure el comportament dels gasos reals.
Si G 1 i G 2 són les energies lliures normals d’un gas a dues pressions p 1 i p 2 , les fugacitats f 1 i f 2 del gas a aquestes pressions són definides de forma que es compleixi l’equació G 2 — G 1 = nRT ln f 2 / f 1 Comparant aquesta equació amb l’equació dels gasos ideals G 2 — G 1 = nRT ln p 2 / p 1 , hom veu que, per al comportament ideal, la fugacitat és proporcional a la pressió contràriament, per al comportament no ideal la fugacitat no coincideix amb la pressió corresponent La fugacitat pot ésser determinada per l’equació RT ln f/p = v — RT /p dp , on v =…
llei de Raoult
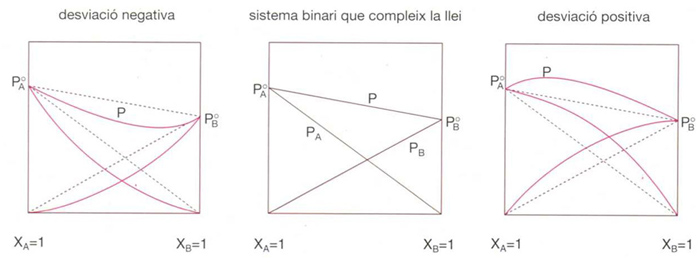
Llei de Raoult
Química
Relació descoberta per F. M. Raoult l’any 1887 en estudiar la pressió de vapor de solucions salines.
Estableix que el descens relatiu de la pressió de vapor d’un líquid pur i en dissoldre-hi una substància no volàtil s , és proporcional a la fracció molar d’aquesta p i o - p i /p i o = x s = 1- x i La llei de Raoult pot ésser també aplicada a mescles líquides binàries i d’ordre superior amb la següent formulació la pressió de vapor parcial del component i p i és igual a la pressió de vapor del líquid i p i o pur a la mateixa temperatura multiplicada per la seva fracció molar en la mescla p i = p i o x i Molt poques solucions compleixen la llei…
destil·lació

Destil·lació fraccionada amb columna de plats
© Fototeca.cat
Química
Operació de separació, total o parcial, dels constituents d’una mescla líquida segons llur diferent pressió de vapor.
Hom basa la destillació en el fet que el vapor en equilibri amb el líquid és, en general, més ric en el constituent més volàtil És una operació molt corrent i important, tant al laboratori com a la indústria, que consisteix a vaporitzar parcialment la mescla en general fent-la bullir i condensar els vapors, recollint el condensat separadament del residu Hom pot fer la condensació directament, evitant qualsevol retrogradació destillació simple , o bé després d’haver obtingut per condensació parcial dels vapors, és a dir, per rectificació, llur progressiu enriquiment en el constituent més…
polietilè
Química
Matèria plàstica termoplàstica obtinguda per polimerització de l’etilè a alta pressió (que pot arribar a unes 1 500 atm) o bé a baixa pressió (entre 10 i 40 atm).
En ambdós casos la polimerització té lloc en presència d’un catalitzador, que en el primer cas és l’oxigen, en molt poca proporció, i en el segon és el catalitzador de Ziegler producte de la reacció del trietilalumini amb el tetraclorur de titani o el catalitzador de Phillips òxid de crom Segons que sigui obtingut a alta o a baixa pressió el polietilè és de baixa o alta densitat, respectivament Hom obté dos tipus de polietilè de densitats intermèdies, bé per la copolimerització de l’etilè amb altres composts, bé per la mescla de polietilens de baixa i alta densitat El polietilè,…
explosió BLEVE
Química
Explosió de tipus mecànic d’un líquid o d’un gas liquat sobreescalfats produïda per una baixada sobtada de la pressió del recipient que la conté.
El sobreescalfament esdevé quan la temperatura del líquid supera la del seu punt d’ebullició sense que s’arribi a formar vapor Aquesta condició es pot donar quan un agent extern fa augmentar la temperatura del recipient afeblint la seva resistència i provocant-ne el trencament, per l’existència d’alguna fissura que produeixi una baixada de pressió en el contingut, i també per escalfament moderat d’un recipient sobrecarregat Qualsevol d’aquestes situacions pot provocar una fuita sobtada del contingut, que canvia massivament a l’estat vapor i produeix una expansió explosiva que…
reforming
Química
Procediment de refinació que permet d’obtenir benzines d’elevats índexs d’octà a partir de benzines pesants, sotmetent-les a l’acció simultània de la pressió i de la temperatura, eventualment en presència de catalitzadors, per tal de modificar-ne la composició per dissociació de llurs molècules.
El reforming fou començat a efectuar cap a l’any 1930, en augmentar la necessitat de carburants d’elevat poder antidetonant, en les installacions de craqueig tèrmic, però posteriorment hom construí installacions especials per a aquest procés, amb forns de tubs d’acer, en les quals la reacció és controlada de manera que el producte sigui refredat bruscament, mitjançant la injecció d’un refrigerant adequat, després d’haver estat el temps necessari en una secció terminal del forn Les principals modificacions que s’esdevenen en l’estructura dels hidrocarburs són, igual que en el…
Paginació
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- …
- Pàgina següent
- Última pàgina