Resultats de la cerca
Es mostren 17 resultats
regles de Woodward i Hoffmann
Química
Cos de teoria elaborat per R. B. Woodward i R. Hoffmann l’any 1965, per a predir la possibilitat de realització, tèrmicament o fotoquímicament, d’una reacció mitjançant un mecanisme concertat, atenent a la conservació de la simetria orbital tot al llarg del procés.
Parteix de la teoria simple d’orbitals moleculars, la qual té en compte únicament el signe de la fase dels orbitals moleculars Les reaccions concertades ocorren amb facilitat quan existeix congruència entre les característiques de simetria dels orbitals dels reactius i les dels productes En un sentit general, pel que fa a les reaccions pericícliques tèrmiques, les regles de Woodward i Hoffmann estableixen que aquestes reaccions són permeses per la simetria, en l’estat fonamental, quan el nombre total de components suprafacials en els quals els dos nous enllaços es…
quiralitat
Química
Propietat de no-identitat d’una molècula, en una configuració o conformació donades, amb la seva imatge especular.
Aquest concepte, que deriva del grec χείρ ‘mà’ i que fa referència a la manca de simetria present en les mans, ha substituït modernament el de dissimetria En termes de la quiralitat, hom classifica les molècules en quirals i aquirals Totes les molècules quirals presenten activitat òptica, de manera que ambdós conceptes es troben biunívocament relacionats D’altra banda, la quiralitat d’un agregat de molècules pot diferir de la de les molècules components, com és el cas dels cristalls quirals de quars, els quals són constituïts per unitats essencialment aquirals El concepte de quiralitat,…
orbital molecular
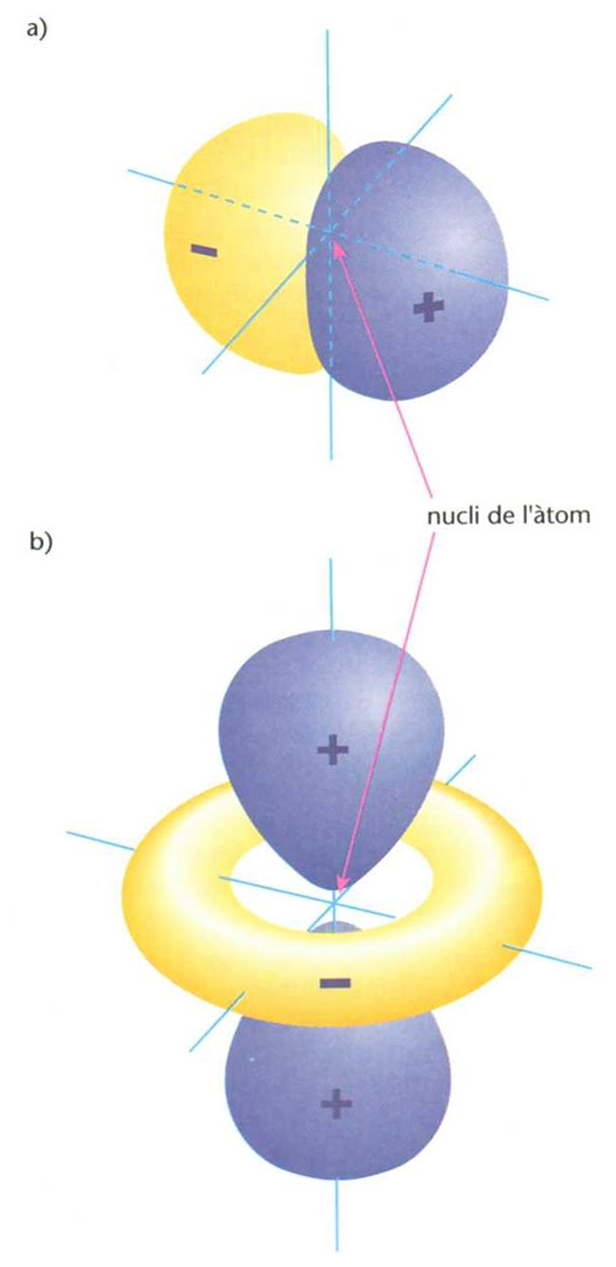
Representació tridimensional de dos orbitals (de nombres quàntics n=2,l = 1 (p) i m=1(a), i n =3,l = 2 (d) i m = 0 (b)) de l’àtom d’hidrogen en prèsencia de camp magnètic extern: assenyalen dos estats energètics de l’electró i la regió al voltant del nucli on és més probable de trobar l’electró en cadascun d’aquests dos estats (els valors de l i m determinen les dimensions, la forma i l’orentació de l’orbital): els caolors respresenten els signes + o - que pren la funció d’ona
© Fototeca.cat
Química
Cadascuna de les funcions d’ona, solució de l’equació de Schrödinger, associades a un electró que forma part d’una molècula.
Presenten les mateixes característiques matemàtiques que els orbitals atòmics Són de natura policèntrica i constitueixen en ells mateixos una interpretació de l’enllaç químic La descripció de l’estructura molecular mitjançant l’ús d’orbitals moleculars és coneguda com a teoria de l’enllaç dels orbitals moleculars , i consisteix a considerar inicialment la molècula com un conjunt de nuclis amb ordenació pròpia, determinar els diversos orbitals de nuclis i omplir els orbitals multicèntrics així obtinguts amb els electrons de la molècula, mitjançant un procediment anàleg al seguit per a establir…
Roald Hoffmann
Química
Químic polonès naturalitzat nord-americà.
Professor de la Cornell University de Nova York, compartí el premi Nobel de química del 1981 amb K Fukui , pels seus treballs basats en la teoria de les pertorbacions als orbitals moleculars, i pel desenvolupament de l’anàlisi de la simetria dels orbitals moleculars que regulen el curs de les reaccions químiques regles de Woodward i Hoffmann
mini
Pintura
Mineralogia i petrografia
Química
Substància pulverulenta, de pes específic 9 i d’un color que va del taronja al vermell segons les dimensions de les partícules.
El mini natural no presenta una simetria definida En la indústria hom l’obté per escalfament de plom al voltant dels 500°C primerament es forma litargiri PbO, el qual, per posterior oxidació, es transforma en mini És insoluble en aigua i molt resistent als àcids minerals Antigament el mini fou molt emprat com a colorant per a tintes i pintures actualment hom l’utilitza en la fabricació de vidre de plom, en la preparació d’esmalts i vernissos sobretot pel seu poder cobrent i per la seva resistència a l’oxidació, com a fundent, etc
anisotropia magnètica
Química
Fenomen de la variació de la susceptibilitat magnètica amb la direcció que presenten moltes substàncies cristal·lines.
En les substàncies magnèticament anisòtropes hi ha només tres direccions ortogonals, anomenades eixos principals d’imantació, per les quals la direcció del moment magnètic induït coincideix amb la direcció del camp Aquests eixos no són forçosament eixos de simetria del cristall ni eixos òptics L’anisotropia magnètica és molt marcada en el grafit, en certs anions oxigenats, com ara els ions carbonat i nitrat, i en els composts orgànics aromàtics En aquests darrers, és una propietat de la molècula, i la susceptibilitat perpendicular al pla del nucli aromàtic és algunes vegades…
enllaç de retrodonació
Química
Model teòric per a la interpretació de l’enllaç entre àtoms metàl·lics pesants de transició i molècules neutres, com ara el monòxid de carboni o una olefina.
En el cas d’una unió de tipus sigma σ entre el metall i la molècula, els orbitals n-1 d del metall tenen energies similars a les dels orbitals ns i np de la capa de valència i, per tant, poden participar en la formació d’enllaços Així, l’enllaç resultant pot considerar-se com a suma d’un enllaç sigma σ, originat per donació d’un parell electrònic no compartit del lligand a un orbital d buit i de simetria adient del metall, i d’una cessió de càrrega d’un orbital d ocupat del metall a un orbital antienllaçant π* desocupat del lligand neutre En el cas d’una unió de tipus pi π,…
orbital pi
Química
Tipus d’orbital molecular caracteritzat pel fet de posseir simetria binària respecte a l’eix d’enllaç.
orbital sigma
Química
Tipus d’orbital molecular caracteritzat pel fet de posseir simetria cilíndrica respecte a l’eix d’enllaç.
polaritzabilitat
Química
Tendència a deformar-se un ió, perdent la simetria esfèrica de l’ió lliure, a conseqüència d’atraccions o repulsions electroestàtiques que experimenta el núvol electrònic.
És important sobretot per als anions i augmenta amb llur volum i càrrega regles de Fajans