Resultats de la cerca
Es mostren 79 resultats
radi de van der Waals
Química
Pel que fa als cristalls moleculars d’elements no metàl·lics o de llurs composts covalents, valor definit per a cada element com la meitat de la distància d’equilibri entre els dos àtoms més pròxims d’aquest no enllaçats entre ells.
Els radis de van der Waals són una conseqüència de les forces intermoleculars d’atracció i repulsió forces de van der Waals i hom els pot considerar com una mesura de la distància mínima a la qual poden apropar-se dos àtoms sense establir un enllaç covalent La determinació experimental d’aquests radis és realitzada mitjançant la difracció de raigs X, i llur valor presenta una oscillació de ±0,05 Å, segons el compost en el qual han estat determinats Els valors numèrics dels radis de van der Waals s’aproximen als dels corresponents radis iònics dels mateixos elements, atès que…
electronegativitat
Química
Capacitat que té un àtom per a atreure’s els electrons de l’enllaç covalent que forma amb un altre àtom, és a dir, tendència que presenta un àtom a compartir desigualment els electrons de l’orbital o els orbitals del seu enllaç.
Hom ha convingut d’acceptar com a valor de l’electronegativitat d’un element el valor que aquest agafa en combinar-se amb l’hidrogen L’escala d’electronegativitats fou calculada per primera vegada per Linus Pauling a partir dels moments dipolars, electroafinitats i potencials d’ionització, bo i donant com a valor patró 4,0 per al fluor L’electronegativitat és emprada en fórmules empíriques per a calcular el caràcter iònic d’un enllaç i també per a calcular de manera aproximada la longitud d’enllaç a partir de la longitud dels radis covalents
pK
Química
En els àcids i les bases, operador definit per l’expressió pK = -logK, essent K la constant d’equilibri de la reacció d’un àcid (pKa) o una base (pKb) amb un solvent amfipròtic.
El pK és una mesura de la força dels àcids i de les bases i és relacionat amb la variació d’energia lliure ∆G de la reacció amb el solvent, d’acord amb l’equació En medi aquós, hom pot relacionar el pK b d’una base amb el pK a del seu àcid conjugat mitjançant el valor del producte iònic de l’aigua K w , segons pK a + pK b = pK w , a qualsevol temperatura En aquestes condicions, un valor petit de pK a indica un àcid fort o una base feble acidesa
pH-metre
Química
Potenciòmetre dotat d’elèctrodes adequats i convenientment disposat per a mesurar el pH d’una dissolució.
N'hi ha de dues menes els potenciomètrics i els de lectura directa Els primers consisteixen essencialment en un potenciòmetre amb amplificació electrònica del corrent no compensat En aquests cada lectura requereix una compensació manual, que hom aconsegueix contraposant una força electromotriu variable, la qual dóna el valor del pH mesurat Els de lectura directa posseeixen un circuit adequat per a obtenir una desviació de l’agulla del galvanòmetre proporcional al pH o una expressió digital del seu valor Els pH-metres de tipus potenciomètric ofereixen una gran…
ordre de reacció
Química
Nombre real definit formalment com la suma dels exponents dels termes de concentració que intervenen en l’expressió diferencial de la velocitat d’una reacció i que té el sentit del nombre mínim d’espècies que semblen reaccionar simultàniament d’acord amb l’equació cinètica que regeix el procés.
L’ordre de reacció és una dada experimental que cal distingir de la molecularitat de la mateixa reacció, malgrat que sovint prenen el mateix valor La determinació de l’ordre de reacció és duta a terme per mètodes numèrics a partir de dades cinètiques els mètodes més emprats són classificats, d’acord amb el tipus d’equació de velocitat que empren, en diferencials i integrals El coneixement de l’ordre de reacció dóna informació sobre el mecanisme de reacció i, en particular, de les espècies que intervenen en el pas limitador de la velocitat Els ordres més comuns són els de …
agregat
Química
Material constituït per la mescla o juxtaposició macroscòpica de dos o més components, que difereixen per llur forma o composició, i que són essencialment insolubles l’un en l’altre.
Els agregats poden ésser de cinc tipus estratificats , formats de components laminars agregats de partícules eventualment amb un medi continu intercalar agregats de fibres eventualment amb un medi continu intercalar agregats de flocs eventualment amb un medi continu intercalar i agregats amb esquelet , formats per un medi continu, amb cavitats regularment distribuïdes, que omple un segon material El comportament i les propietats dels agregats depenen de la forma i disposició estructural dels components, de llur natura i de llurs interaccions Segons els casos s’obté una suma de propietats…
polarímetre
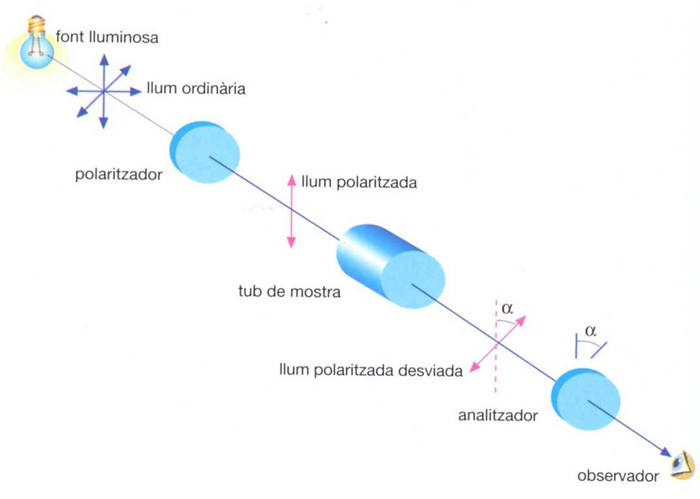
Esquema bàsic d’un polarímetre
© Fototeca.cat
Física
Química
Instrument per a mesurar la rotació del pla de vibració de la llum polaritzada en travessar un medi òpticament actiu.
Consta fonamentalment d’una font lluminosa que emet radiació monocromàtica, generalment una làmpada de vapor de sodi, un polaritzador, constituït per un prisma de Nicol o un polaroide, el qual transforma la llum ordinària en polaritzada, un tub situat en la direcció de propagació de la radiació, el qual conté la mostra, i un analitzador, constituït generalment per un altre prisma de Nicol El funcionament d’un polarímetre simple és el següent quan el tub per a la mostra és buit, es transmet un màxim de llum a través de l’analitzador quan aquest és alineat amb el polaritzador En collocar en el…
coeficient d’activitat
Química
Quantitat γ per la qual cal multiplicar les pressions gasoses o les concentracions per a obtenir les activitats.
Amb les convencions usuals respecte als estats de referència, γ = a/P en el cas dels gasos i γ = a/c en el cas de les solucions Segons que la concentració sigui expressada en fracció molar, molalitat o molaritat, el valor numèric de γ varia L’interès dels coeficients d’activitat resideix en el fet que varien molt més lentament que les activitats i es presten millor, per tant, a les interpolacions i extrapolacions En el cas dels electròlits forts, com que és impossible calcular les activitats individuals dels ions, hom introdueix un coeficient d’activitat mitjà γ ± , deduïble de…
temps de semireacció
Química
En una reacció química, temps necessari perquè la concentració d’un substrat inicial es redueixi a la meitat.
El seu valor pot ésser deduït, coneguda l’equació cinètica d’un procés en particular, a partir de l’expressió de la constant de velocitat
punt d’anilina
Química
Temperatura a la qual una gasolina és miscible amb un volum igual d’anilina.
És un valor indicatiu del contingut aproximat de la gasolina en hidrocarburs aromàtics com més alt és el punt d’anilina, menor és la proporció d’aromàtics
Paginació
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- Pàgina següent
- Última pàgina