Resultats de la cerca
Es mostren 65 resultats
fase
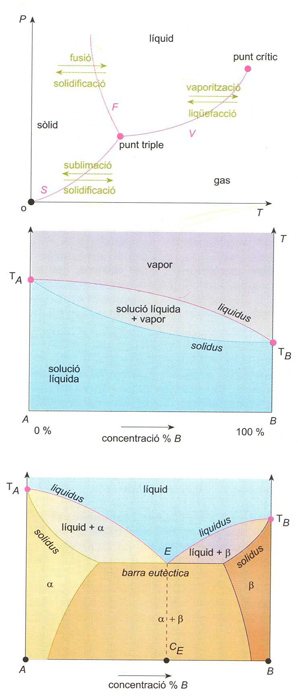
Diagrama de fases: (a) d’un sistema d’un sol component (F, corba de fusió; S, corba de sublimació; V, corba de vaporització); (b) d’un sistema binari líquid-vapor ( TA i TB . punts d’ebullició d' A i B ); (c) d’un sistema binari solid-líquid eutèctic ( TA i TB . punts de fusió d' A i B ); E punt eutèctic; CE, composició eutèctica: α i β són les dues fases sòlides que es presenten
© Fototeca.cat
Física
Química
Part d’un sistema, formada per un nombre qualsevol de components, homogènia i amb uns límits ben determinats que la separen de les altres parts del sistema i de la resta de l’univers.
La noció de fase generalitza la d’estat físic sòlid, líquid, gasós i permet distincions més subtils, com la que hi ha entre dues formes de cristallització d’un sòlid Els components d’un sistema són les substàncies que l’integren, i els constituents són les diferents fases que el formen Si només hi ha una fase, el sistema és homogeni, i si n'hi ha més, heterogeni El pas de la fase sòlida a la líquida és anomenat fusió , el de la líquida a la gasosa, vaporització , i el de la sòlida a la gasosa, sublimació Aquests canvis de fase són progressius, i els canvis en sentit contrari són anomenats…
sistema de referència
Física
Conjunt d’un sistema de coordenades espacials i un rellotge, amb els quals un observador pot caracteritzar cada esdeveniment per les seves coordenades (x, y, z) i per l’instant t en què succeeix.
És anomenat també referencial En la física clàssica, dominada per la transformació de Galileu entre referenecials, no té gaire importància la consideració del rellotge en el sistema de referència en canvi, en té en la física relativista, a causa de les fórmules de transformació de Lorentz
energia de deformació
Física
Energia que cal cedir a un cos perquè es deformi.
Si el material és elàstic, l’energia resta acumulada en forma d’energia mecànica en el material, la qual és recuperada en desaparèixer la deformació L’energia de deformació solament depèn dels estats inicial i final del material i no de la forma en què ha estat aconseguida la deformació Si el material no és elàstic, l’energia és consumida en el canvi d’estructura
disponibilitat
Física
Funció termodinàmica introduïda per J.W. Gibbs el 1873 amb el nom d’ energia disponible
i reconsiderada per J.H. Keenan (1941).
Siguin E, S i V l’energia, l’entropia i el volum, respectivament, emprats per a definir els diferents estats d’un sistema B i P o i T o la pressió i la temperatura del medi M amb què és en contacte després d’un canvi reversible en què és assolit l’equilibri termodinàmic amb el medi M, la disponibilitat o energia disponible és
invariància CPT
Física
Principi segons el qual la descripció física d’un fenomen no resulta alterada si es realitza una combinació de les operacions de canvi de càrrega, paritat i temps.
En alguns casos, com la desintegració de mesons K neutres, s’ha observat alguna lleu violació d’aquest principi Hom considera que la violació de la invariància CPT implicaria a la vegada un trencament de la simetria de Lorentz S’ha demostrat que la violació de la invariància CPT postulada en la desintegració dels mesons K o kaons neutres no es produeix, ja que tan sols és una violació CP També s’ha proposat una possible violació de la invariància per part de neutrins i antineutrins, però no s’ha pogut demostrar
fórmules de Fresnel
Física
Fórmules que relacionen les amplituds reflectida (A´´) i refractada (A´) amb l’amplitud incident (A) del camp elèctric d’una ona lluminosa que incideix sobre un dielèctric isòtrop.
En el cas que el vector del camp elèctric sigui parallel al pla d’incidència, les fórmules són i essent l’angle d’incidència i r l’angle de refracció, i en el cas que el vector sigui perpendicular són En el cas que tingui una direcció qualsevol, per descomposició del vector aquest cas és reduït als anteriors Les fórmules de Fresnel permeten també d’estudiar el canvi de fase entre les ones incident, reflectida i refractada
calorimetria
Física
Branca de la física experimental que tracta de la mesura de l’energia en forma de calor que es transfereix en canvis físics o químics.
La calor pot ésser mesurada quantitativament calorímetre observant els efectes que produeix, els més importants dels quals són l’elevació de la temperatura d’una substància en fornir-hi calor el canvi de fase d’una substància, com, per exemple, de sòlid a líquid, de líquid a gas, etc i la transformació de l’energia química, elèctrica o mecànica en calor, o viceversa Són objectes de la calorimetria les mesures de la calor de combustió, la calor de reacció, la capacitat calorífica, la calor específica i les calors de transformació
deriva
Física
Variació lenta i contínua, generalment incontrolable, que es produeix al llarg del temps en el valor d’una magnitud física o en les propietats d’un circuit elèctric o electrònic.
En electrònica, és deguda sovint a un efecte de canvi de certes propietats, sobretot la resistivitat, dels semiconductors, motiu pel qual el corrent varia amb la temperaturaEn els transistors provoca un desplaçament del punt de treball, la qual cosa introdueix sempre una certa distorsió en el senyal de sortida aquest efecte és particularment enutjós en els amplificadors de corrent continu, perquè pot donar lloc a un corrent continu de sortida en absència de senyal d’entrada La deriva és també perjudicial en els amplificadors operacionals, perquè fa desplaçar el zero com a punt de…
Takaaki Kajita

Takaaki Kajita
© Asahi Shimbun
Física
Físic japonès.
Es graduà a la Universitat de Saitama 1981 i més tard féu el doctorat a la de Tòquio 1986 El 1988 s'incorporà a l'Institut de Recerca dels Raigs Còsmics, on és professor des del 1999 és director del Centre per a l'Estudi dels Neutrins Còsmics d'aquest mateix Institut El 1998 detectà a l'observatori Super-Kamiokande l'oscillació de neutrins associada al canvi d'aromes a partir de la collisió de raigs còsmics a l'atmosfera terrestre, cosa que el portà a concloure l'existència de massa en aquestes partícules Per aquesta descoberta rebé el premi Nobel de física el 2015, que…
vaporització
Física
Pas de l’estat líquid a l’estat gasós.
Semblantment a la fusió, en augmentar per temperatura l’energia cinètica de les molècules que formen una substància o per descompressió la distància entre elles es produeix el canvi d’agregació de la matèria que fa passar de l’estat líquid al gasós Segons les condicions en què té lloc la vaporització d’un líquid aquesta s’anomena evaporació o ebullició en el primer cas es manifesta en la superfície del líquid a qualsevol temperatura, i en el segon en tota la massa i a temperatura constant tensió de vapor Hom anomena calor de vaporització la calor necessària per a convertir en gas…