Resultats de la cerca
Es mostren 156 resultats
gasós | gasosa
teoria cinètica dels gasos
Física
Teoria sobre la conformació dels gasos.
Considera que són formats per partícules diminutes molècules, independents, perfectament elàstiques, dotades de moviment continuat i que xoquen entre elles i amb les parets del recinte que les conté A cadascuna d’aquestes hom pot aplicar les lleis de la mecànica clàssica i obtenir, així, expressions macroscòpiques que permeten de determinar la pressió, l’energia interna i les calors específiques dels gasos
aire
Física
Química
Mescla de gasos que forma l’atmosfera terrestre.
A les capes baixes de l’atmosfera, l’aire perfectament sec té, a 0°C i a 760 mm de pressió, amb variacions mínimes, la següent composició en volum nitrogen 78,084%, oxigen 20,946%, argó 0,934%, diòxid de carboni 0,033%, altres gasos rars 0,002% Durant molts segles l’aire fou considerat un element Les primeres proves que era una substància complexa foren donades per John Mayow 1674 La presència de petites quantitats de diòxid de carboni fou establerta per Joseph Black 1755 Pel que fa a la natura de l’aire, Lavoisier demostrà 1774 que és format per nitrogen i oxigen La primera determinació…
vaporització
Física
Pas de l’estat líquid a l’estat gasós.
Semblantment a la fusió, en augmentar per temperatura l’energia cinètica de les molècules que formen una substància o per descompressió la distància entre elles es produeix el canvi d’agregació de la matèria que fa passar de l’estat líquid al gasós Segons les condicions en què té lloc la vaporització d’un líquid aquesta s’anomena evaporació o ebullició en el primer cas es manifesta en la superfície del líquid a qualsevol temperatura, i en el segon en tota la massa i a temperatura constant tensió de vapor Hom anomena calor de vaporització la calor necessària per a convertir en gas…
efusió
Física
Química
Procés pel qual els gasos sotmesos a pressió passen a través de forats petits.
La llei que expressa les velocitats d’efusió de dos gasos en funció de llurs densitats és V 1 /V 2 =
recuperador
Física
Aparell o instal·lació que permet la recuperació d’una part de la calor dels gasos de combustió d’un fogar abans que es perdin en l’atmosfera.
Algunes vegades els gasos de combustió, generalment molt abundants i molt calents, passen per un recuperador, abans d’ésser conduïts a la xemeneia, i en ésser-hi refredats permeten d’escalfar l’aigua d’alimentació o l’aire comburent Unes altres vegades, els gasos passen per economitzadors economitzador per tal de fornir del vapor necessari la mateixa fàbrica on és situat el forn Hi ha recuperadors anomenats d’inversió , que permeten d’escalfar el gas combustible i l’aire de combustió amb els gasos que surten dels fogars dels forns industrials importants forns alts, de les fàbriques de gas,…
analitzador d’Orsat
Física
Absorciòmetre portàtil que permet de determinar el percentatge de diòxid de carboni, oxigen i òxid de carboni que conté una mostra de gasos de combustió.
La mesura és basada en les variacions de volums produïdes per absorcions selectives dels diferents gasos, mitjançant reactius apropiats En forma més evolucionada permet també l’anàlisi d’hidrocarburs no saturats, d’hidrogen i de metà
manòmetre
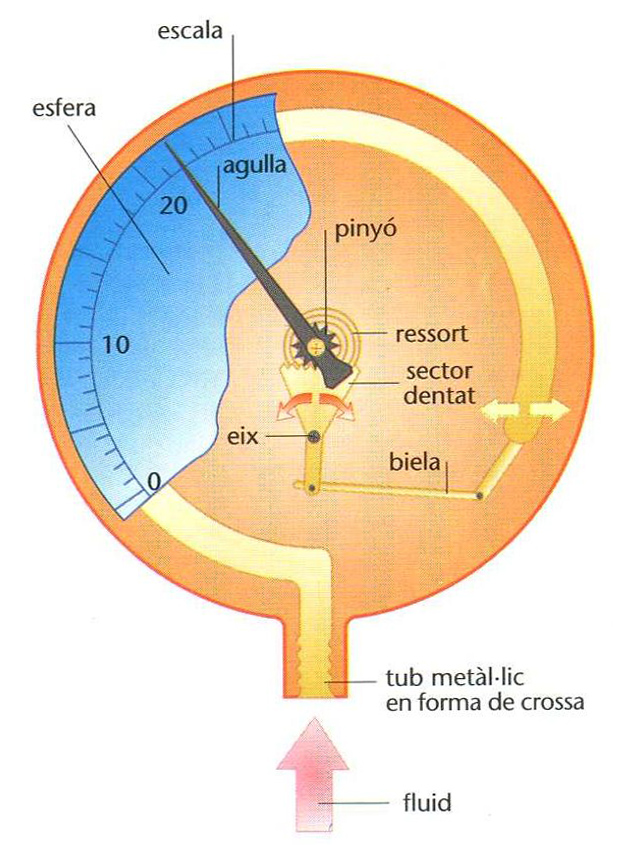
Manòmetre metàl·lic
© Fototeca.cat
Física
Instrument utilitzat per a mesurar la pressió dels fluids, especialment dels gasos.
Els més primaris es basen en la igualtat de pressions que hi ha en els diversos punts d’un mateix pla horitzontal d’un fluid en equilibri manòmetres de columna i tenen una bona precisió, per la qual cosa tots els manòmetres d’ús científic són d’aquest tipus Per a mesurar pressions molt altes hom pot fer muntatges en sèrie de manòmetres de columna, tot fraccionant la pressió a mesurar, o bé pot utilitzar manòmetres-balança com els de Stückrath o de Stanton , els quals mesuren forces exercides sobre èmbols de secció coneguda Uns altres manòmetres, com el de Lissell , es basen en la variació…
llei d’Avogadro
Física
Llei enunciada per Amedeo Avogadro el 1811 en forma d’hipòtesi i actualment experimentada a partir de la llei de Gay-Lussac dels volums de combinació entre gasos, segons la qual volums iguals de gasos diferents, a igual pressió i temperatura, contenen el mateix nombre de molècules.
Si per a un gas determinat hom defineix un volum-tipus volum molar tal que, a 0°C i 760 mm de Hg de pressió pesi en grams el valor donat pel seu pes molecular molècula gram , el nombre de molècules que es troben en aquest volum és igual al nombre d’Avogadro, qualsevol que sigui el gas Generalitzant, hom pot afirmar que una molècula gram de qualsevol substància, en estat sòlid, líquid o gasós, conté un nombre de molècules igual al nombre d’Avogadro
escalfador
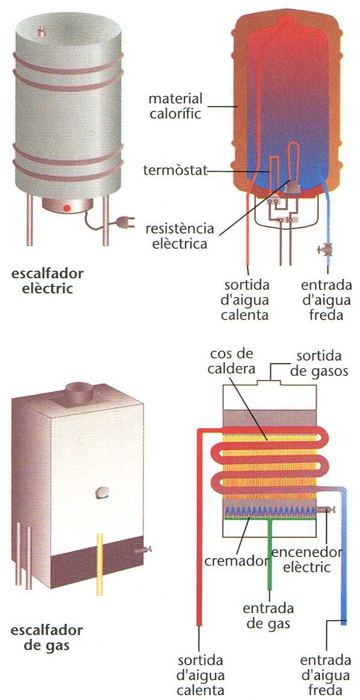
Escalfadors domèstics: elèctric (a dalt), de gas (a baix)
© Fototeca.cat
Física
Aparell emprat per a escalfar aigua o un altre fluid per mitjà d’energia elèctrica o d’un combustible, generalment gasós o líquid.
Els escalfadors elèctrics consisteixen en un recipient, que conté el fluid, voltat d’unes resistències elèctriques i proveït d’un aïllament per tal d’evitar pèrdues de calor En els escalfadors per combustió el fluid circula per un serpentí escalfat pels gasos produïts en la combustió Sovint van proveïts d’una vàlvula que obre el pas del combustible quan hom fa circular el fluid pel serpentí, la qual es tanca automàticament en cessar la circulació
Paginació
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- …
- Pàgina següent
- Última pàgina