Resultats de la cerca
Es mostren 10 resultats
regla de Hund
Física
Regla segons la qual tots els orbitals d’un mateix nivell energètic han d’ésser ocupats per un electró abans que un d’ells pugui ésser ocupat per un doblet electrònic.
variància
Física
En un sistema termodinàmic, nombre màxim de variables termodinàmiques intensives (pressió, temperatura, etc) independents.
La variància depèn del nombre de components i de fases del sistema, i és calculada mitjançant la regla de les fases fase 3
resultant
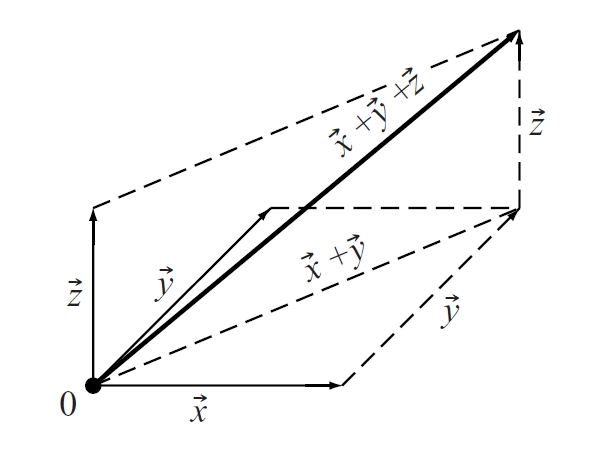
Resultant d’una suma de vectors
Física
Vector equivalent a la suma de dos vectors.
Donats dos vectors, hom n'obté la resultant per la regla del parallelogram cal construir un parallelogram que tingui per costats els vectors donats, i la resultant és aleshores la diagonal d’aquest parallelogram
funció de Gibbs
Física
Funció termodinàmica G definida per l’equació G = U-TS+pV = H-TS (U essent-hi l’energia interna, T la temperatura absoluta, S l’entropia, p la pressió, V el volum i H l’entalpia).
Anomenada també entalpia lliure , és una funció d’estat del sistema considerat Una propietat important és que, per a un sistema en equilibri, la funció de Gibbs específica té el mateix valor per a les fases líquida i gasosa Una conseqüència d’aquesta propietat és la regla de les fases o de Gibbs fase
Josiah Willard Gibbs
Física
Matemàtiques
Fisicoquímic i matemàtic nord-americà.
Estudià a les universitats de París, Heidelberg i Berlín, i el 1871 fou nomenat professor de física matemàtica a Yale Els seus estudis versaren sobre termodinàmica química aplicació de la primera llei de la termodinàmica i de la segona en l’estudi de l’equilibri de substàncies heterogènies Establí les bases teòriques de la fisicoquímica i descobrí, juntament amb Helmholtz, l’equació que porta llur nom, com també la regla de les fases
punt triple
Física
Punt del diagrama de fases dels sistemes d’un sol component que representa l’estat del sistema en què coexisteixen les tres fases.
D’acord amb la regla de les fases fase 3, l’estat representat pel punt triple és invariant, i, per tant, per a cada sistema hi ha una pressió i una temperatura, anomenades triples Per al sistema aigua sòlida-líquida-vapor és P t = 4,6 torr i T t = 0,007°C Quan un sistema presenta polimorfisme a l’estat sòlid, es poden presentar punts triples entre dues fases sòlides i la líquida o entre dues fases sòlides i la fase vapor o, també, entre tres fases sòlides
George Gamow
Física
Físic soviètic, naturalitzat nord-americà l’any 1939.
Estudià a les universitats de Leningrad, de Göttingen, de Copenhaguen i de Cambridge i fou deixeble de Bohr i de Rutherford Fou professor de física teòrica a la Universitat de Leningrad i, des del 1934, a la Universitat George Washington EUA Entre els seus treballs més importants es destaquen l’elaboració d’un model de nucli atòmic, anomenat del fluid nuclear , i l’enunciat de la regla de Gamow-Teller Ha estudiat les reaccions termonuclears que tenen lloc a l’interior dels estels, ha elaborat una teoria neutrínica de les supernovae i ha construït un model, dit de les capes, per…
David Brewster
Física
Físic escocès.
Professor de física a Edimburg, s’interessà especialment per l’òptica Els seus principals treballs tracten de l’absorció de la llum, de l’òptica metàllica i de la polarització Estudià la difracció de la llum 1799 i formulà la regla sobre la polarització total de la llum reflectida llei de Brewster Inventà un polarímetre i fou el primer a emprar el sodi com a productor de llum monocromàtica Determinà l’anomenat punt de Brewster, un dels tres punts del vertical que passa pel Sol, per als quals la radiació celeste difosa té polarització nulla i que roman entre 15° i 20° per sota…
fase
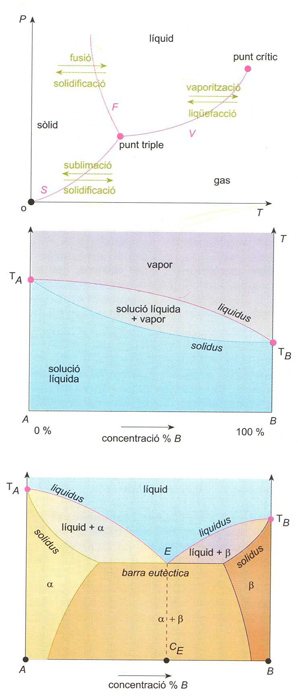
Diagrama de fases: (a) d’un sistema d’un sol component (F, corba de fusió; S, corba de sublimació; V, corba de vaporització); (b) d’un sistema binari líquid-vapor (TA i TB. punts d’ebullició d’A i B); (c) d’un sistema binari solid-líquid eutèctic (TA i TB. punts de fusió d’A i B); E punt eutèctic; CE, composició eutèctica: α i β són les dues fases sòlides que es presenten
© Fototeca.cat
Física
Química
Part d’un sistema, formada per un nombre qualsevol de components, homogènia i amb uns límits ben determinats que la separen de les altres parts del sistema i de la resta de l’univers.
La noció de fase generalitza la d’estat físic sòlid, líquid, gasós i permet distincions més subtils, com la que hi ha entre dues formes de cristallització d’un sòlid Els components d’un sistema són les substàncies que l’integren, i els constituents són les diferents fases que el formen Si només hi ha una fase, el sistema és homogeni , i si n’hi ha més, heterogeni El pas de la fase sòlida a la líquida és anomenat fusió , el de la líquida a la gasosa, vaporització , i el de la sòlida a la gasosa, sublimació Aquests canvis de fase són progressius , i els canvis en sentit contrari són anomenats…
moment magnètic
Física
Donada una espira per la qual circula un corrent d’intensitat I, vector μ definit per la fórmula μ = I s, on s és un vector perpendicular al pla de l’espira, de sentit donat per la regla del tirabuixó i de mòdul igual a la superfície de l’espira.
És anomenat també moment dipolar magnètic Mitjançant el càlcul integral hom generalitza el concepte de moment magnètic per a qualsevol tipus d’espira, sigui o no plana, per a un solenoide μ = NI s , essent N el nombre d’espires i per a un cos sotmès a l’acció d’un camp magnètic imantació D’altra banda, hom també associa un moment magnètic a les òrbites tancades que poden seguir les càrregues elèctriques en vol, com poden ésser les dels electrons atòmics en els models de Rutherford i Bohr