Resultats de la cerca
Es mostren 39 resultats
àtom de Bohr
Física
Model atòmic proposat per N.H.D. Bohr el 1913 per a descriure l’àtom d’hidrogen.
Recolza sobre les hipòtesis següents l’àtom només pot existir en uns certs estats estacionaris, caracteritzats pel fet que el seu electró només pot ocupar unes òrbites o nivells energètics ben definides, que, tot i ésser governades per la mecànica clàssica, són determinades per la condició que el moment angular orbital de l’electró sigui un múltiple enter de la constant de Planck reduïda L = nh , essent h = h/ 2π l’emissió i absorció d’energia per l’àtom no es realitza de forma contínua , com demanaria l’electrodinàmica clàssica en explicar el moviment circular dissipatiu d’un electró, sinó…
efecte de Bohr
Biologia
Fenomen pel qual l’equilibri de dissociació de l’oxihemoglobina en hemoglobina i oxigen es desplaça cap a la formació d’hemoglobina quan augmenta la pressió parcial de diòxid de carboni.
Així, en els teixits anòxics amb un contingut baix d’oxigen i alt de diòxid de carboni es produeix una ràpida conversió de l’oxihemoglobina en hemoglobina a causa no solament de la baixa pressió d’oxigen, sinó també de l’efecte de Bohr Anàlogament, la disminució del pH sanguini produeix el mateix efecte gràcies a l’estreta correlació entre la concentració de diòxid de carboni i el pH
magnetó de Bohr
Física
Unitat de moment magnètic intrínsec de l’electró.
És definit per μ Β = ħ | e | |/ 2 m e c , essent ħ la constant de Planck dividida per 2π, | e | el valor absolut de la càrrega elèctrica de l’electró, m e la massa en repòs de l’electró i c la velocitat de la llum El seu valor és 0,578 837 85 95 × 10 -14 MeV G -1 o bé 9,274078 36 × 10 -24 J T -1 El moment magnètic intrínsec de l’electró és μ = -g e μ Β S / ħ, essent g e el factor giromagnètic de l’electró i S el spin en conseqüència, en un estat de spin ħ / 2, el moment magnètic de l’electró és - g e / 2 en unitats de magnetó de Bohr
radi de Bohr
Física
Radi de l’òrbita de l’estat fonamental (n=1) de l’àtom d’hidrogen (àtom de Bohr).
El seu valor és a o = ħ 2 / m e e 2 =0,529 177 Å
teoria de Bohr-Wheeler
Física
Model de la gota líquida per a l’esbrinament de l’estructura del nucli atòmic (fissió).
àtom
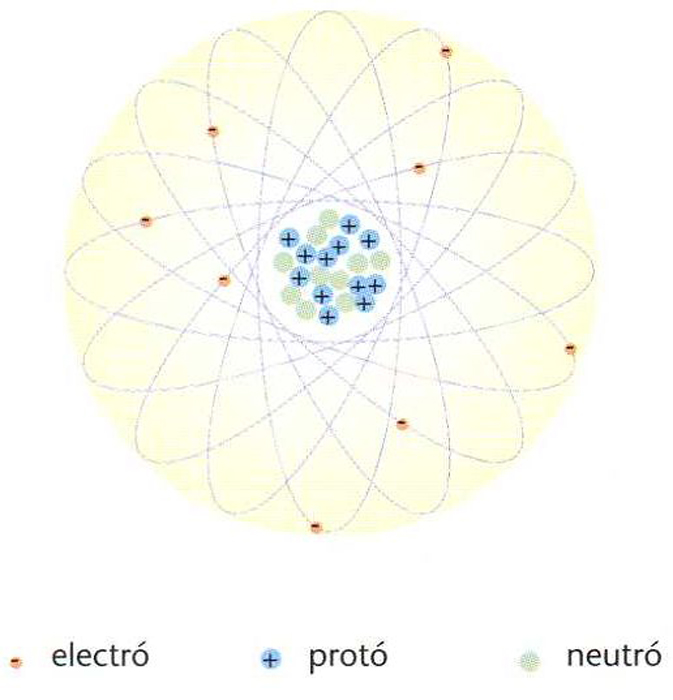
Model d’àtom de Bohr-Rutherford
© Fototeca.cat
Física
Sistema format per un determinat nombre de partícules elementals (essencialment protons, neutrons i electrons) que, essent elèctricament neutre, posseeix intrínsecament les característiques d’un element químic i n’és la quantitat més petita que pot intervenir en una combinació química.
Bàsicament un àtom consta de dues parts D’una banda el nucli , format per protons i neutrons, que conté gairebé tota la massa de l’àtom ~99,9% però que només n’ocupa una part infíma ~10 - 5 vegades les seves dimensions Els electrons, d’altra banda, envolten el nucli formant capes a diferents nivells i, a conseqüència de llur càrrega elèctrica negativa, neutralitzen la càrrega positiva del nucli Les masses dels àtoms van dels 10 - 2 7 kg als 10 - 2 5 kg, i llurs dimensions dels 10 - 1 0 m als 10 - 9 m Els àtoms d’un mateix element tenen el mateix nombre de protons i electrons nombre atòmic, Z…
sèrie de Pfund
Física
Conjunt de ratlles infraroges que apareixen en l’espectre atòmic de l’hidrogen quan l’electró de l’àtom excitat cau a l’òrbita de nombre quàntic principal n=5.
La longitud d’ona λde cadascuna d’aquestes ratlles, segons la teoria atòmica de Bohr àtom de Bohr , és donada, en Å, per l’equació λ = 22794X N 2 / N 2 -25, essent N un nombre enter més gran que 5
sèrie de Paschen
Física
Conjunt de ratlles infraroges que apareixen en l’espectre atòmic de l’hidrogen quan l’electró de l’àtom excitat cau a l’òrbita de nombre quàntic principal n=3.
La longitud d’ona λ de cadascuna d’aquestes ratlles, segons la teoria atòmica de Bohr àtom de Bohr , és donada, en Å, per l’equació λ = 8205,9 N 2 | N 2 -9, essent N un nombre enter més gran que 3
sèrie de Lyman
Física
Conjunt de ratlles ultraviolades que apareixen en l’espectre atòmic de l’hidrogen quan l’electró de l’àtom excitat cau a l’òrbita de nombre quàntic principal n = 1.
La longitud d’ona λ de cadascuna d’aquestes ratlles, segons la teoria atòmica de Bohr àtom de Bohr , és donada, en Å, per l’equació λ = 911,8 N 2 / N 2 - 1, essent N un nombre enter més gran que 1
nucli
Física
Part de l’àtom en la qual es concentra gairebé tota la seva massa (99,9%) i tota la càrrega elèctrica positiva.
El nucli atòmic és format per protons i neutrons nucleons, units entre ells per les forces nuclears interacció forta Segons la proporció de protons i neutrons, el nucli pot ésser estable o inestable en aquest darrer cas es desintegra radioactivitat, modifica la seva constitució i es converteix en un altre de característiques diferents A la natura hi ha 274 tipus de nuclis núclids que són estables, i hom en coneix més de 1 500 d’inestables La història del nucli és més moderna que la de l’àtom, car la seva existència ha estat intuïda i descoberta més recentment Durant el s XIX les…