Resultats de la cerca
Es mostren 441 resultats
àcid fitínic
Bioquímica
Èster hexafosfòric de l’inositol.
Ocorre abundantment en els teixits de sosteniment dels vegetals, especialment dels cereals En els intestins, l’àcid fitínic ingerit dóna lloc a la fitina, que és molt insoluble a pH superior a 3, amb la consegüent disminució de l’absorció dels ions Ca + + i Mg + + per la mucosa intestinal Aquest efecte d’anticalcificació és inhibit per la vitamina D
àcid peroxodisulfúric
Química
Peroxoàcid mineral sòlid cristal·lí que es fon amb descomposició a 65°C.
Hom l’obté per oxidació anòdica de l’àcid sulfúric amb elèctrodes de platí, per sota de 30°C És un oxidant molt enèrgic, segons la semiequació S 2 O 8 2 - +2e →2SO 4 2 - , E °=2,01 V Es descompon lentament i dóna àcid sulfúric i àcid peroxomonosulfúric És emprat en anàlisi química per a identificar ions metàllics
Low Energy Antiproton Ring
Desaccelerador de partícules per a produir antiprotons del CERN de Ginebra.
Construït el 1982 i operatiu fins el 1996, produïa antiprotons amb una energia de 21 MeV i permeté estudiar més a fons les propietats de l’antimatèria i Fou transformat en l’anell d’ions de baixa energia Low Energy Ion Ring, el qual, al seu torn, contribuí a la construcció del Gran Collisionador d’Hadrons, inaugurat el 2007
Johannes Nicolaus Brønsted
Física
Fisicoquímic danès.
Professor de química de la Universitat de Copenhaguen i director de l’institut fisicoquímic d’aquesta universitat Es distingí per treballs de recerca sobre catàlisi, propietats dels ions, cinètica química i, sobretot, juntament amb Thomas Martin Lowry, en l’enunciat de la teoria àcid-base , que porta llur nom àcid de Brønsted-Lowry , base de Brønsted-Lowry
lawrenci
Química
Element radioactiu, de nombre atòmic 103.
Fou obtingut el 1961 per A Ghiorso i els seus collaboradors del Lawrence Radiation Laboratory de Berkeley Califòrnia, per bombardeig del californi amb ions de bor accelerats, segons l’equació 250-252 98 Cf + 10-11 5 B → 257 103 Lr + x 1 0 n Tots els isòtops del lawrenci són radioactius el seu isòtop més estable conegut és el 262
protoporfirina
Bioquímica
La més abundant de totes les porfirines, formada per una molècula de porfina substituïda per 4 grups metil, 2 grups vinil i 2 grups d’àcid propiònic.
N'hi ha 15 isòmers possibles, el més abundant dels quals és la protoporfirina IX Es troba a l’hemoglobina, a la mioglobina i a la majoria de citocroms Forma quelats amb ions metàllics ferro, magnesi, zinc, níquel, cobalt i coure El complex amb ferro II és anomenat protohem o simplement hem, i el format amb ferroIII, hemina o hematina
dipeptidasa
Bioquímica
Nom usual del grup d’enzims anomenats dipeptidohidrolases, que hidrolitzen específicament l’enllaç peptídic dels dipèptids.
Contenen ions metàllics divalents en la molècula CO 2 + , Mn 2 + o Zn 2 + o bé els necessiten per a èsser actives Les dipeptidases que intervenen en la digestió dels dipèptids en els mamífers són a la mucosa intestinal Moltes són específiques per a un dipèptid, com la glicil-leucinadipeptidasa També han estat trobades dipeptidases en les plantes i en els microorganismes
carrall
Odontologia
Substància groguenca, de natura calcària, dura i molt adherent, que s’acumula a la cara interna de les dents.
És un irritant responsable de l’inici de malalties gingivals gingivitis El carrall —anomenat també tosca dentària o niell — és format per cristalls de calci placa dental impregnada d’ions de calci i fosfats dipositats sobre una estructura reticular d’hidroxilapatita i per substància orgànica representada per bacteris filamentosos i cèllules epitelials descamades És causat bàsicament per una manca d’higiene dental
acidesa
Química
Indicació quantitativa de les propietats àcides.
L’acidesa d’un àcid HA en un solvent amfipròtic S, o sigui, la seva força en aquest solvent, ve mesurada per la seva tendència a cedir un protó al solvent, és a dir, per la constant d’acidesa K A expressió on a i és l’activitat de l’espècie i i K és la constant de l’equilibri HA + S ⇌ HS + + A - La força d’un àcid depèn, doncs, del solvent En general, resulta còmode d’expressar l’acidesa en unitats logarítmiques, i per obtenir nombres positius hom pren el logaritme de la inversa de K A , que és representat pel símbol pK A pK A = - log K A Com més elevada és l’acidesa, és a dir, com més…
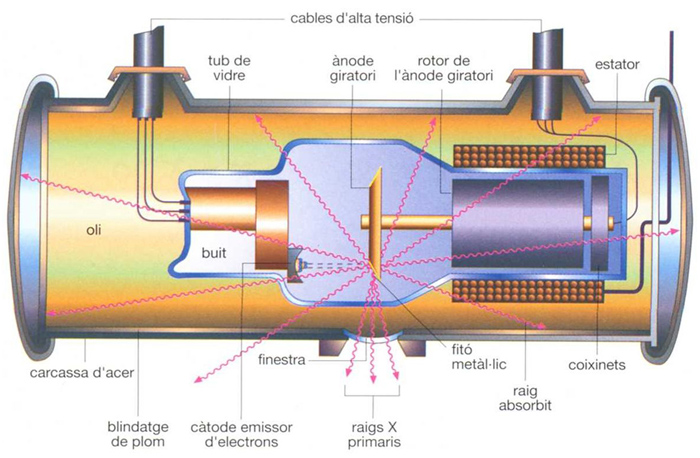
raigs X
fototeca.cat
©
Física
Radiació electromagnètica de freqüència superior a la visible emesa per un àtom en produir-se el salt d’un electró d’una òrbita externa a una d’interna, pel fet d’haver perdut aquesta un electró per efecte d’una excitació exterior o d’una absorció per part del nucli (captura K).
En l’espectre de les ones electromagnètiques els raigs X es troben en la franja de longituds d’ona compresa entre 100 Å i 10 -6 Å El nom de raigs X els fou donat per WC Röntgen el 1895, en descobrir-los i desconèixer-ne la natura Correntment hom els obté per impacte sobre un fitó metàllic de platí o tungstè d’electrons accelerats mitjançant una diferència de potencial d’uns quants milers de volts això té lloc a l’interior d’un tub de vidre tancat on ha estat fet un buit elevat Hi ha dos tipus de tubs productors de raigs X els de càtode fred i els de càtode calent Els primers són tubs de raigs…
Paginació
- Primera pàgina
- Pàgina anterior
- …
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- …
- Pàgina següent
- Última pàgina