Resultats de la cerca
Es mostren 34 resultats
entalpia
Física
Química
Magnitud termodinàmica, funció d’estat del sistema físic considerat.
Per definició H = U + pV , H essent l’entalpia, U, l’energia interna, p , la pressió, i V , el volum El primer principi de la termodinàmica, en funció de l’entalpia, adopta la forma dQ = dH - Vdp , és a dir, la quantitat de calor fornida a un sistema és emprada per a augmentar-ne l’entalpia i fer un treball extern - Vdp En un procés a pressió constant per exemple, en un recipient obert en què actua sempre la pressió atmosfèrica, les variacions d’entalpia mesuren la quantitat de calor que hi intervé En una transformació a temperatura i…
equació de Kirchhoff
Física
Equació que relaciona la variació d’entalpia amb la temperatura a pressió constant.
S'expressa per i permet de calcular la variació d’entalpia H d’una reacció a la temperatura T 2 , tot coneixent la variació de l’entalpia de la reacció a una certa temperatura T 1 i les capacitats calorífiques dels productes i dels reactius a T 1 i T 2
coeficient de Joule-Thomson
Física
Coeficient que expressa la variació de la temperatura d’un gas quan, en condicions adiabàtiques (entalpia constant), és sotmès a un procés d’expansió.
És donat per on P, V, T són la pressió, el volum i la temperatura, H l’entalpia i C p la calor específica a pressió constant La temperatura a la qual μ J T =0, a una pressió determinada, és anomenada temperatura d’inversió
funció de Gibbs
Física
Funció termodinàmica G definida per l’equació G = U-TS+pV = H-TS (U essent-hi l’energia interna, T la temperatura absoluta, S l’entropia, p la pressió, V el volum i H l’entalpia).
Anomenada també entalpia lliure , és una funció d’estat del sistema considerat Una propietat important és que, per a un sistema en equilibri, la funció de Gibbs específica té el mateix valor per a les fases líquida i gasosa Una conseqüència d’aquesta propietat és la regla de les fases o de Gibbs fase
diagrama de Mollier
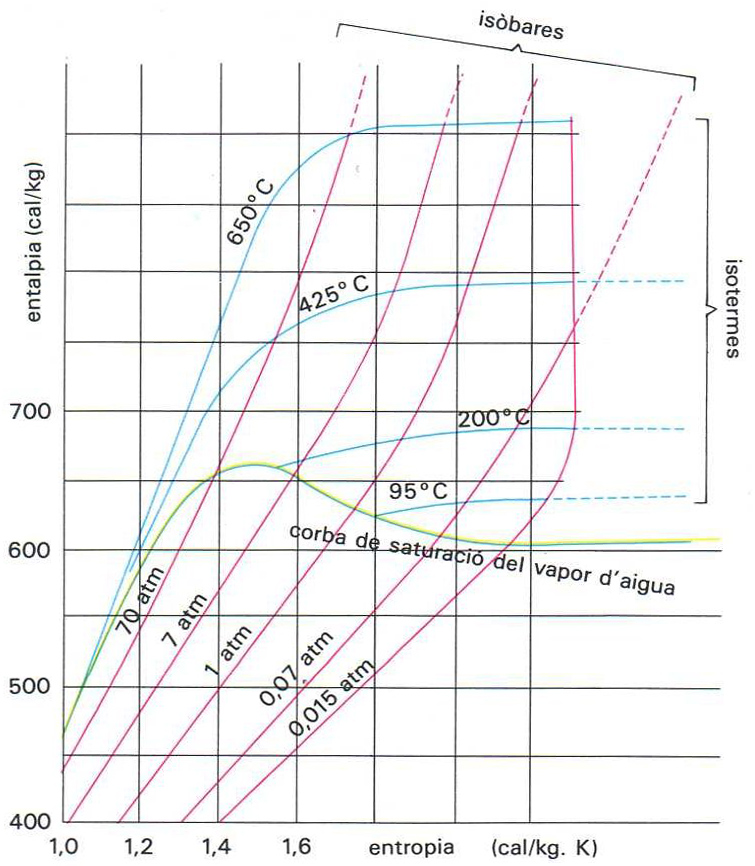
Diagrama de Moñlier del vapaor d’aigua
© Fototeca.cat
Física
Diagrama que té per objecte de posar de manifest les propietats energètiques del vapor d’aigua (o d’un altre fluid) i, concretament, mostrar la relació general entre la pressió, la temperatura, l’entalpia i l’entropia del dit vapor.
És anomenat també diagrama entàlpic El diagrama consisteix en un sistema de coordenades cartesianes, amb l’entropia a l’eix d’abscisses i l’entalpia al d’ordenades, sobre el qual hom representa les famílies de corbes isòbares i isotermes El diagrama és dividit per una corba de saturació en dues zones la zona de vapor saturat , que és situada a la part inferior de la corba, i la de vapor sobreescalfat , situada a la part superior El diagrama de Mollier té considerables aplicacions industrials així, els valors que hom necessita per a calcular numèricament el treball o el rendiment…
calor de reacció
Química
Energia tèrmica alliberada o absorbida en qualsevol procés químic.
Quan aquest és dut a terme a pressió constant, l’esmentada energia coincideix amb la que en termodinàmica rep el nom d' entalpia , i quan ho és a volum constant, amb l’anomenada energia interna Segons la natura del procés, la calor de reacció té expressions pròpies Així, la calor de formació d’un compost és l’increment d’entalpia que tindrà lloc quan un mol d’aquest és format teòricament a partir dels seus elements considerats en l’estat tipus, a una pressió i una temperatura determinades la calor de combustió , quan és cremat completament un mol, a una temperatura…
termodinàmica química
Física
Química
Branca de la termodinàmica dedicada a l’estudi general de les relacions entre l’energia i els processos químics que forneix una base teòrica per a la racionalització dels diversos capítols de la química on són presos en consideració els bescanvis d’energia.
Comprèn la termoquímica, en l’estudi de la qual hom fa ús de les funcions termodinàmiques, energia interna i entalpia l'estàtica química, on entren en joc les funcions derivades del segon principi de la termodinàmica, principalment l’entropia i l’entalpia lliure de Gibbs i una part important de l'electroquímica, que és sistematitzada emprant aquesta darrera funció, equivalent al treball útil que hom pot obtenir d’una reacció química, a pressió i temperatura constants Aquestes funcions termodinàmiques es relacionen amb les equacions d’estat dels sistemes materials,…
equació de Van’t Hoff
Química
Equació que determina la variació de la constant d’equilibri químic K en funció de la temperatura.
Segons l’expressió ∂ln K /∂ T p = Δ H 0 / RT 2 , Δ H 0 essent la variació d’entalpia en la reacció en condicions normals, R la constant dels gasos i T la temperatura absoluta
explosòfor
Militar
Química
Agrupació atòmica molt inestable que per descomposició o reordenació allibera una gran quantitat de calor.
Hom distingeix els grups de formació endotèrmica, que en descompondre's alliberen una quantitat de calor igual a llur entalpia de formació com és ara el grup azida, -N=N≡N, que es descompon produint nitrogen, dels grups de formació exotèrmica, en els quals la calor generada és deguda a reaccions entre els elements del grup