Resultats de la cerca
Es mostren 14 resultats
gasificació
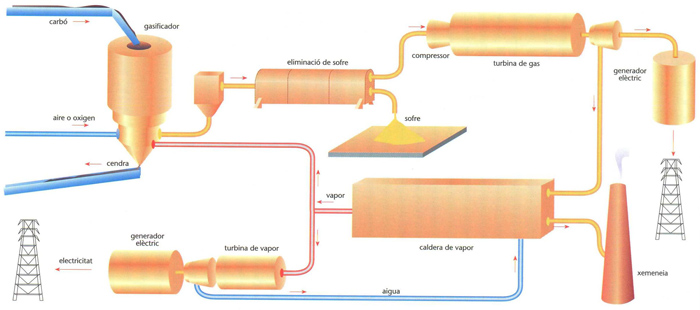
Procés de gasificació del carbó per a produir energia elèctrica
© Fototeca.cat
Química
Procediment de conversió d’un combustible sòlid o líquid en un gas combustible per combinació parcial del carboni amb l’oxigen, amb la qual hom obté una mescla gasosa rica en monòxid de carboni capaç de recombinar-se amb més oxigen i produir, així, una nova combustió.
La pèrdua de calor que s’esdevé en la formació del monòxid és compensada pels avantatges que representa de disposar d’un combustible gasós de combustió molt més perfecta i més neta, que permet un control millor de l’atmosfera de combustió i un aprofitament de combustibles sòlids de baix poder energètic
Ramon Mestres i Quadreny
Química
Químic.
Germà del compositor Josep Mestres i Quadreny Féu els seus estudis a la Universitat de Barcelona, on, el 1962, es doctorà en ciències químiques i el 1965 en filosofia a la Universitat d’Oxford Exercí la docència a les universitats de Sant Sebastià 1976, les Balears 1980 i València 1985 Posteriorment s’establí al Perú on ingressà 1986 com a professor a la Universitat de Piura A més de la docència, exercia funcions d’assessorament en la formació del professorat, en l’elaboració dels plans d’estudi i en l’organització del laboratori de química Dedicat a la recerca en el seu camp, ha…
biocombustible
Química
Tecnologia
Combustible constituït per un agregat de matèria orgànica, com ara deixalles domèstiques, sabons biodegradables, palla, fusta, restes de cereals, etc., amb un poder calorífic elevat que prové directament o indirectament de la captació i fixació d’energia solar en processos de fotosíntesi.
Es tracta d’un combustible sòlid, líquid o gasós d’origen biològic biomassa que ha seguit un procés de transformació per tal d’adaptar-lo a una funció substitutiva dels combustibles convencionals d’origen fòssil La idea inicial de la utilització de biocombustibles fou l’aprofitament de residus, principalment agrícoles, però també la fracció orgànica dels residus domèstics, per a obtenir una energia alternativa a un cost relativament baix Els biocombustibles generen menys emissions de diòxid de carboni que els combustibles fòssils, i es classifiquen en biocombustibles de primera , segona ,…
clorur de calci
Farmàcia
Química
Sòlid incolor, cristal·lí, molt soluble en aigua, amb la qual es combina formant nombrosos hidrats.
A diferència d’altres composts salins, és soluble en acetona i en diversos alcohols, amb els quals dóna composts d’addició Hom el pot obtenir en solució per neutralització de l’àcid clorhídric amb calç o carbonat de calci, i així resulta sovint com a subproducte en diversos processos industrials, en la fabricació de sosa pel procediment Solvay i en l’aprofitament de salmorres naturals El clorur de calci en estat de fusió dissol quantitats importants de calci metàllic 9 g/100 g de CaCl 2 i esdevé un líquid de color roig que hom atribueix a la presència, no confirmada, d’un…
absortància
Química
Nom que rep generalment el coeficient d’absorció quan és referit a l’àmbit de la construcció i, principalment, al càlcul d’instal·lacions per a l’aprofitament de l’energia solar.
Representa la relació entre la potència radiant absorbida per un material o per un sistema i la potència radiant que hi incideix
oxicloració
Química
Variant de la cloració per substitució en la qual el subproducte de la reacció, clorur d’hidrogen, és oxidat catalíticament a clor mitjançant oxigen, d’on resulta un aprofitament total de l’agent clorant.
El procés té una gran importància econòmica augmenta notablement la rendibilitat de les cloracions per substitució i és aplicat en un gran nombre de processos industrials
aigua
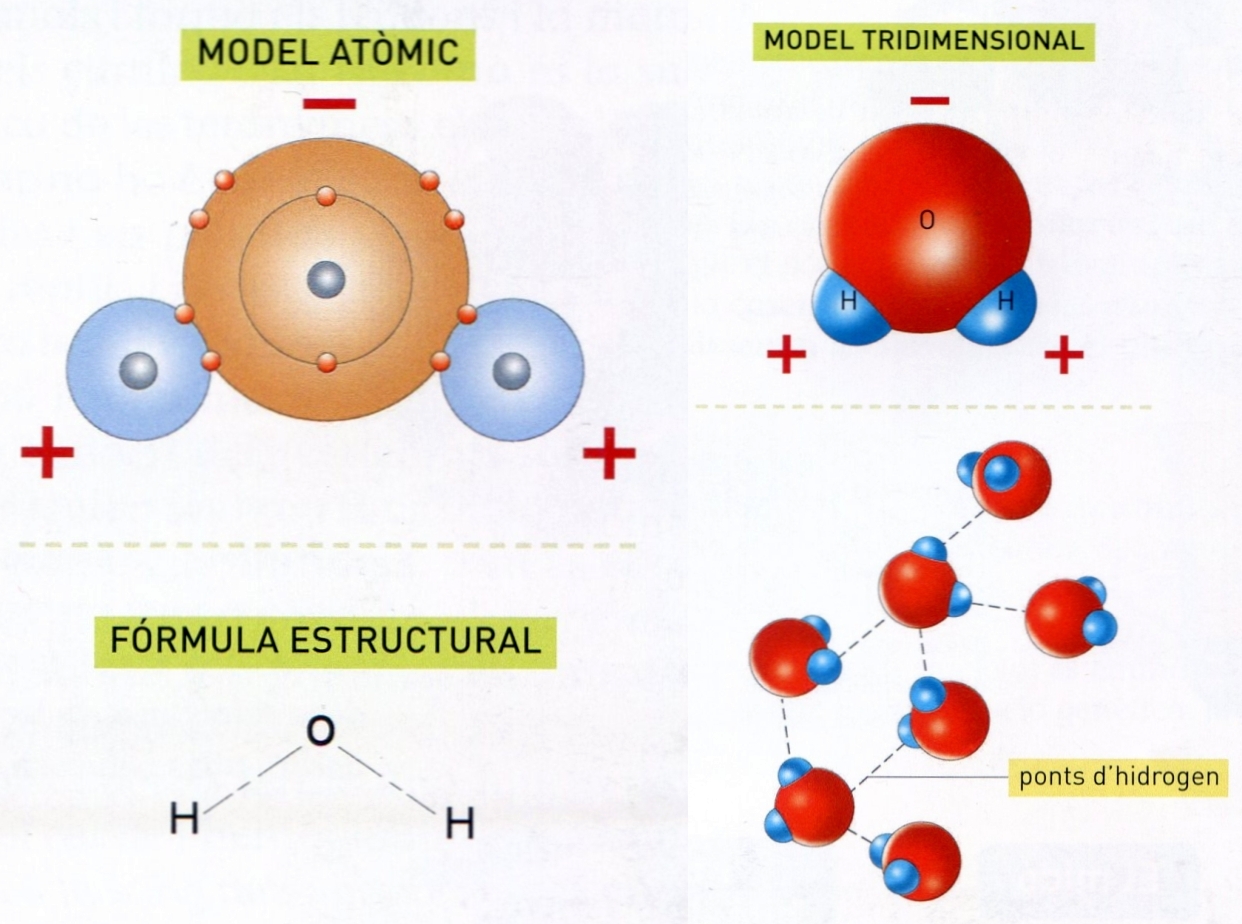
La molècula d’aigua
© Fototeca.cat
Química
Compost d’hidrogen i oxigen de fórmula H2O; atesos el seu paper a la natura i els seus innombrables usos, és la més important de totes les substàncies i fou considerada durant segles com un element.
Propietats fisicoquímiques de l’aigua Composició La seva composició fou establerta per síntesi per Cavendish el 1781 fent explotar una mescla d’hidrogen i oxigen 2H + O 2 → 2H 2 O L’anàlisi fou feta per Lavoisier i Meusnier, el 1783, descomponent el vapor amb ferro roent 4H 2 O + 3Fe → Fe 3 O 4 + 4H 2 La descomposició electrolítica H 2 O 2 + ½O 2 fou realitzada per primera vegada per Nicholson i Carlisle l’any 1800 La represa d’aquests experiments amb mètodes més precisos permeté de determinar exactament la composició ponderal, establir la fórmula definitiva i confirmar les lleis…
metall
Química
Nom donat a un nombre d’elements, aproximadament uns 70, situats a les primeres columnes de la classificació periòdica o en els períodes de transició, amb alts punts de fusió i d’ebullició, llevat de l’argent viu, que és líquid.
Tots aquests elements tenen en comú unes característiques determinades, que hom anomena característiques metàlliques, les quals representen un conjunt de propietats, com la malleabilitat, la brillantor, la conductivitat elèctrica i calòrica, etc, que es manifesten amb major o menor grau tant en les substàncies pures metalls purs com en les unions de diverses substàncies, és a dir els aliatges La densitat dels metalls és molt variable, entre 0,534 per al liti i 22,48 per a l’osmi, i el punt de fusió oscilla entre - 38,9°C per al mercuri i 3 410°C per al tungstè Propietats diferencials entre…
espectrometria
Astronomia
Física
Química
Estudi dels espectres mitjançant un espectròmetre.
Segons com sigui produït l’espectre hom distingeix diferents tipus d’espectrometria espectrometria de massa, espectrometria infraroja, espectrometria visible, espectrometria ultraviolada, espectrometria Raman efecte Raman, espectrometria d’emissió atòmica, espectrometria d’absorció atòmica , ressonància magnètica nuclear, ressonància paramagnètica electrònica ressonància de spin electrònic, espectrometria de raigs X, espectrometria de fluorescència X L’espectrometria tracta del mesurament de l’energia radiant emesa o absorbida per la matèria, com a resultat d’interaccions matèria-energia de…
brom
Química
Element no metàl·lic, de la família dels halògens, pertanyent al grup VII A de la taula periòdica, de nombre d’oxidació -1, 0, +1, +3, +5 i +7.
Propietats del brom Hom en coneix dos isòtops naturals de nombre màssic 79 i 81 Es presenta en forma de líquid roig fosc, i els seus vapors, d’olor semblant al clor, són fortament irritants Forma molècules diatòmiques Br 2 , molt estables, que només es dissocien apreciablement per damunt de 1000°C És relativament poc soluble en aigua la solució és anomenada aigua de brom , bé que la solubilitat canvia molt en presència de sals, sobretot de bromurs, amb els quals forma ions complexos, com Br 3 - i Br 5 - És molt soluble en alguns dissolvents orgànics sulfur de carboni, tetraclorur de carboni…