Resultats de la cerca
Es mostren 5 resultats
espectroscòpia d’ultraviolat i visible
Química
Tècnica espectroscòpica d’absorció (absorciometria).
Es basa en la interacció de la radiació electromagnètica de l’ultraviolat 100 nm ≤ λ ≤400 nm o del visible 400 nm ≤ λ ≤ 750 nm amb ions, molècules o radicals, la qual origina transicions entre diferents estats electrònics d’aquestes espècies, mitjançant la promoció d’electrons cap a orbitals moleculars desocupats Dels diferents tipus d’espectre, els d’ultraviolat i visible, coneguts genèricament com a espectres electrònics , són els que comporten bescanvis energètics més grans de l’ordre de 200-500 kJ L’absorció d’aquests tipus de radiacions provoca alhora variacions energètiques…
orbital molecular
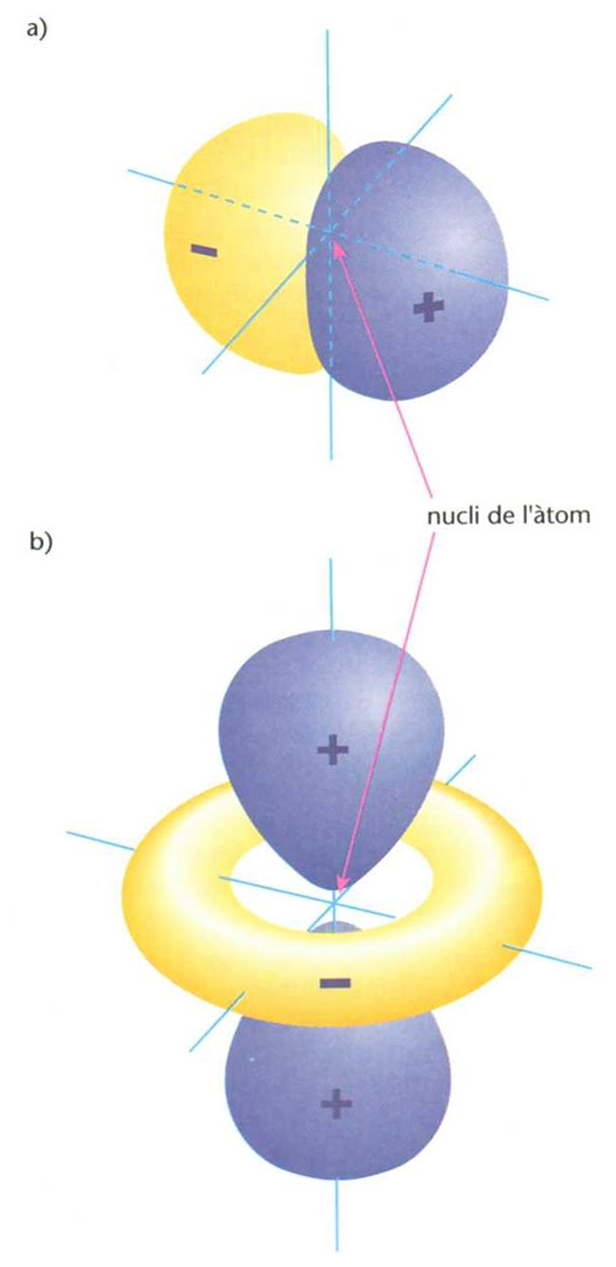
Representació tridimensional de dos orbitals (de nombres quàntics n=2,l = 1 (p) i m=1(a), i n =3,l = 2 (d) i m = 0 (b)) de l’àtom d’hidrogen en prèsencia de camp magnètic extern: assenyalen dos estats energètics de l’electró i la regió al voltant del nucli on és més probable de trobar l’electró en cadascun d’aquests dos estats (els valors de l i m determinen les dimensions, la forma i l’orentació de l’orbital): els caolors respresenten els signes + o - que pren la funció d’ona
© Fototeca.cat
Química
Cadascuna de les funcions d’ona, solució de l’equació de Schrödinger, associades a un electró que forma part d’una molècula.
Presenten les mateixes característiques matemàtiques que els orbitals atòmics Són de natura policèntrica i constitueixen en ells mateixos una interpretació de l’enllaç químic La descripció de l’estructura molecular mitjançant l’ús d’orbitals moleculars és coneguda com a teoria de l’enllaç dels orbitals moleculars , i consisteix a considerar inicialment la molècula com un conjunt de nuclis amb ordenació pròpia, determinar els diversos orbitals de nuclis i omplir els orbitals multicèntrics així obtinguts amb els electrons de la molècula, mitjançant un procediment anàleg al seguit per a establir…
enllaç de retrodonació
Química
Model teòric per a la interpretació de l’enllaç entre àtoms metàl·lics pesants de transició i molècules neutres, com ara el monòxid de carboni o una olefina.
En el cas d’una unió de tipus sigma σ entre el metall i la molècula, els orbitals n-1 d del metall tenen energies similars a les dels orbitals ns i np de la capa de valència i, per tant, poden participar en la formació d’enllaços Així, l’enllaç resultant pot considerar-se com a suma d’un enllaç sigma σ, originat per donació d’un parell electrònic no compartit del lligand a un orbital d buit i de simetria adient del metall, i d’una cessió de càrrega d’un orbital d ocupat del metall a un orbital antienllaçant π* desocupat del lligand neutre En el cas d’una unió de tipus pi π, opera un…
diborà
Química
Hidrur de bor de la sèrie dels borans que, com ells, presenta un dèficit d’electrons en l’estructura.
Hom admet que aquest compost disposa de 12 electrons de valència, quantitat suficient per a unir els sis hidrògens als àtoms de bor per enllaços covalents normals, no restant, però, cap electró per a l’enllaç bor-bor Per tal d’explicar aquest fet, el diborà ha estat molt estudiat La interpretació de les dades experimentals, sobretot espectroscòpiques, permet de suposar que el diborà presenta una estructura amb ponts d’hidrogen en la qual dos grups BHS22 són coplanaris i els dos hidrògens restants van disposats al mig, simètricament per sobre i per sota del pla Des del punt de vista de la…
reacció homolítica
Química
Reacció consistent en la ruptura d’un enllaç de forma homogènia; sobre cadascun dels dos fragments que es produeixen resta un electró procedent del doblet electrònic enllaçant.
Aquesta ruptura pot ésser catalitzada per la llum fotòlisi, per la calor piròlisi o per uns altres radicals