Resultats de la cerca
Es mostren 329 resultats
solució amortidora
Química
Solució el pH de la qual es modifica molt poc per dilució o per addició de quantitats moderades d’àcids o de bases, àdhuc forts.
Les solucions amortidores, dites també solucions tampó , deuen llurs propietats a la presència d’un sistema amortidor constituït, en general, per una mescla d’un àcid feble i una de les seves sals, o d’una base feble i una de les seves sals, o de dues sals estadis successius de la neutralització d’un poliàcid Escollint convenientment l’àcid o la base i les concentracions relatives, és possible d’obtenir solucions amortidores per a qualsevol valor del pH La magnitud de l’efecte amortidor és molt considerable L’addició de 10 ml de solució normal d’àcid fort a un litre d’aigua pura…
solució
Química
Mescla en la qual els components són distribuïts homogèniament en tota l’extensió del sistema.
En els sistemes binaris, hom acostuma a denominar solut el component minoritari, i dissolvent el majoritari, classificació que pot ésser estesa als sistemes de més components D’acord amb l’estat físic en què ocorren, hom sol distingir les solucions sòlides, les líquides i les gasoses Les solucions sòlides es formen mitjançant la interpenetració de les xarxes cristallines dels components, i llur formació exigeix no solament l’existència de forces atractives entre aquests, sinó també estructures cristallines idèntiques, cosa que ocorre principalment entre els sòlids que originen cristalls molt…
solució regular
Física
Química
Solució en què l’entropia de barreja té el valor esperat per a una solució ideal, però en la qual l’entalpia de barreja no és zero.
solució sobresaturada
Química
Solució que, a una temperatura determinada, conté una quantitat de solut superior a la que pot estar en equilibri amb el solut no dissolt (solubilitat, producte de solubilitat).
Les solucions sobresaturades es troben en equilibri inestable, però hi ha diverses tècniques per a provocar la precipitació o cristallització parcial fins a assolir un estat d’equilibri Atesa l’existència de factors dissolvent, pH, etc que permeten el manteniment de solucions sobresaturades o que provoquen, convenientment manipulades, llur precipitació, l’estudi de les dissolucions sobresaturades troba una gran aplicació en anàlisi química, tant gravimètrica com volumètrica coprecipitació, oclusió, precipitació, i en processos de cristallització, puix que la velocitat d’aquesta determina…
solució d’urea
Química
Transports
Additiu d’un sistema de reducció catalítica selectiva consistent en una dissolució sintètica d’urea al 32,5% en aigua desmineralitzada, continguda en un dipòsit específic del sistema, que reacciona amb els gasos resultants de la combustió del motor.
La forma AdBlue és una marca comercial
àcid
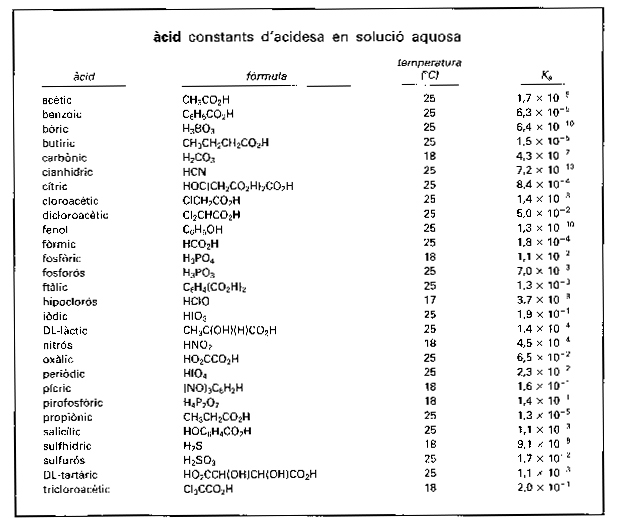
Constants d’acidesa en solució aquosa
Química
Cada una de les substàncies caracteritzades químicament pel fet de provocar canvis de color en les substàncies anomenades indicadors i de reaccionar molt ràpidament amb les substàncies d’un altre grup anomenades bases.
Les propietats típiques d’ambdós reactius desapareixen pel fet de la reacció, cosa que és interpretada com una neutralització mútua dels àcids i de les bases que dóna composts neutres tals com, per exemple, les sals Aquestes dues propietats essencials van acompanyades, en general, d’altres de menys fonamentals i no sempre presents, com el sabor àcid, l’activitat catalítica i la propietat —en solució aquosa— de dissoldre certes substàncies insolubles com els carbonats i molts metalls A més, els àcids i les bases poden desplaçar-se mútuament de llurs composts correlativament a…
aigua de clor
Farmàcia
Química
Solució de clor en aigua.
L’aigua dissol 4,61 volums de clor a 0°C i 2,26 a 20°C la solució té el color, el gust i l’olor del clor Refredada a 0°C diposita un hidrat, Cl 2 8H 2 O, que actualment es considera un clatrat L’aigua de clor es descompon a poc a poc per hidròlisi i a la llum dóna oxigen per descomposició de l’àcid hipoclorós format
cromatografia
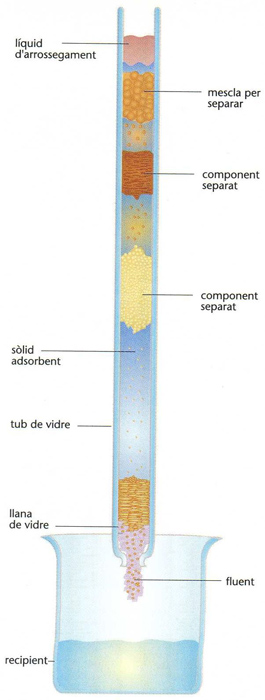
cromatografia en columna d’adsorció entre un sòlid (fase estacionària) i una solució líquida (fase mòbil)
© Fototeca.cat
Química
Mètode d’anàlisi immediat basat en la percolació d’una fase líquida o gasosa (mescla problema) al llarg d’una fase estacionària, que pot ésser sòlida —porosa o finament dividida— o bé líquida fixa impregnant un suport inert.
Els components de la mescla es separen d’acord amb llur distinta velocitat de migració tot al llarg de la fase estacionària Entren en la definició anterior la cromatografia de paper, la de capa fina, la de columna, la de gasos, i també la de bescanvi iònic i la de filtració per gels permeables les dues darreres tenen, però, algunes característiques especials Els ràpids progressos fets en la identificació, purificació i separació de vitamines, hormones, enzims, antibiòtics, alcaloides, proteïnes i alguns grups de substàncies inorgàniques no haurien estat possibles sense aquest conjunt de…
molaritat
Química
Nombre de mols de solut continguts en un litre de solució.
Hom la representa per la lletra M L’expressió HCl12M significa que 1 litre de la solució conté 12 mols d’àcid clorhídric 12 T 36,45 g, és a dir, 438 g/l de HCl Si hom agafa 0,5 l de la solució precedent, la concentració serà 12M, però contindrà només 6 mols de solut
concentració
Química
Quantitat d’una substància en una unitat de mescla, solució o mineral que la conté.
Correntment hom acostuma a expressar la concentració d’una manera general i, en el cas d’una solució, relacionant el solut en pes o en volum i cent parts en pes o en volum de la solució tant per cent en pes o en volum, relacionant el nombre de mols o el d’equivalents de solut i un litre de la solució molaritat i normalitat, respectivament, relacionant el nombre de mols de solut i un quilogram del solvent molalitat o bé relacionant el nombre de mols d’un component de la solució i el nombre total de mols dels components fracció molar
Paginació
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- …
- Pàgina següent
- Última pàgina