Resultats de la cerca
Es mostren 111 resultats
vapor saturat
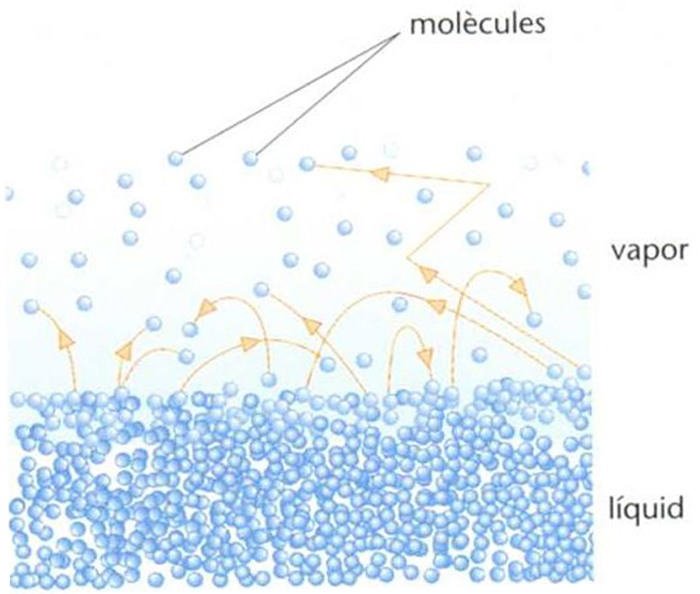
Representació del vapor saturat : en un instant donat, hi ha tantes molècules que es vaporitzen com molècules que es condensen
© Fototeca.cat
Física
En un recinte tancat o que es pugui considerar com a tal, dit del vapor d’una substància que és en equilibri amb la fase líquida d’aquesta, és a dir, que en un instant donat, per a unes determinades condicions de pressió i de temperatura, el nombre de molècules que es condensen i de molècules que es vaporitzen és el mateix.
Hom pot condensar totalment el vapor saturat d’un recinte tancat mitjançant l’inici d’una operació de compressió o de refredament, sense que la pressió ni la temperatura variïn mentre hi resti vapor per condensar
osmosi
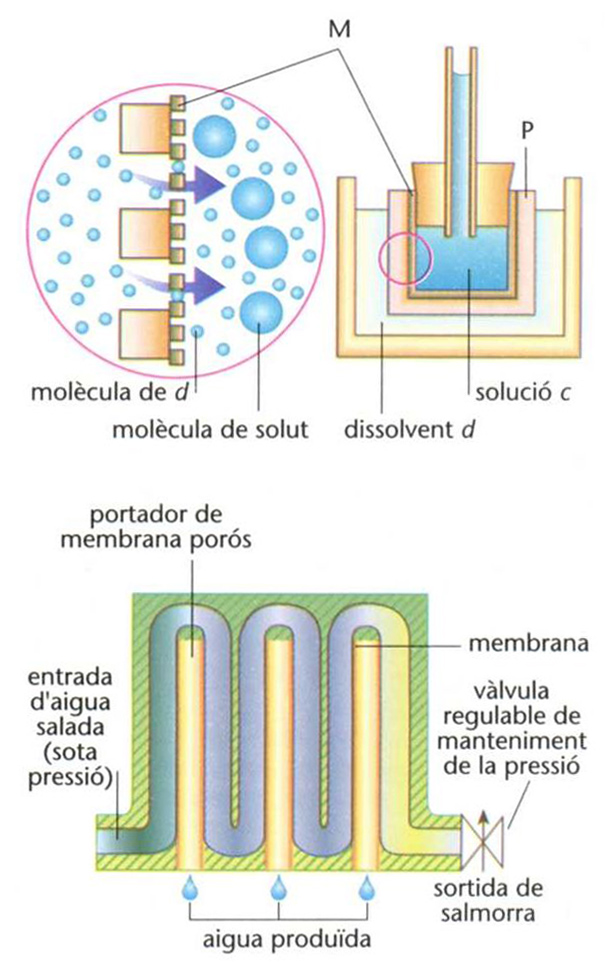
Omosi adalt, les molècules de d són les úniques que travessen la mambrana M (P suport porós); abaix, principi de funcionament d’una instalació d’osmosi inversa per a dessalar aigua de mar
© Fototeca.cat
Física
Química
En un sistema format per dues dissolucions de concentracions diferents, però amb el mateix dissolvent, separades per una membrana dita semipermeable,
tendència a passar dissolvent de la dissolució menys concentrada a la que ho és més.
Una membrana semipermeable, d’origen natural o artificial, és la que deixa passar uns tipus de molècules les del dissolvent i uns altres no les del solut
agitació tèrmica
Física
Moviment desordenat que, en funció de la temperatura, presenten les molècules de qualsevol substància.
En escalfar-se un sòlid augmenta l’agitació tèrmica de les seves molècules fins a vèncer les forces de cohesió que les manté unides, passant a l’estat líquid si la temperatura continua augmentant, el moviment arriba a ésser tan intens que les molècules s’independitzen estat gasós Segons la teoria cinètica, en el zero absolut de temperatura l’agitació tèrmica s’anulla L’observació del moviment brownià posà de manifest l’agitació tèrmica
gas perfecte
Física
Gas en el qual la interacció entre les seves molècules (forces de cohesió) és nul·la.
Físicament, un gas pot ésser considerat perfecte si les forces de cohesió són molt més petites que les forces exteriors a les quals és sotmès, independentment de la distància que separa les molècules, o bé si el gas és enrarit, és a dir, que la distància entre les molècules és suficientment gran i, per tant, les forces de cohesió són negligibles En un gas perfecte es compleix la relació pv = RT , p essent-hi la pressió, v el volum específic, T la temperatura absoluta i R la constant dels gasos Aquesta relació és l’anomenada equació d’estat dels gasos perfectes
autodifusió
Física
Difusió de les molècules d’una substància en d’altres de la mateixa substància.
Aquest fenomen té un interès pràctic quan hom estudia l’evolució de les molècules formades per àtoms pertanyents a diferents isòtops del mateix element traçador
gas
Física
Estat de la matèria en què les molècules que el componen resten poc lligades entre elles per les forces de cohesió.
No presenta ni una forma ni un volum definits, sinó que sempre omple totalment i uniformement el recipient que el conté És costum de dir que una substància és gas quan es presenta en forma gasosa a la temperatura ambient La densitat dels gasos sempre és més petita que la de la mateixa substància a l’estat sòlid o líquid, car, en el gas, les molècules resten molt més separades La calor específica d’un gas depèn de les condicions en què té lloc la variació de la seva temperatura a pressió constant o a volum constant La calor específica a pressió constant sempre és més elevada que a…
bescanvi isotòpic
Física
Entre dues molècules, substitució mútua d’àtoms d’un mateix element però isotòpicament diferents
.
L’ús de traçadors ha posat en evidència l’espontaneïtat de les reaccions de bescanvi isotòpic, bé que n'hi ha que necessiten la intervenció d’un catalitzador perquè llur velocitat sigui apreciable El bescanvi isotòpic té aplicacions en la preparació de composts marcats, la separació d’isòtops i com a mitjà d’estudi dels mecanismes de reaccions, dels enllaços químics i de l’estructura de les molècules
estat líquid

L’aigua, exemple d’estat líquid
(CC0)
Física
Estat de la matèria en què les molècules resten relativament lliures i poden canviar llur posició respectiva, però les forces de cohesió les obliguen a mantenir-se en un volum fix.
Els líquids ocupen un volum pràcticament constant en funció de la temperatura o la pressió L’estat líquid és l’intermedi entre el sòlid i el gasós els líquids i els gasos són anomenats fluids , i ambdós tenen una gran mobilitat molecular, manifestada en la difusió entre líquids o entre gasos, i no presenten rigidesa ni forma particular d’altra banda, líquids i sòlids constitueixen els estats condensats de la matèria, amb poca compressibilitat i amb interaccions moleculars elevades Dins un líquid, les molècules són atretes igualment en totes direccions per les veïnes i, per tant,…
llei d’Avogadro
Física
Llei enunciada per Amedeo Avogadro el 1811 en forma d’hipòtesi i actualment experimentada a partir de la llei de Gay-Lussac dels volums de combinació entre gasos, segons la qual volums iguals de gasos diferents, a igual pressió i temperatura, contenen el mateix nombre de molècules.
Si per a un gas determinat hom defineix un volum-tipus volum molar tal que, a 0°C i 760 mm de Hg de pressió pesi en grams el valor donat pel seu pes molecular molècula gram , el nombre de molècules que es troben en aquest volum és igual al nombre d’Avogadro, qualsevol que sigui el gas Generalitzant, hom pot afirmar que una molècula gram de qualsevol substància, en estat sòlid, líquid o gasós, conté un nombre de molècules igual al nombre d’Avogadro
estat sòlid

Diamants, exemple d’estat sòlid
(CC0)
Física
Estat de la matèria en què les molècules que la componen, a causa de les forces de cohesió, tenen un moviment entre elles molt restringit, limitat a una vibració entorn d’una posició d’equilibri fixa.
Quan un sòlid és format per molècules repartides regularment en l’espai, de manera que és possible de definir un vector constant que permet de passar d’un punt a un altre d’anàleg, hom diu que el sòlid és un cristall o que és cristallitzat quan hi ha un cert ordre, bé que no hi ha una regularitat en la xarxa, hom parla de quasicristall D’altres, però, tenen llurs components escampats aleatòriament per la massa que constitueix el cos i són anomenats amorfs , com és el cas del vidre, la fusta, el niló, etc De fet, només els cossos cristallins són considerats sòlids en l’estudi d’…
Paginació
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- …
- Pàgina següent
- Última pàgina