Resultats de la cerca
Es mostren 51 resultats
mètode de Rast
Química
Mètode analític per a la determinació de pesos moleculars de substàncies, introduït per K. Rast l’any 1922 i que es basa en una de les propietats col·ligatives de les dissolucions, el descens crioscòpic (crioscòpia).
El mètode consisteix a mesclar una petita quantitat del solut, el pes molecular del qual hom vol determinar, amb un excés de dissolvent i a determinar el punt de fusió de la mescla, la variació del qual respecte al del solvent pur és relacionada amb el pes molecular del solut Originàriament, hom emprà com a solvent la càmfora, atès el valor elevat que presenta la seva constant crioscòpica K f modernament, hom empra altres solvents de punt de fusió més baix, tals com el camfè o els clorofluoroetans freó Els valors dels pesos moleculars així determinats són…
criometria
Química
Mesura de les temperatures de congelació de les dissolucions.
En aplicar-hi la llei de Raoult, hom pot determinar la concentració de solut en la dissolució crioscòpia
osmosi
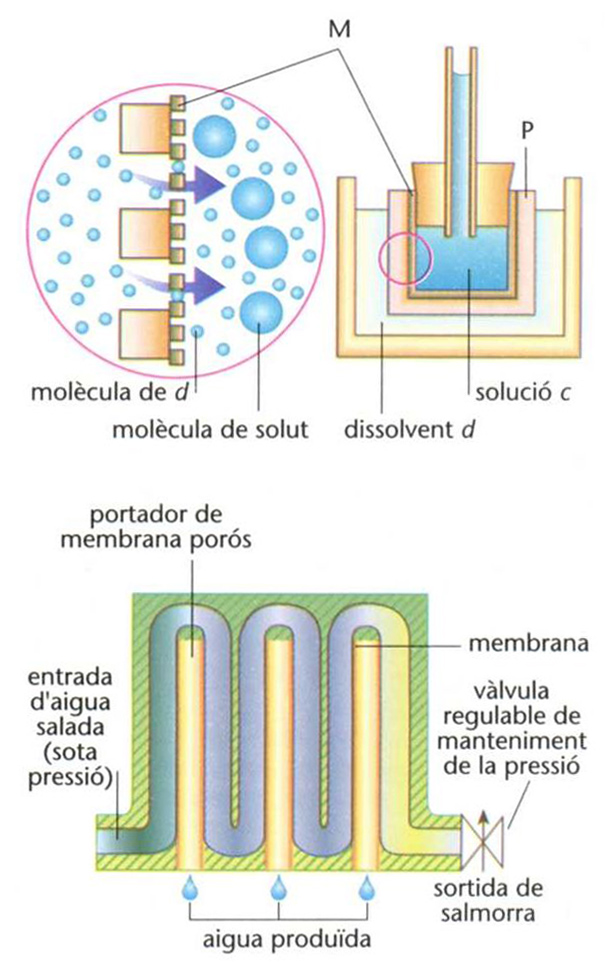
Omosi adalt, les molècules de d són les úniques que travessen la mambrana M (P suport porós); abaix, principi de funcionament d’una instalació d’osmosi inversa per a dessalar aigua de mar
© Fototeca.cat
Física
Química
En un sistema format per dues dissolucions de concentracions diferents, però amb el mateix dissolvent, separades per una membrana dita semipermeable,
tendència a passar dissolvent de la dissolució menys concentrada a la que ho és més.
Una membrana semipermeable, d’origen natural o artificial, és la que deixa passar uns tipus de molècules les del dissolvent i uns altres no les del solut
Charles Blagden
Metge i químic anglès.
Enuncià la llei de Blagden , segons la qual la disminució de la temperatura de solidificació d’una solució és proporcional a la concentració de solut si aquesta és baixa
coeficient osmòtic
Física
Química
Coeficient introduït per Bjerrum, que inclou tots els factors que expressen la desviació del comportament d’una solució respecte del comportament ideal.
D’aquesta forma, per un component i d’una barreja, el potencial químic s’expressa per μ i =μ o i + g i RT ln x i on g i és el coeficient osmòtic i x i és la fracció molar del solut en la dissolució
xoc osmòtic
Biologia
Química
Canvi sobtat en la pressió osmòtica que afecta un sistema o organisme viu.
S'esdevé en canviar l’organisme en un medi de diferent concentració cas d’organismes dulciaqüícoles en aigües salades o marins en aigües dolces o bé en afegir dissolvent o solut en el medi cas de cultius cellulars, en què hom pot fer esclatar les membranes cellulars o bé provocar l’encongiment de les cèllules
solució
Química
Mescla en la qual els components són distribuïts homogèniament en tota l’extensió del sistema.
En els sistemes binaris, hom acostuma a denominar solut el component minoritari, i dissolvent el majoritari, classificació que pot ésser estesa als sistemes de més components D’acord amb l’estat físic en què ocorren, hom sol distingir les solucions sòlides, les líquides i les gasoses Les solucions sòlides es formen mitjançant la interpenetració de les xarxes cristallines dels components, i llur formació exigeix no solament l’existència de forces atractives entre aquests, sinó també estructures cristallines idèntiques, cosa que ocorre principalment entre els sòlids que originen…
llei de Beer
Física
Llei que permet de calcular la disminució de la intensitat d’un raig de llum, o d’una radiació electromagnètica semblant, després d’haver travessat una solució.
La quantitat de llum absorbida I és donada per l’expressió essent la intensitat del raig de llum incident, b el coeficient d’absorció per unitat de concentració de solut, que depèn de la longitud d’ona de llum emprada, c la concentració de la solució, i x el gruix travessat per la radiació L' absorbància de les substàncies que satisfan la llei de Beer és proporcional a la concentració
absorciometria
Química
Mesurament de l’absorció de l’energia radiant per la matèria.
Hom fa passar la radiació emesa per un focus a través d’un gruix donat de la mostra de matèria per exemple, en forma de solució i la intensitat de la radiació emergent és mesurada per un detector adequat Aquesta mesura és comparada amb l’obtinguda en idèntiques condicions després que la radiació ha travessat el mateix gruix d’una substància suposada no absorbent per exemple, el dissolvent d’aquella solució La fracció de la radiació absorbida pel solut és donada per la raó entre les dues mesures, perquè, fent el mesurament d’aquesta manera comparativa, són eliminats els efectes de…
eluotròpic
Dit de la capacitat d’un solvent d’arrossegar els soluts retinguts en la fase estacionària d’un sistema cromatogràfic líquid o d’adsorció.
Aquesta capacitat depèn directament de la polaritat de cada solvent i és pràcticament independent de la naturalesa del solut retingut en la fase estacionària, amb la qual cosa es pot associar amb cada solvent una força eluotròpica característica Això permet de definir una sèrie eluotròpica de dissolvents ordenats segons la seva força Un dissolvent no polar, com per exemple el pentà, se situa al principi de la sèrie, mentre que l’aigua, que és fortament polar, ho fa a l’altre extrem La sèrie eluotròpica permet l’elecció del dissolvent, o del gradient de dissolvents, adequat per a…