Resultats de la cerca
Es mostren 14 resultats
dihidrat
Química
Compost que conté dues molècules d’aigua de cristal·lització en la molècula.
alúmina hidratada
Química
Qualsevol dels hidrats d’alúmina.
Els ben definits són el monohidrat Al 2 O 3 H 2 O diàspor i el trihidrat Al 2 O3 3H 2 O hidrargillita, hidròxid d' alumini La bauxita és, més o menys, un dihidrat molt impur
al·loxantina
Química
Compost que resulta de la reducció i la dimerització de l’al·loxana.
S'envermelleix a l’aire, dóna un dihidrat i es descompon a 253-255°C Poc soluble, dóna solucions aquoses àcides Provoca diabetis per destrucció selectiva de les cèllules β dels illots de Langerhans, per alteració de la permeabilitat de la membrana cellular
àcid periòdic
Química
Oxoàcid mineral sòlid, cristal·lí i incolor, que se sublima a 110°C i es descompon a 138°C.
És soluble en l’aigua i l’alcohol Forma un dihidrat, el qual perd l’aigua de cristallització a l’entorn dels 100°C Hom l’obté per reacció entre el iode i l’àcid perclòric concentrat o per electròlisi a baixa temperatura de solucions concentrades d’àcid iòdic És emprat com a oxidant
àcid piromel·lític
Química
Àcid tetracarboxílic aromàtic que es forma en la piròlisi de l’àcid mel·lític.
És un sòlid cristallí incolor que es fon a 276°C i es deshidrata amb facilitat per damunt d’aquesta temperatura per formar el dianhídrid És soluble en alcohol i poc soluble en l’aigua Absorbeix humitat de l’atmosfera tot formant un dihidrat, i té propietats irritants És emprat com a intermediari en la preparació de polièsters i poliamides
dicromat de sodi
Química
Cristalls vermells, molt solubles en l’aigua, que es fonen a 357°C.
Forma un dihidrat, molt estable, que és la forma comercial i es presenta en forma de cristalls deliqüescents Hom l’obté a partir de la cromita per torrefacció alcalina i posterior lixiviació És emprat com a oxidant, inhibidor de la corrosió, en la preparació de pigments i com a producte de partida per a altres composts del crom
àcid barbitúric
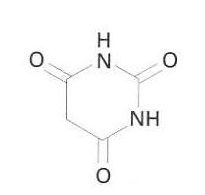
Àcid barbitúric
Farmàcia
Química
Ureid cíclic de l’àcid malònic.
Forma un dihidrat que es fon a 245°C amb una mica de descomposició és soluble en èter, no tant en aigua i alcohol Les solucions aquoses són àcides És obtingut per la condensació de l’èster malònic amb urea catalitzada per l’etòxid sòdic La substitució dels dos àtoms d’hidrogen en posició 5 per diversos grups dóna lloc a tota una gamma de productes farmacèutics barbiturat És emprat també com a catalitzador de polimerització i en la indústria de colorants
brucina

Brucina
©
Farmàcia
Química
Alcaloide extret de la nou vòmica.
Es presenta com a dihidrat o tetrahidrat en forma de pólvores amargants, cristallitzades en petites agulles, de tast molt amarg És soluble en els solvents orgànics Té el punt de fusió a 178ºC És emprada com a desnaturalitzant d’alcohols i olis, i en forma d’hidroclorur o de nitrat en medicina, amb les mateixes indicacions que l’estricnina, tot i que sembla que hom li ha descobert clares propietats carcinògenes en anàlisi química té utilitat per a separar mescles racèmiques
nitroprussiat
Farmàcia
Química
Cianocomplex de ferro.
La seva sal sòdica nitroprussiat sòdic és emprada per al reconeixement de l’ió sulfur S = , amb el qual dóna una coloració vermella fugaç, que és deguda al compost Na 4 FeNCN 5 NOS La sal sòdica té activitat com a fàrmac vasodilatador El seu dihidrat es presenta en forma de cristalls de color vermell, molt poc solubles en alcohol, i solubles en 2,3 parts d’aigua La solució aquosa és inestable en presència de llum En medicina és emprat per via intravenosa en les crisis hipertensives ja que actua produint vasodilatació perifèrica directa
arginina
Bioquímica
aminoàcid
essencial per al creixement, glucoformador, fortament bàsic (pK 1
= 2,18), constituent universal de les proteïnes, present en particular en proporcions molt elevades (fins prop del 75%) en les protamines.
La seva amida fosfòrica és el fosfagen dels músculs de certs invertebrats Els àlcalis bullents i l’arginasa el descomponen en urea i ornitina mitjançant aquesta reacció és un intermediari fonamental en la biogènesi de la urea cicle de l’ornitina Lliure o combinat amb les proteïnes dóna la reacció de Sakaguchi Per descarboxilació dóna l’agmatina La forma natural L + és obtinguda fàcilment hidrolitzant la gelatina i precipitant-la en forma de flavianat poc soluble Cristallitza en forma de dihidrat, que esdevé anhidre a 105°C Es descompon a 244°C