Resultats de la cerca
Es mostren 53 resultats
electròlit
Química
Substància que, fosa o dissolta en un solvent ionitzant, es dissocia donant ions i, doncs, esdevé conductora de l’electricitat.
Els electròlits són generalment àcids, bases o sals, i hom els classifica en forts o febles, segons que llur dissociació sigui completa o no, i en ionòfors i ionògens, segons que els ions en estat sòlid preexisteixin o no La dissociació parcial de l’electròlit permet de parlar d’un grau de dissociació, que ha estat estudiat i interpretat mitjançant les teories d'Arrhenius i de Debye-Hückel La conductivitat electrolítica és producte del moviment dels ions positius i negatius, i això la diferencia de la conductivitat deguda als electrons cas de la conducció en els metalls i en els…
no-electròlit
Química
Compost no iònic que dóna solucions aquoses no conductores de l’electricitat.
bateria de flux
Electrònica i informàtica
Bateria recarregable l’electròlit de la qual és format per substàncies electroactives i que flueix a través del reactor de la bateria on genera electricitat a partir d’una reacció electroquímica.
Aquest electròlit està emmagatzemat en un dipòsit des del qual s’alimenta el reactor La recàrrega és tan simple com afegir més electròlit i regenerar el que ja s’ha gastat en una reacció electroquímica reversible
ànode
Electrònica i informàtica
Química
Elèctrode receptor de càrregues negatives en tots aquells dispositius a l’interior dels quals existeix un medi no metàl·lic (gas més o menys enrarit, electròlit o semiconductor) que esdevé conductor sota determinades condicions.
Per l’ànode entra el corrent al dispositiu i, per tant, en surten els electrons cap al circuit exterior L’ànode és, doncs, l’elèctrode positiu en els dispositius alimentats per una font exterior de tensió i l’elèctrode negatiu en els dispositius generadors, piles o acumuladors En els tubs electrònics l’ànode, dit també placa , rep els electrons procedents del càtode gràcies a la tensió existent entre ambdós elèctrodes En un electròlit, l’ànode rep els anions de la solució, els quals són neutralitzats elèctricament, de forma que els electrons alliberats surten cap al circuit…
electròlisi
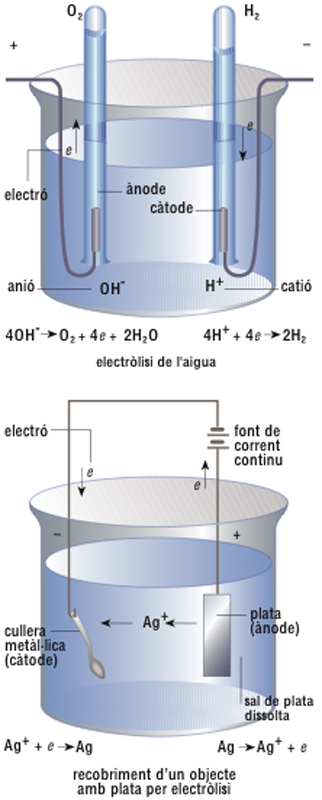
Esquema dels fenòmens d’electròlisi
© Fototeca.cat
Química
Tecnologia
Conjunt de fenòmens que s’esdevenen en el si d’una solució electrolítica o d’un electròlit fos en passar-hi un corrent elèctric de forma continuada.
Aquest terme fou creat en descobrir que el pas del corrent elèctric a través de determinades substàncies conductores solucions aquoses, sals foses permet de descompondre-les Les primeres experiències d’electròlisi foren fetes el 1800 per W Nicholson i A Carlisle en fer passar el corrent d’una pila de Volta per una solució d’aigua acidulada, amb obtenció d’hidrogen i oxigen H Davy, treballant sobre sals foses, obtingué el sodi i el potassi El 1833 M Faraday establí les lleis quantitatives de l’electròlisi que fixen les relacions existents entre la intensitat del corrent que travessa un medi…
càtode
Electrònica i informàtica
Química
Elèctrode fornidor de càrregues negatives i receptor de les positives en tots aquells dispositius a l’interior dels quals hi ha un medi no metàl·lic (gas més o menys enrarit, electròlit o semiconductor) que esdevé conductor sota determinades condicions.
Per tant, en els dispositius alimentats per una font de tensió exterior, pel càtode entren els electrons del circuit exterior cap a l’interior del dispositiu, i, per això, és l’electrode negatiu en canvi, és el positiu en els generadors electroquímics, piles o acumuladors En els tubs electrònics el càtode produeix electrons per algun tipus d’emissió termoelectrònica, fotoelectrònica, etc, els quals són atrets per l’ànode segons el tipus d’emissió hom parla de càtode termoelectrònic, càtode fotoelectrònic, càtode fred, etc En un rectificador sòlid, el càtode forneix també els electrons que, a…
pila
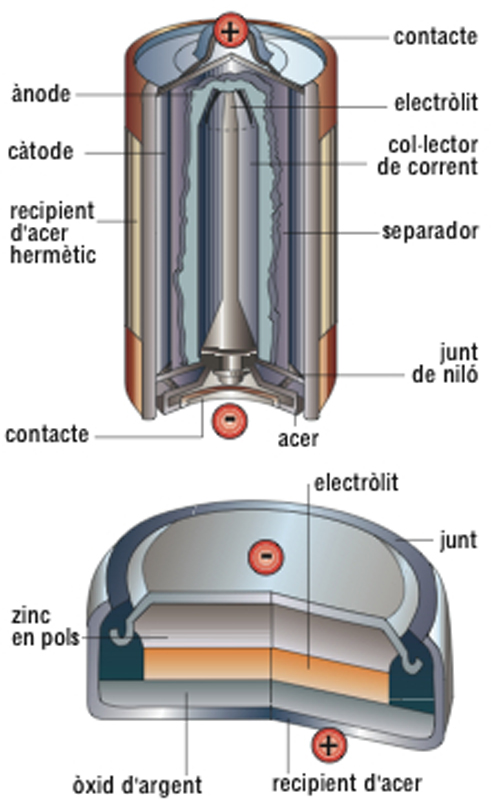
Esquemes d’una pila alcalina (a dalt) i d’una de botó d’òxid d’argent (a baix)
© Fototeca.cat
Química
Generador electroquímic que produeix una tensió contínua per acció d’una reacció química ( cel·la electroquímica
), tensió que va decreixent a mesura que la pila es va consumint.
És anomenada també pila elèctrica, pila galvànica o pila voltaica Essencialment es compon d’un electròlit i dos elèctrodes positiu i negatiu, que constitueixen un parell voltaic a més, hi ha el despolaritzador La primitiva pila de Volta 1793 era formada per una sèrie de discs de coure i zinc disposats alternativament i entre els quals hi havia unes peces de cartó o drap amarades d’àcid sulfúric Aquesta pila presentava l’inconvenient de polaritzar-se, i per això les posteriors modificacions introduïdes donaren lloc a diversos tipus de piles en les quals hom disposava un…
efecte anòdic
Química
En l’electròlisi ígnia, increment important i sobtat del voltatge, que es produeix quan la densitat de corrent anòdic depassa un cert valor crític, més alt com més elevada és la temperatura.
L’efecte anòdic és causat per la formació, entre l’ànode i l’electròlit fos, d’una pellícula gasosa contínua que actua com a aïllant En la fabricació de l’alumini hom observa l’efecte anòdic quan l’electròlit s’empobreix en alúmina La tensió passa de 5-6 volts a 20 volts o més el corrent s’estableix per formació d’un arc que trenca la capa de gas tot produint un so característic, i la cèllula s’escalfa en excés Per a cessar el fenomen cal afegir alúmina i remenar per accelerar-ne la dissolució per a prevenir-lo hom limita les dimensions dels ànodes per tal de…
bateria de liti
Electrònica i informàtica
Bateria d’un sol ús (no recarregable) composta per liti metàl·lic com a ànode i diòxid de manganès com a càtode.
L’electròlit sol ser una sal de liti dissolta en un dissolvent orgànic
coeficient d’activitat
Química
Quantitat γ per la qual cal multiplicar les pressions gasoses o les concentracions per a obtenir les activitats.
Amb les convencions usuals respecte als estats de referència, γ = a/P en el cas dels gasos i γ = a/c en el cas de les solucions Segons que la concentració sigui expressada en fracció molar, molalitat o molaritat, el valor numèric de γ varia L’interès dels coeficients d’activitat resideix en el fet que varien molt més lentament que les activitats i es presten millor, per tant, a les interpolacions i extrapolacions En el cas dels electròlits forts, com que és impossible calcular les activitats individuals dels ions, hom introdueix un coeficient d’activitat mitjà γ ± , deduïble de mesures, el…
Paginació
- 1
- 2
- 3
- 4
- 5
- 6
- Pàgina següent
- Última pàgina