Resultats de la cerca
Es mostren 10 resultats
amanitina
Bioquímica
Nom de dues substàncies extremament tòxiques, extretes de la farinera borda, d’estructura polipeptídica, considerades sovint com a alcaloides malgrat no tenir caràcter bàsic.
L' amanitina α C 4 0 H 5 6 N 1 0 O 1 3 S bloqueja específicament l’acció de l’enzim ARNpolimerasa en la reacció de síntesi de l’ARN missatger, i és l’amida de l' amanitina β C 4 0 H 5 5 N 9 O 1 4 S
àcid biliar
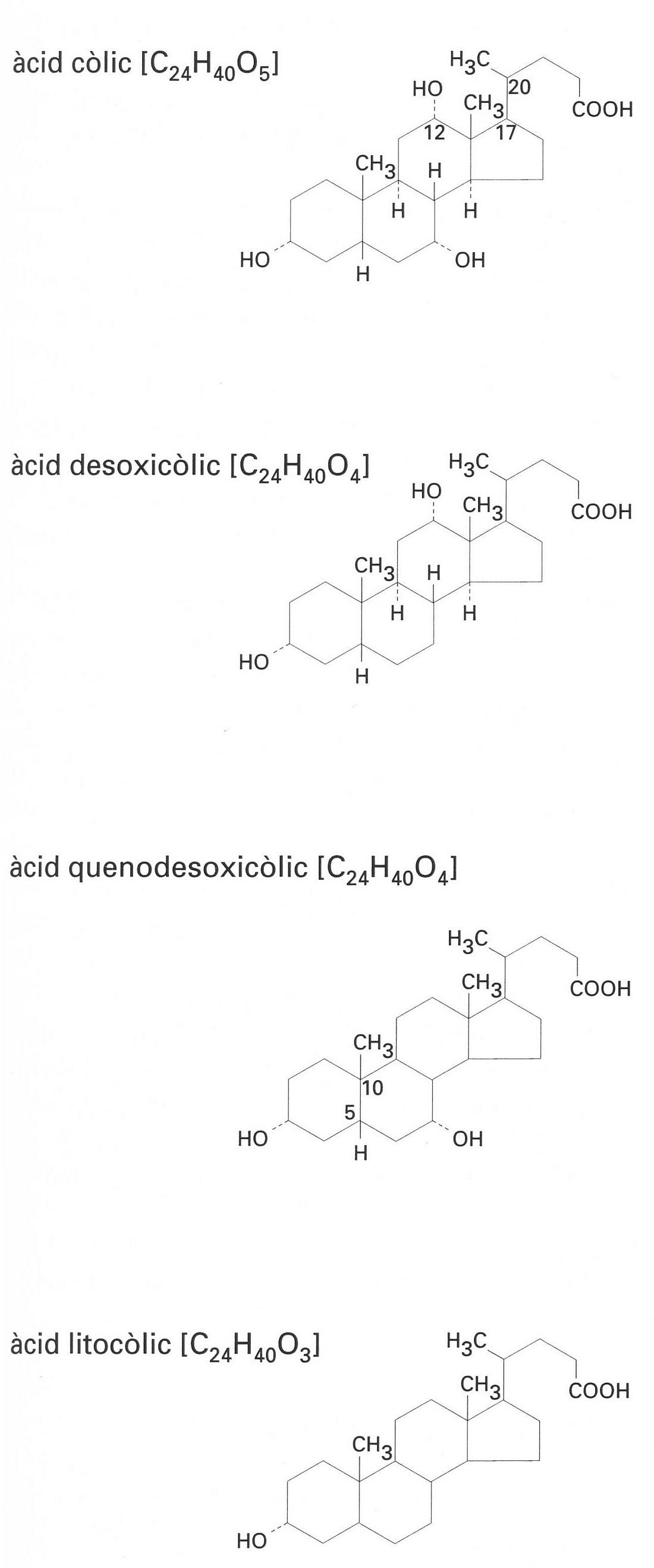
Àcids biliars
Bioquímica
Cadascun dels esteroides que hi ha a la bilis caracteritzats per la posició cis dels anells A i B i perquè tots els grups hidroxil són en posició a.
Els més coneguts són els àcids còlic , desoxicòlic , quenodesoxicòlic i litocòlic Provenen de la síntesi hepàtica a partir del colesterol i són a la bilis en forma de sals biliars conjugats amb la glicina o la taurina, i donen els àcids glicòocòlic i taurocòlic, per formació de l’amida entre els grup carboxílic de l’àcid biliar i el grup amina de l’aminoàcid
nicotinamida
Bioquímica
Amida de l’àcid nicotínic
.
També és anomenada niacinamida i factor PP preventiu de la pellagra Fou descoberta per Warburg i Christian el 1935 En l’organisme dels mamífers es forma a partir del triptòfan La seva importància bioquímica prové del fet que forma part dels piridin-nucleòtids, que tenen un paper fonamental com a coenzims transportadors d’hidrogen És el precursor del dinucleòtid adenina-nicotinamida NAD Es troba a totes les cèllules vivents i, en forma lliure, a l’orina dels animals
arginina
Bioquímica
aminoàcid
essencial per al creixement, glucoformador, fortament bàsic (pK 1
= 2,18), constituent universal de les proteïnes, present en particular en proporcions molt elevades (fins prop del 75%) en les protamines.
La seva amida fosfòrica és el fosfagen dels músculs de certs invertebrats Els àlcalis bullents i l’arginasa el descomponen en urea i ornitina mitjançant aquesta reacció és un intermediari fonamental en la biogènesi de la urea cicle de l’ornitina Lliure o combinat amb les proteïnes dóna la reacció de Sakaguchi Per descarboxilació dóna l’agmatina La forma natural L + és obtinguda fàcilment hidrolitzant la gelatina i precipitant-la en forma de flavianat poc soluble Cristallitza en forma de dihidrat, que esdevé anhidre a 105°C Es descompon a 244°C
asparagina
Bioquímica
Aminoàcid natural, no essencial, que intervé en el metabolisme del nitrogen en els vegetals.
La forma levogira L--asparagina és especialment abundant a les arrels i als brots de les lleguminoses i dels espàrrecs, d’on és extreta per hidròlisi enzimàtica també és obtinguda sintèticament Cristallitza com a monohidrat C 4 H 8 N 2 O 3 H 2 O que es fon a l’entorn de 234-235°C La funció amida li comunica propietats hidròfiles la hidròlisi àcida o alcalina dóna amoníac i àcid aspàrtic És emprada com a diürètic i per a preparar alguns medis de cultiu especials en bacteriologia Sembla ser que es tracta d’una substància indispensable en el desenvolupament de certes cèllules canceroses
biuret
Bioquímica
Amida de l’àcid al·lofànic, obtinguda escalfant la urea.
Es presenta en forma de cristalls que es fonen al voltant de 193°C i són solubles en aigua i alcohol Fa la típica reacció del biuret És emprada en anàlisi química
urea
Bioquímica
Amida de l’àcid carbònic, de fórmula (NH 2
) 2
C=O.
És el principal metabòlit de les proteïnes, i és excretat per l’orina a raó de 30 grams per dia en els individus humans adults Des d’un punt de vista històric, té una gran importància, puix que la seva síntesi, efectuada per FWöhler l’any 1828 per escalfament del cianat amònic quan ja era coneguda la natura metabòlica de la urea, representà l’inici del descrèdit de la teoria de la força vital i marcà l’inici de la recerca sistemàtica en el camp de la síntesi orgànica La urea es presenta en forma de cristalls blancs, gairebé inodors i de gust salí, solubles en aigua, alcohol i benzè, i…
dipèptid
Bioquímica
Molècula constituïda per dues unitats d’aminoàcid que van enllaçades formant una amida substituïda o enllaç peptídic.
Per hidròlisi els dipèptids es descomponen en els dos aminoàcids L’origen de molts dipèptids és la hidròlisi parcial de les llargues cadenes polipeptídiques de les proteïnes Als éssers vius hi ha també dipèptids que no provenen de les proteïnes, composts, alguns, d’aminoàcids poc abundants, entre els quals dipèptids hi ha l’anserina Nβ-alanil-1-metil-L-histidina dels músculs dels vertebrats
pèptid
Bioquímica
Polímer format per poques unitats d’aminoàcids units mitjançant grups amida resultants de la condensació d’un grup carbonílic i un grup amina de dos aminoàcids (enllaç peptídic).
Els pèptids es formen per hidròlisi parcial de les proteïnes i poden ésser degradats a aminoàcids per exemple, amb tripsina Hi ha pèptids que no deriven de les proteïnes, com el glutatió, la carnosina, l’oxitocina, la vasopressina, la bradiquinina, etc Molts pèptids petits han estat obtinguts cristallins Donen la reacció del biuret Hi ha diferents mètodes de síntesi de pèptids, però hom empra actualment un mètode automatitzat tècnica de la fase sòlida o de Merrifield per a la síntesi de grans pèptids fins a uns quaranta aminoàcids, no exempt, però, d’inconvenients
lípid
Bioquímica
Nom genèric de les substàncies constituïdes per un àcid alifàtic de cadena mitjana i nombre parell d’àtoms de carboni (de 4 a 30 àtoms), lligat per un enllaç èster, de vegades amida o èter, amb composts que tenen una funció alcohol o més (esfingosina, alcohols grassos superiors, etc).
Els lípids poden tenir també uns altres constituents en llur molècula, com ara àcids fosfòrics, àcid sulfúric, bases nitrogenades i sucres La presència de llargues cadenes hidrocarbonades en la molècula dels lípids els confereix la propietat d’ésser insolubles en aigua i solubles en solvents orgànics apolars Hom anomena lípids simples els que només contenen carboni, oxigen i hidrogen, i comprenen els triglicèrids, anomenats greixos greix o olis oli segons que siguin sòlids o líquids, les ceres cera i els èsters dels esterols esterol dins aquest darrer…