Resultats de la cerca
Es mostren 7 resultats
ornitina
Bioquímica
Aminoàcid no essencial que correspon a la fórmula NH2 (CH2)3 CH(NH2) COOH.
L’isòmer natural, L+ornitina, és soluble en l’aigua i l’alcohol i es fon a 140°C L’ornitina és produïda per l’organisme a partir de l'arginina, no formant part de la constitució de les proteïnes
cicle de l’ornitina
Bioquímica
Procés metabòlic que permet als organismes d’evitar una acumulació d’amoníac (procedent dels àcids glutàmic i aspàrtic) a concentracions elevades, mitjançant la formació d’urea.
L’àcid carbònic necessari, en forma activa carbamilfosfat, és transferit en un primer pas a l’ornitina
arginina
Bioquímica
aminoàcid
essencial per al creixement, glucoformador, fortament bàsic (pK 1
= 2,18), constituent universal de les proteïnes, present en particular en proporcions molt elevades (fins prop del 75%) en les protamines.
La seva amida fosfòrica és el fosfagen dels músculs de certs invertebrats Els àlcalis bullents i l’arginasa el descomponen en urea i ornitina mitjançant aquesta reacció és un intermediari fonamental en la biogènesi de la urea cicle de l’ornitina Lliure o combinat amb les proteïnes dóna la reacció de Sakaguchi Per descarboxilació dóna l’agmatina La forma natural L + és obtinguda fàcilment hidrolitzant la gelatina i precipitant-la en forma de flavianat poc soluble Cristallitza en forma de dihidrat, que esdevé anhidre a 105°C Es descompon a 244°C
arginasa
Bioquímica
Enzim que provoca la reacció d’hidròlisi:
i que actua també sobre les L-argines a-N- substituïdes.
Es troba present en molts teixits animals, i en concentració especialment elevada en el fetge de tots els vertebrats ureotèlics, i és al cap i a la fi l’enzim determinant de la producció d’urea com a metabòlit definitiu de la degradació de les proteïnes Intervé fonamentalment en el cicle de l’ornitina, proposat originàriament per Krebs, el qual explica la bioformació de la urea a partir del CO 2 respiratori i del NH 3 que resulta de les desaminacions biològiques L’arginasa, que és activable pel manganès i pel cobalt, ha estat obtinguda molt pura del fetge de cavall Hom n'ha…
citrul·lina
Bioquímica
Aminoàcid format en el cicle de la urea com a intermediari entre l’ornitina i l’arginina.
putrescina
Bioquímica
Diamina molt tòxica, d’olor desagradable, que es forma en la putrefacció de les proteïnes per descarboxilació de l’ornitina (ptomaïna).
És un sòlid cristallí, soluble en l’aigua, que es fon a 28°C i bull a 159°C Presenta caràcter fortament bàsic i és emprada en síntesi orgànica Forma un dihidroclorur que per escalfament es converteix en pirrolidina
aminoàcid
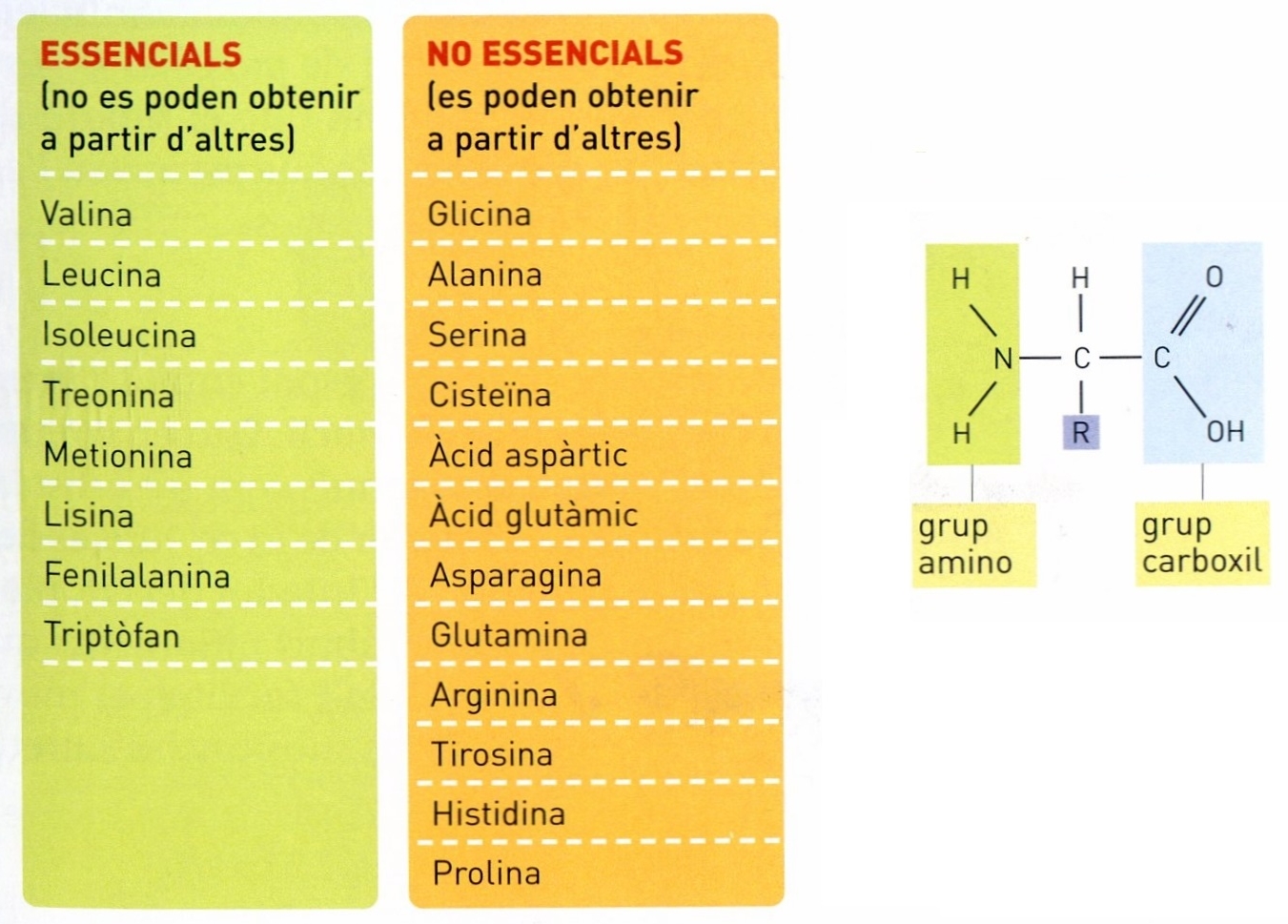
Els vint aminoàcids de les proteïnes i l’estructura d’un aminoàcid
© fototeca.cat
Bioquímica
Substància orgànica que té almenys una funció àcid carboxílic i una funció amina.
La posició relativa d’aquests dos grups ve indicada per les lletres α, β, γ,, i ϖ si els grups són als dos caps de la cadena Els aminoàcids són sòlids cristallins, en general poc solubles en aigua i en solvents orgànics, i tenen propietats amfòteres En solució existeixen en forma de sals internes formen ions mixtos per migració d’un protó del grup —COOH al grup —NH₂ Al laboratori són preparats per mètodes molt diversos entre els quals un dels més generals és la síntesi de Strecker Llurs propietats químiques combinen les dels àcids carboxílics i les de les amines, i per tant formen sals amb…