Resultats de la cerca
Es mostren 25 resultats
àcid
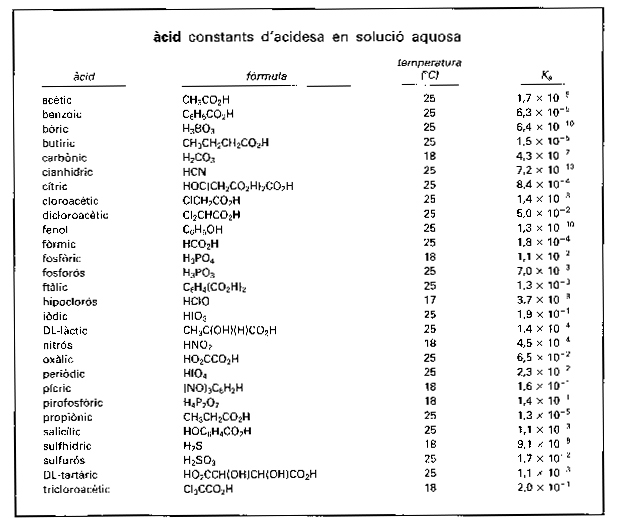
Constants d’acidesa en solució aquosa
Química
Cada una de les substàncies caracteritzades químicament pel fet de provocar canvis de color en les substàncies anomenades indicadors i de reaccionar molt ràpidament amb les substàncies d’un altre grup anomenades bases.
Les propietats típiques d’ambdós reactius desapareixen pel fet de la reacció, cosa que és interpretada com una neutralització mútua dels àcids i de les bases que dóna composts neutres tals com, per exemple, les sals Aquestes dues propietats essencials van acompanyades, en general, d’altres de menys fonamentals i no sempre presents, com el sabor àcid, l’activitat catalítica i la propietat —en solució aquosa— de dissoldre certes substàncies insolubles com els carbonats i molts metalls A més, els àcids i les bases poden desplaçar-se mútuament de llurs composts correlativament a llurs forces El…
afinitat
Química
Tendència d’una mescla de substàncies a reaccionar químicament, que ve mesurada per la disminució de l’energia lliure de Gibbs que la reacció, a temperatura i a pressió constants, provoca.
Històricament, bé que el mot havia estat utilitzat en un sentit similar des de més antic Albert Magne, la noció d’afinitat és a dir, d’‘inclinació’ mútua de les substàncies que reaccionen fou introduïda per tal d’explicar els fenòmens químics al segle XVIII, i popularitzada especialment per Boerhaave Per als químics de l’època, l’afinitat era la força desconeguda que provocava i mantenia la unió dels àtoms, i durant molts anys un gran esforç especulatiu fou fet per identificar-la Primerament, seguint el suggeriment de Newton, hom considerà que era una manifestació més de les…
equació de van der Waals
Química
Equació d’estat introduïda per J. D. van der Waals l’any 1873.
Fou la primera que intentà d’explicar les desviacions dels comportaments dels gasos respecte a la idealitat Té la forma a i b essent dues constants introduïdes per a tenir en compte, respectivament, la cohesió entre les molècules forces de van der Waals i llur volum Des d’un punt de vista termodinàmic, aquestes constants depenen de la pressió i el volum crítics de cada gas en particular Tot i representar una gran millora envers l’equació del gas perfecte gas 1 2, existeixen també desviacions respecte a aquesta, pel fet que les constants a i b depenen…
equació d’Onsager
Química
Equació deduïda el 1927 per L. Onsager, basant-se en la teoria de Debye-Hückel, que relaciona la conductivitat equivalent (Λ) d’una dissolució de concentració donada (c) i la conductivitat equivalent a dilució infinita (Λo).
La seva expressió és A i B essent constants que depenen exclusivament de la temperatura i del dissolvent L’equació és aplicable únicament a dissolucions diluïdes
reflux
Química
Operació consistent en l’ebullició d’un líquid en un recipient, generalment un matràs, de tal manera que els vapors, en condensar-se en un refrigerant convenientment acoblat a la part superior del sistema, reflueixin.
La finalitat química del reflux és de mantenir un sistema obert a una temperatura constant, generalment la del punt d’ebullició del solvent emprat, conservant igualment constants el volum i la composició del sistema
propietats additives
Química
Propietats que en un sistema donat vénen representades per la suma de les propietats corresponents dels elements que el constitueixen.
L’única propietat absolutament additiva és la massa, però en el cas de les mescles n'hi ha moltes d’altres que ho són de manera força aproximada Quan el sistema considerat és una molècula, només poden ésser propietats realment additives les que no depenen, o depenen molt poc, dels enllaços químics i de la geometria molecular Si considerem, per simplificar, un compost binari A α B β , una propietat F serà additiva quan F A α B β = αF A + βF B , F A i F B essent constants atribuïbles als àtoms A i B Aquest tipus d’additivitat és observat en molt pocs casos, i encara amb no gaire…
regla de Trouton
Química
Relació aproximada, enunciada per A. Pictet l’any 1876 i estudiada sistemàticament per F. Trouton l’any 1884, que estableix que el quocient entre l’entalpia molar de vaporització d’un líquid (ΔHv) i la seva temperatura absoluta d’ebullició (Te) és constant i igual a 21 si ΔHv s’expressa en calories.
Un corollari d’aquesta relació és la constància aproximada de l’entropia de vaporització de les substàncies líquides Cal fer esment del fet que els líquids associats presenten desviacions notables aigua, 26,1 etanol, 26,9, i també els líquids de punt d’ebullició elevat cadmi, 22,9 argent, 24,6 i els de pes molecular i de punt d’ebullició baixos nitrogen, 17,2 oxigen, 18,1 L’any 1915 JH Hildebrand introduí en aquesta regla una modificació, consistent a mesurar les entropies de vaporització a temperatures tals que les concentracions moleculars del vapor P/RT fossin constants, amb…
entalpia
Física
Química
Magnitud termodinàmica, funció d’estat del sistema físic considerat.
Per definició H = U + pV , H essent l’entalpia, U, l’energia interna, p , la pressió, i V , el volum El primer principi de la termodinàmica, en funció de l’entalpia, adopta la forma dQ = dH - Vdp , és a dir, la quantitat de calor fornida a un sistema és emprada per a augmentar-ne l’entalpia i fer un treball extern - Vdp En un procés a pressió constant per exemple, en un recipient obert en què actua sempre la pressió atmosfèrica, les variacions d’entalpia mesuren la quantitat de calor que hi intervé En una transformació a temperatura i pressió constants, l’entalpia mesura el…
lleis ponderals de la química
Química
Conjunt de lleis que constitueixen el fonament de l’estequiometria.
La formulació de les lleis ponderals arrenca, històricament, del principi de la conservació de la matèria d’AL Lavoisier, d’acord amb el qual, en una reacció química la massa de les substàncies reaccionants és igual a la massa dels productes de reacció Les lleis ponderals pròpiament dites són la llei de les proporcions recíproques de JB Richter 1792, d’acord amb la qual els pesos de dos elements o bé múltiples simples d’aquests pesos que reaccionen amb el mateix pes d’un tercer element poden també reaccionar entre ells la llei de les proporcions definides o constants , de JL…
associació
Química
Formació d’espècies moleculars relativament complexes per unió de dues o més molècules simples d’una mateixa substància.
Aquest fenomen és el responsable de les propietats físiques anormals que presenten l’aigua, l’amoníac, els alcohols, els fenols, els àcids carboxílics, etc Hom el troba en dissolucions, en líquids purs i en vapors i es manifesta pels mètodes corrents de determinació de pesos moleculars, puix que les molècules associades es comporten com a unitats de pes molecular múltiple, segons el grau d’associació Hom atribueix a associacions intermoleculars que en donar uns relatius complexos de doble, triple, etc, pes molecular del de les molècules simples fa que les substàncies que tinguin associacions…