Resultats de la cerca
Es mostren 6 resultats
acidimetria
Química
Part de la volumetria
que comprèn els mètodes d’anàlisi de substàncies de caràcter bàsic per valoració amb una solució d’un àcid de concentració coneguda.
Els mètodes de l’acidimetria són fonamentats en reaccions de neutralització , quan és una base lliure la que hom valora amb la solució àcida, o de desplaçament , quan la substància valorada és una sal d’un àcid molt dèbil i l’agent valorant un àcid fort Hom calcula la quantitat de substància bàsica problema a partir del volum d’agent valorant àcid necessari perquè la reacció arribi a ésser completa, moment que la solució assoleix un valor específic del pH Hom posa de manifest aquest moment mitjançant l’ús d’alguns dels indicadors de neutralització , substàncies orgàniques àcides o bàsiques…
biamperometria
Química
Tècnica electroanalítica de detecció del punt final d’una volumetria, relacionada amb l’amperometria i basada en l’ús de dos microelèctrodes inerts polaritzats, entre els quals hom aplica una petita diferència de potencial (potencial de polarització).
Si la solució que hom valora conté els dos membres d’un parell redox reversible —per exemple, iode-iodur, ions ferroII-ferroIII, etc—, aquesta diferència de potencial és suficient per a provocar el pas d’un corrent elèctric detectable en un galvanòmetre muntat entre els microelèctrodes, en un dels quals té lloc la reducció i en l’altre l’oxidació del parell mencionat, corrent que s’anulla, en el moment del punt final, quan desapareix de la solució un dels dos membres del parell Quan el parell redox present en la solució problema és irreversible, no passa corrent durant la valoració, però la…
indicador
Química
Compost químic emprat en anàlisi per a posar de manifest, generalment per un canvi de color, el punt d’equivalència de les volumetries.
Els indicadors de neutralització són àcids o bases febles, la forma ionitzada dels quals és de diferent color que la forma molecular El color resultant és així determinat pel valor del pH de la solució que hom valora Els més importants són el blau de timol, l’ataronjat de metil, el verd de bromocresol, la fenolftaleïna i la timolftaleïna Els indicadors mixts són mescles de dos indicadors o d’un indicador i un colorant, i fan més precisa la detecció del punt final Per a les volumetries de precipitació hom empra indicadors que donen lloc en el punt final a l’aparició o desaparició d’un…
anàlisi conductomètrica
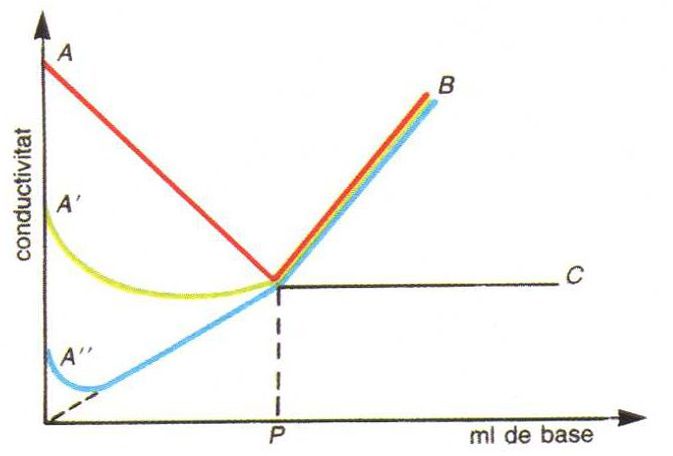
Valoració conductomètrica d’un àcid amb una base: corba AB, àcid fort amb una base forta; corba A'B, àcid mitjanament fort amb una base forta; corba A''B àcid feble amb una base feble; P, punt d’equivalència
©
Química
Procediment analític usat per a determinar el punt final de les volumetries, basat en la mesura de la variació de la conductivitat electrolítica de la solució problema deguda a l’addició de reactiu valorant.
Com que la conductivitat electrolítica depèn de la mobilitat dels ions presents en la solució i de llurs concentracions, l’addició d’un reactiu en provoca canvis importants sempre que doni lloc a la desaparició d’una espècie iònica de la solució sigui per formació d’un compost poc dissociat o d’una sal insoluble i a la seva substitució per quantitats equivalents d’un dels ions del reactiu de mobilitat diferent de la de l’espècie eliminada Així, hom pot dur a terme conductimètricament volumetries de neutralització, de precipitació i de formació de complexos, però només en casos favorables…
bromatometria
Química
Part de la volumetria que inclou els mètodes d’anàlisi en els quals el reactiu valorant és una solució de bromat de potassi.
Hom aprofita analíticament les propietats oxidants d’aquest compost potencial normal de reducció = +1,45 eV de dues maneres diferents per a valorar directament substàncies reductores o per a generar quantitats controlades de brom elemental per tal d’efectuar la bromació de substàncies orgàniques En el primer cas, hom fa la determinació volumètrica en medi àcid fort, en el qual la semireacció de reducció del bromat és la següent la qual serveix per a valorar reductors com ara arsènic III, antimoni III, estany II, coure I, ferro II, talli I, nitrit, selenit, iodur, monoclorur de iode i molts d’…
complexometria
Química
Procediment volumètric d’anàlisi quantitativa d’ions metàl·lics per valoració amb una solució patró d’una complexona
, especialment de la sal disòdica de l’àcid etilendiaminotetraacètic (EDTA), basat en la formació de complexos estables dels ions metàl·lics amb l’agent valorant, la qual formació dóna lloc en el punt d’equivalència a una variació brusca de la concentració d’aquells ions, que pot servir de base per a la detecció del punt esmentat.
El comportament de l’EDTA i de les complexones, en general és àmpliament selectiu per tal de poder determinar específicament cada metall cal procedir a la regulació del pH de la solució i a la introducció d’agents complexants auxiliars Així, els ions metàllics tetravalents i trivalents, que formen els complexos més estables, són valorats en medi fortament àcid, mentre que els divalents ho han d’ésser en medi neutre o bàsic segons l’estabilitat de llurs complexos Els agents complexants auxiliars cianur, trietanolamina, 2,3-dimercaptopropanol, etc són emprats per a formar amb els ions…