Resultats de la cerca
Es mostren 13 resultats
àcid aspàrtic
Bioquímica
Aminoàcid natural, no essencial, que intervé en els processos del metabolisme intermediari com a precursor important de composts nitrogenats i donador de grups amina.
La forma dextrogira L+-àcid aspàrtic és la més comuna i es fon a 270-271°C És especialment abundant a la canya de sucre tendra i a les melasses de sucre de bleda-rave Hom l’obté de la hidròlisi de les proteïnes i a partir de l’amoníac i de l’àcid fumàric És emprat en la investigació bioquímica i clínica, en detergents i com a fungicida i germicida
metionina
Bioquímica
Aminoàcid contingut normalment a les proteïnes
.
Els bacteris i les plantes el sintetitzen a partir de l’àcid aspàrtic, però és un aminoàcid essencial en la nutrició dels mamífers, perquè no el sintetitzen En la síntesi de proteïnes és l’aminoàcid iniciador de la cadena polipeptídica
base pirimidínica
Bioquímica
Substància de caràcter bàsic, derivada de la pirimidina i que forma part dels àcids nucleics.
En són exemples l'uracil, la timina, la citosina i la tiamina Les pirimidines es biosintetitzen a partir de l’àcid aspàrtic i a través de l’àcid oròtic Llur catabolisme acaba donant urea i amoníac en la majoria d’espècies animals
asparagina
Bioquímica
Aminoàcid natural, no essencial, que intervé en el metabolisme del nitrogen en els vegetals.
La forma levogira L--asparagina és especialment abundant a les arrels i als brots de les lleguminoses i dels espàrrecs, d’on és extreta per hidròlisi enzimàtica també és obtinguda sintèticament Cristallitza com a monohidrat C 4 H 8 N 2 O 3 H 2 O que es fon a l’entorn de 234-235°C La funció amida li comunica propietats hidròfiles la hidròlisi àcida o alcalina dóna amoníac i àcid aspàrtic És emprada com a diürètic i per a preparar alguns medis de cultiu especials en bacteriologia Sembla ser que es tracta d’una substància indispensable en el desenvolupament de certes cèllules…
aspartam
Alimentació
Química
Edulcorant artificial de fórmula C 1 4
H 1 8
N 2
O 5
.
Descobert el 1965, és un dels principals edulcorants utilitzat com a additiu alimentari i és centenars de vegades més dolç que el sucre Contràriament a altres edulcorants, no presenta cap regust i és relativament estable en un medi àcid, malgrat que no resisteix un escalfament fort A l’organisme, es transforma en fenilalanina, àcid aspàrtic i metanol, el primer dels quals és un aminoàcid essencial, és a dir, que l’ésser humà no el pot sintetitzar i l’ha d’obtenir de la dieta Als països de la UE el codi de l’aspartam es representa per E-951, i el seu ús no és aconsellable per a…
albúmina
Bioquímica
Nom genèric d’un grup de proteïnes solubles en aigua pura i en solucions salines diluïdes, insolubles en alcohol de grau elevat.
Les albúmines són solubles en solució mig saturada de sulfat d’amoni, però precipiten si la solució se satura amb aquesta sal i abans de la saturació si el medi és àcid tenen caràcter àcid punts isoelèctrics ben inferiors a 7, pes molecular elevat i són susceptibles de cristallització en condicions adequades Llurs solucions es coagulen per la calor entre 70°C i 90°C En total absència de sals no hi ha coagulació, però es produeix tanmateix una desnaturalització irreversible Les albúmines són, generalment, riques en àcids glutàmic i aspàrtic, lisina i leucina, contenen asparagina i…
Els aminoàcids essencials
L’organisme humà elabora les pròpies proteïnes a partir de la combinació dels diferents tipus d’aminoàcids que demanda el codi genètic Aquests aminoàcids són absorbits després de la digestió de les proteïnes contingudes en els aliments Tanmateix, l’organisme no solament és capaç de sintetitzar les proteïnes pròpiament dites, sinó de transformar alguns tipus d’aminoàcids en d’altres, mitjançant un procés metabòlic anomenat transaminació, que és portat a terme a l’interior de les cèllules hepàtiques Per tal d’elaborar les seves pròpies proteïnes, l’organisme requereix la presència de tots els…
aminoàcid
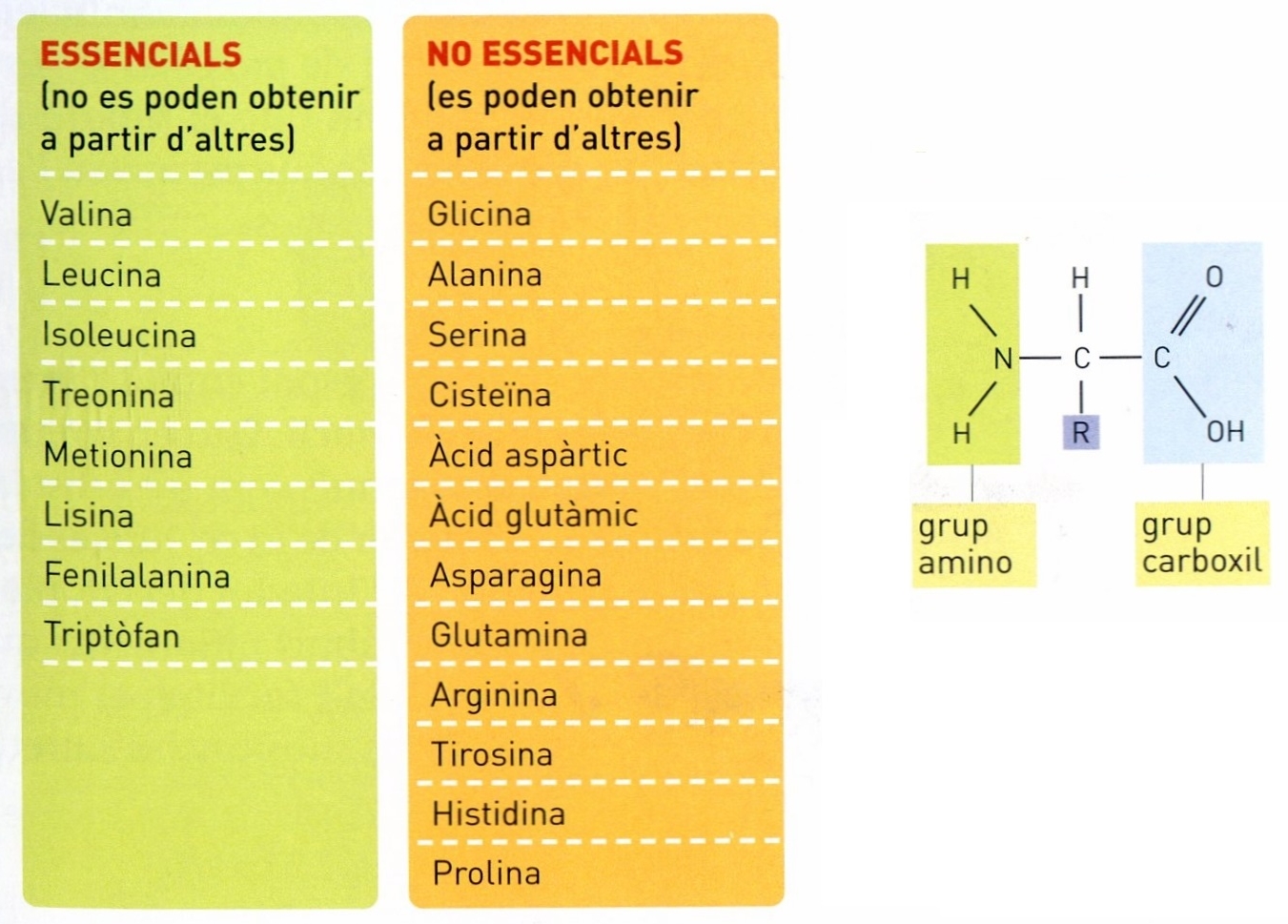
Els vint aminoàcids de les proteïnes i l’estructura d’un aminoàcid
© fototeca.cat
Bioquímica
Substància orgànica que té almenys una funció àcid carboxílic i una funció amina.
La posició relativa d’aquests dos grups ve indicada per les lletres α, β, γ,, i ϖ si els grups són als dos caps de la cadena Els aminoàcids són sòlids cristallins, en general poc solubles en aigua i en solvents orgànics, i tenen propietats amfòteres En solució existeixen en forma de sals internes formen ions mixtos per migració d’un protó del grup —COOH al grup —NH₂ Al laboratori són preparats per mètodes molt diversos entre els quals un dels més generals és la síntesi de Strecker Llurs propietats químiques combinen les dels àcids carboxílics i les de les amines, i per tant formen sals amb…
Síntesi de proteïnes
Genètica
Cada gen estructural té la informació pertinent per a l’elaboració d’un determinat polipèptid En alguns casos la cadena polipeptídica sintetitzada a partir de la informació d’un gen constitueix una proteïna en altres casos, la informació existent en dos o més gens actua conjuntament, originant les diverses cadenes peptídiques que poden constituir algunes proteïnes La manera com el ADN emmagatzema aquesta informació, si bé a primera vista sembla molt complexa, de fet té un principi senzill la llarga molècula de ADN, segons la disposició dels seus elements, disposa d’un codi o alfabet de quatre…
cicle de l’ornitina
Bioquímica
Procés metabòlic que permet als organismes d’evitar una acumulació d’amoníac (procedent dels àcids glutàmic i aspàrtic) a concentracions elevades, mitjançant la formació d’urea.
L’àcid carbònic necessari, en forma activa carbamilfosfat, és transferit en un primer pas a l’ornitina