Resultats de la cerca
Es mostren 13 resultats
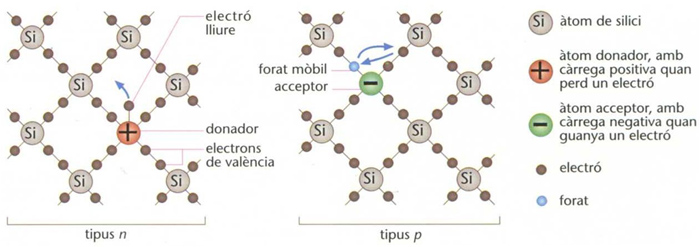
sílice
fototeca.cat
©
Mineralogia i petrografia
Química
Mineral que ocorre a la natura tant en forma pura ( quars
, cristobalita
) com en una gran varietat de formes impures ( sorra
, àgata
, calcedònia
, òpal
, etc).
Abundant com a component de les roques, és infusible i insoluble, la seva densitat oscilla entre 2,65 i 2,80, representa el paper d’àcid dins el grup dels silicats i presenta una fractura vítria Pot ésser també preparada sintèticament a partir de silicats solubles, per deshidratació i calcinació La sílice presenta una estructura polimèrica, constituïda per tetràedres de SiO 4 , els vèrtexs dels quals són ocupats pels quatre àtoms d’oxigen Es presenta en forma de cristalls incolors o pólvores cristallines blanques, inodores i insípides, insolubles en l’aigua i els àcids, excepte el fluorhídric…
zeolita
Química
Denominació genèrica de diversos aluminosilicats, tant naturals com sintètics, d’estructura tridimensional, la part aniònica dels quals pot ésser representada per la fórmula [(Al, Si)O2] n
.
Presenten, com a característica més important, xarxes obertes que determinen l’existència de cavitats en el si de l’estructura, la qual cosa permet el seu ús com a bescanviadors d’ions i, fonamentalment, com a adsorbents selectius d’una gran efectivitat Actualment hom coneix un gran nombre de zeolites sintètiques, les quals responen a fórmules del tipus M n x / n AlO 2 x SiO 2 y z H 2 O i constitueix un grup de materials d’una gran importància ecònomica Una de les més emprades és la fórmula Na 1 2 AlO 2 1 2 SiO 2 1 2 27 H 2 O que hom obté per…
silicat
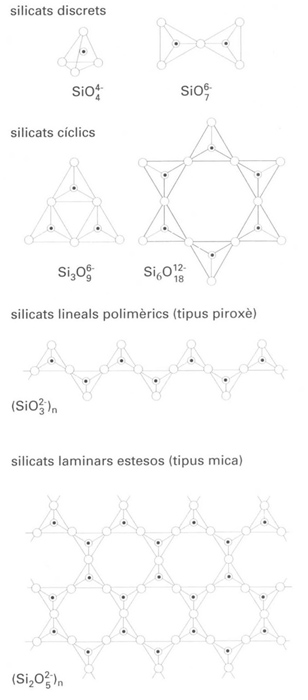
Estructura dels silicats
© fototeca.cat
Química
Denominació genèrica dels anions poliatòmics que contenen el silici com a àtom central i dels composts, de natura molt diversa, que contenen els esmentats anions.
Els silicats poden ésser obtinguts per fusió conjunta de la sílice SiO 2 amb carbonats de metalls alcalins, en forma de mescles complexes La solubilitat en l’aigua d’aquestes mescles varia proporcionalment a llur contingut en àlcali, i les espècies presents varien des d’anions discrets, com és ara SiO 2 OH 2 2 - , fins a espècies polimèriques D’altra banda, hi ha un gran nombre de silicats, d’ocurrència natural, l’estructura dels quals es basa en la del tetràedre de SiO 4 , i que gaudeixen d’una gran importància per llurs aplicacions Hom ha classificat…
àcid silícic
Química
Denominació no sistemàtica de la sílice amorfa i hidratada que hom obté per acidificació del silicat de sodi.
D’acord amb la concentració inicial del silicat, pot presentar aspectes que van des del gel fins a la solució colloidal Estructuralment, és constituït per una xarxa polimèrica tridimensional desordenada de tetràedres de SiO 4 , en la qual una certa proporció d’àtoms d’oxigen es troben substituïts per grups hidroxil Hom el pot representar per la fórmula SiO 2 nH 2 O La diferència entre l’àcid silícic i el gel de sílice és, però, merament quantitativa
àcid fluorosilícic
Química
Substància que només és coneguda en dissolució, on es comporta com un electròlit fort.
Hom l’obté mitjançant la reacció 6HF + SiO 2 →H 2 SiF 6 + 2H 2 O o per hidròlisi aquosa del SiF 4 en fase de vapor es dissocia en els seus components H 2 SiF 6 ⇋HF 2 + SiF 4 Amb els metalls forma fluorosilicats, segons la reacció Zn + H 2 SiF 6 →ZnSiF 6 + H 2 ↑ És emprat com a agent esterilitzador
aluminosilicat
Química
Designació genèrica dels silicats dobles d’alumini i d’un altre metall, monovalent o divalent.
Els aluminosilicats són sòlids, generalment d’origen natural i de constitució complexa Hom interpreta llur estructura, com la dels silicats en general, considerant la manera com estan units els grups tetraèdrics SiO 4 en l’edifici cristallí En alguns aluminosilicats, tals com el beril , aquests grups formen estructures cícliques, i en d’altres, com ara les miques , formen capes de dues dimensions El cas més corrent és, però, aquell en què formen estructures contínues de tres dimensions, amb substitució parcial, de manera regular i ordenada, del silici per alumini també…
àcid fluorhídric
Química
Nom no sistemàtic amb què és conegut el fluorur d’hidrogen, de fórmula HF.
És el derivat més important del fluor i el compost fonamental per a obtenir nombrosos derivats fluorats, minerals o orgànics Es presenta en forma d’un líquid d’olor irritant, que desprèn fum corrosiu Les molècules es polimeritzen i formen el seu hexàmer, HF 6 , car s’associen per formació de ponts d’hidrogen En solució amb aigua, es comporta com un àcid mitjanament fort, i forma sals amb els metalls que són per dessota de l’hidrogen en l’escala dels potencials electroquímics, i també amb els òxids metàllics i els carbonats Amb el silici i els silicats reacciona segons un procés autocatalític…
àcid silícic
Química
Denominació genèrica de diversos àcids —H4SiO4 (ortosilícic), H2SiO3 (metasilícic), etc—, no coneguts en estat lliure, dels quals deriven formalment els silicats.
silici
Química
Element químic de nombre atòmic 14 i símbol Si, pertanyent al grup IV A de la taula periòdica, aïllat per J.J.Berzelius l’any 1824 per reducció amb potassi del tetrafluorur de silici (SiF4).
És, després de l’oxigen, l’element més abundant de l’escorça terrestre, de la qual constitueix un 26% en pes És constituït per una mescla de tres isòtops naturals, estables, amb masses 28 92,21%, 29 4,70% i 30 3,09%, que determinen un pes atòmic de 28,086 Són també coneguts cinc radioisòtops artificials de l’element, amb masses que van de 25 a 32 El silici és àmpliament difós a la natura, i hom ha detectat la seva presència al Sol, en estels i en meteorits No ocorre natiu i les seves menes més importants són les diverses varietats de sílice SiO 2 i els silicats L’obtenció de l’…
oxigen
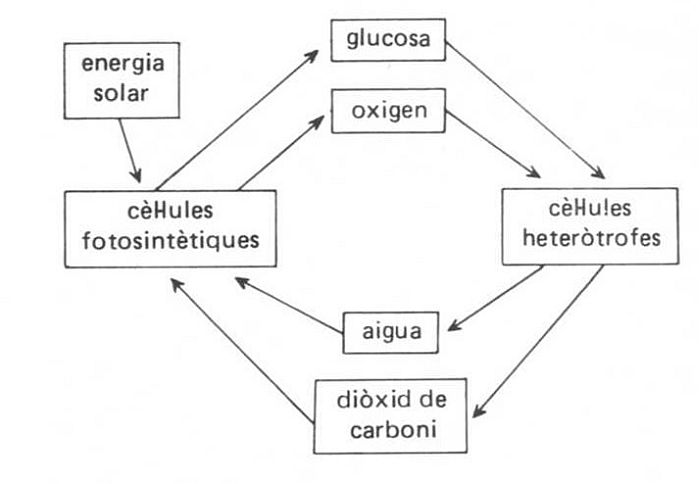
Cicle de l’oxigen
Química
Element no metàl·lic pertanyent al grup VI de la taula periòdica, de nombre atòmic 8, el més abundant de l’escorça terrestre.
Fou descobert, independentment, per J Priestley 1774 i KW Scheele 1773 El 1775 Antoine Laurent Lavoisier li donà el nom definitiu i basà en ell la seva teoria de la combustió i l’oxidació L’oxigen es troba a la natura en estat lliure, com a O 2 i, en molt més petita proporció, com a O i O 3 ozó constitueix el 23% de la massa de l’atmosfera, i combinat en un gran nombre de composts, els més importants dels quals són l’aigua, la sorra SiO 2 i els silicats, constitueix el 46,5% de la massa de l’escorça terrestre Existeix en forma de tres isòtops naturals estables 16 O 99,759%,…