Resultats de la cerca
Es mostren 18 resultats
lantànid
Química
Cadascun dels 15 elements químics els nombres atòmics dels quals van del 57 (lantà) al 71 (luteci), els quals, juntament amb l’escandi i l’itri, formen el grup de les terres rares.
Les propietats físiques dels lantànids i de llurs composts varien molt d’un element a l’altre, i la interpretació teòrica d’aquestes propietats, d’acord amb l’estructura electrònica, constitueix una confirmació de la validesa de les teories quàntiques Els lantànids són feblement electronegatius i, per tant, bescanvien amb facilitat llurs tres electrons perifèrics per donar combinacions iòniques
Jaume Arbós i Tor
Química
Químic.
El 1857 installà una fabrica de gas a Mataró, i cinc anys després patentà el primer gasogen d’aspiració L’anomenat gas Arbós , que es feu servir a diferents punts de Catalunya, és una barreja de gas d’aigua amb un hidrocarbur que dóna brillantor a la flama Féu treballs, alguns dels quals foren publicats, sobre temes químics, i d’altres d’interpretació de la ciència, des d’un punt de vista teològic
orbital molecular
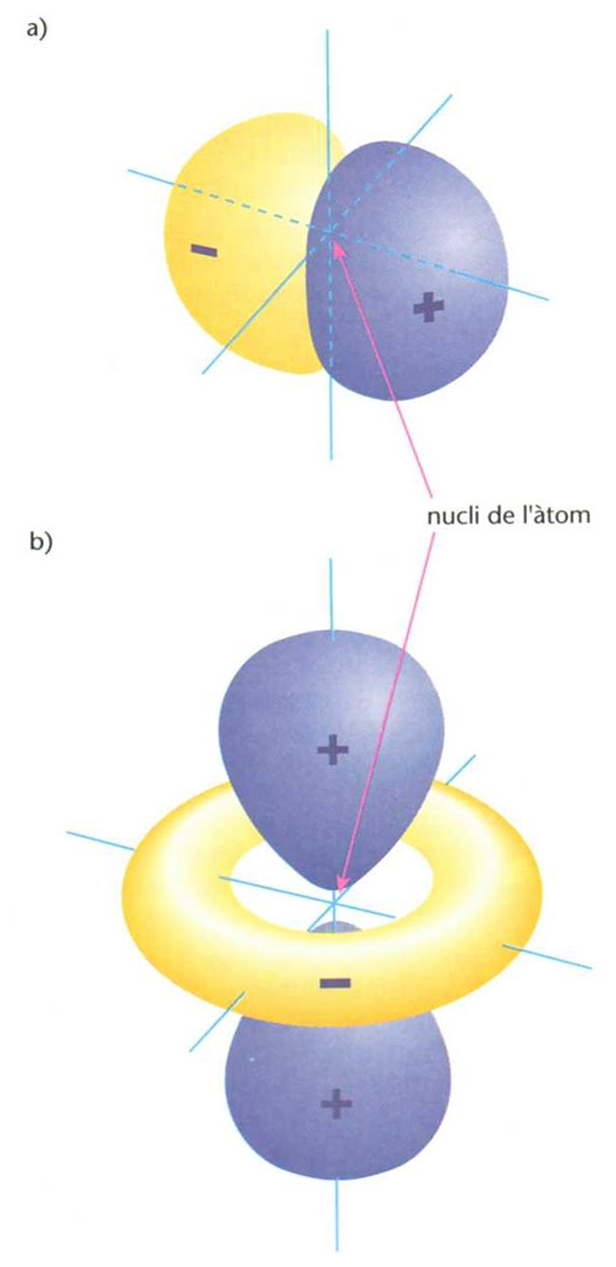
Representació tridimensional de dos orbitals (de nombres quàntics n=2,l = 1 (p) i m=1(a), i n =3,l = 2 (d) i m = 0 (b)) de l’àtom d’hidrogen en prèsencia de camp magnètic extern: assenyalen dos estats energètics de l’electró i la regió al voltant del nucli on és més probable de trobar l’electró en cadascun d’aquests dos estats (els valors de l i m determinen les dimensions, la forma i l’orentació de l’orbital): els caolors respresenten els signes + o - que pren la funció d’ona
© Fototeca.cat
Química
Cadascuna de les funcions d’ona, solució de l’equació de Schrödinger, associades a un electró que forma part d’una molècula.
Presenten les mateixes característiques matemàtiques que els orbitals atòmics Són de natura policèntrica i constitueixen en ells mateixos una interpretació de l’enllaç químic La descripció de l’estructura molecular mitjançant l’ús d’orbitals moleculars és coneguda com a teoria de l’enllaç dels orbitals moleculars , i consisteix a considerar inicialment la molècula com un conjunt de nuclis amb ordenació pròpia, determinar els diversos orbitals de nuclis i omplir els orbitals multicèntrics així obtinguts amb els electrons de la molècula, mitjançant un procediment anàleg al seguit…
efecte de quelat
Química
Fenomen consistent en un gran augment de l’estabilitat dels complexos de coordinació quan llurs lligands són multidentats i originen quelats, respecte a complexos molt semblants amb lligands monodentats.
N'és un exemple característic la comparació dels següents equilibris on l’efecte de quelat determina una estabilitat 10 10 vegades més gran del segon sistema respecte al primer Dels dos factors que determinen en definitiva la formació i l’estabilitat dels complexos, variació d’entalpia i variació d’entropia, l’efecte de quelat és de natura netament entròpica, havent estat explicat el guany entròpic del sistema en el procés de quelació per l’augment del nombre total de molècules lliures o, partint de l’establiment del primer enllaç entre l' agent quelant i l’ió metàllic, pels factors estèrics…
coordinació
Química
Formació d’un enllaç químic entre un element ió o compost de natura electròfila (acceptor de parells d’electrons, a causa, per exemple, de contenir orbitals de valència vacants) i un ió o molècula nucleòfil (donador de parells electrònics).
L’enllaç és anomenat coordinat i a voltes semipolar en la teoria electrònica de la valència de Gilbert Newton Lewis i Nevil Vincent Sidgwick , segons la qual aquest enllaç difereix del covalent normal només en el fet que els dos electrons que el constitueixen procedeixen d’un sol dels dos àtoms que s’enllacen, la qual cosa permet d’explicar l’estructura electrònica d’alguns grups no saturats per exemple, -NO 2 de molècules orgàniques i inorgàniques, la dels complexos complex i la dels adductes formats per molècules neutres, l’una acceptora i l’altra donadora per exemple F 3 BNH 3 Segons la…
naftalè
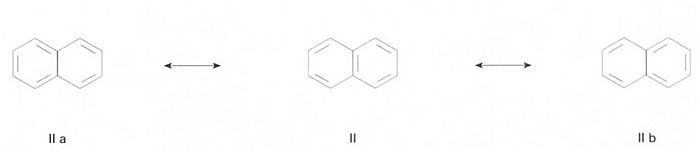
Naftalè
Química
Hidrocarbur aromàtic format per dos anells benzènics ajuntats.
Fou descobert i aïllat el 1856 en el quitrà, i la seva fórmula I, postulada per Erlenmeyer 1866, fou demostrada per CGraebe 1868 La fórmula II del naftalè es presenta abreujada, com en el cas del benzè Les posicions 1, 4, 5 i 8 i 2, 3, 6 i 7 són equivalents Hom anomena les primeres per la lletra α i les segones per la lletra β En una interpretació electrònica hom considera que l’estructura del naftalè és un híbrid de ressonància entre distintes estructures electròmeres Les més importants són la II, la IIa i la IIb, la II essent la més estable El naftalè es presenta en forma d’un sòlid blanc,…
enllaç de retrodonació
Química
Model teòric per a la interpretació de l’enllaç entre àtoms metàl·lics pesants de transició i molècules neutres, com ara el monòxid de carboni o una olefina.
En el cas d’una unió de tipus sigma σ entre el metall i la molècula, els orbitals n-1 d del metall tenen energies similars a les dels orbitals ns i np de la capa de valència i, per tant, poden participar en la formació d’enllaços Així, l’enllaç resultant pot considerar-se com a suma d’un enllaç sigma σ, originat per donació d’un parell electrònic no compartit del lligand a un orbital d buit i de simetria adient del metall, i d’una cessió de càrrega d’un orbital d ocupat del metall a un orbital antienllaçant π* desocupat del lligand neutre En el cas d’una unió de tipus pi π, opera un…
diborà
Química
Hidrur de bor de la sèrie dels borans que, com ells, presenta un dèficit d’electrons en l’estructura.
Hom admet que aquest compost disposa de 12 electrons de valència, quantitat suficient per a unir els sis hidrògens als àtoms de bor per enllaços covalents normals, no restant, però, cap electró per a l’enllaç bor-bor Per tal d’explicar aquest fet, el diborà ha estat molt estudiat La interpretació de les dades experimentals, sobretot espectroscòpiques, permet de suposar que el diborà presenta una estructura amb ponts d’hidrogen en la qual dos grups BHS22 són coplanaris i els dos hidrògens restants van disposats al mig, simètricament per sobre i per sota del pla Des del punt de…
termoquímica
Química
Denominació clàssica de la part de la termodinàmica que tracta de la mesura i de la interpretació dels canvis calorífics que acompanyen canvis d’estat o reaccions químiques.
Essencialment, consisteix en l’aplicació als sistemes químics del principi de la conservació de l’energia primer principi de la termodinàmica Des del punt de vista termoquímic, una reacció és exotèrmica quan té lloc amb alliberament de calor, i endotèrmica quan cal fornir-li calor perquè evolucioni Atès que l’energia interna d’un sistema és una funció d’estat, la mesura de les calors de reacció serà, sempre que no s’exerceixi cap treball positiu o negatiu, una mesura de la variació energètica del procés considerat Aquesta condició s’acompleix en els processos desenvolupats a volum constant,…
base
Química
Cadascuna de les substàncies caracteritzades químicament per les següents propietats:.
provocar el canvi de color o el viratge de determinades substàncies orgàniques, anomenades indicadors , o bé regenerar llur color primitiu quan aquest ha estat alterat prèviament pels àcids, i donar amb els àcids reaccions de neutralització en què es perden les propietats característiques d’ambdues classes de substàncies i es formen sals Trets organolèptics menys generals de les bases són llur sabor amarg i llur tacte untuós El concepte de base s’ha desenvolupat parallelament al d' àcid La primera teoria moderna que intentà de relacionar les propietats àcides o bàsiques amb la composició…